Αβακαβίρη
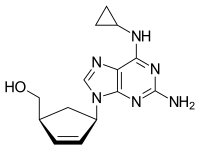 | |
 Χημική δομή της αβακαβίρης | |
| Ονομασία IUPAC | |
|---|---|
{(1S,4R)-4-[2-amino-6-(cyclopropylamino)-9H-purin-9-yl]cyclopent-2-en-1-yl}methanol | |
| Κλινικά δεδομένα | |
| Προφορά | |
| Εμπορικές ονομασίες | Ziagen, άλλα[1] |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a699012 |
| Δεδομένα άδειας | |
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Από το στόμα (σιρόπι ή δισκία) |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | 83% |
| Μεταβολισμός | Ήπαρ |
| Βιολογικός χρόνος ημιζωής | 1.54 ± 0.63 ώρες |
| Απέκκριση | Νεφροί (1.2% αβακαβίρη, 30% 5'-carboxylic acid metabolite, 36% 5'-glucuronide metabolite, 15% μη ταυτοποιημένοι μεταβολίτες). Κόπρανα (16%) |
| Χημικά στοιχεία | |
| Χημικός τύπος | C14H18N6O |
| Μοριακή μάζα | 286,34 g·mol−1 |
n3c1c(ncn1[C@H]2/C=C\[C@@H](CO)C2)c(nc3N)NC4CC4 | |
InChI=1S/C14H18N6O/c15-14-18-12(17-9-2-3-9)11-13(19-14)20(7-16-11)10-4-1-8(5-10)6-21/h1,4,7-10,21H,2-3,5-6H2,(H3,15,17,18,19)/t8-,10+/m1/s1 Key:MCGSCOLBFJQGHM-SCZZXKLOSA-N | |
| Φυσικά στοιχεία | |
| Σημείο τήξης | 165 °C (329 °F) |
| (verify) | |
Η αβακαβίρη, που είναι διαθέσιμη με την εμπορική ονομασία Ziagen, είναι ένα φάρμακο που χρησιμοποιείται για την πρόληψη και τη θεραπεία του HIV/AIDS.[1] [2] Όπως και οι άλλοι νουκλεοσιδικοί αναστολείς της αντίστροφης μεταγραφάσης (NRTIs), η αβακαβίρη χρησιμοποιείται σε συνδυασμό με άλλα φάρμακα για τον HIV και δεν συνιστάται η χρήση ως μονοθεραπεία.[3] Λαμβάνεται από το στόμα ως δισκίο ή σιρόπι και μπορεί να χρησιμοποιηθεί σε παιδιά ηλικίας άνω των τριών μηνών.[1][4]
Η αβακαβίρη είναι γενικά καλά ανεκτή.[4] Οι συχνότερες ανεπιθύμητες ενέργειες περιλαμβάνουν έμετο, προβλήματα με τον ύπνο, πυρετό και αίσθημα κόπωσης. [1] Πιο σοβαρές ανεπιθύμητες ενέργειες περιλαμβάνουν αντίδραση υπερευαισθησίας, ηπατική βλάβη και γαλακτική οξέωση.[1] Ο γενετικός έλεγχος μπορεί να δείξει εάν ένα άτομο διατρέχει υψηλότερο κίνδυνο να εκδηλώσει υπερευαισθησία.[1] Τα συμπτώματα της αντίδρασης υπερευαισθησίας περιλαμβάνουν εξάνθημα, έμετο και δύσπνοια.[4] Η αβακαβίρη ανήκει στην κατηγορία NRTI, φάρμακα που δρουν αναστέλλοντας την αντίστροφη μεταγραφάση, ένα ένζυμο που απαιτείται για την αναπαραγωγή του HIV.[5] Εντός της κατηγορίας των NRTI, η αβακαβίρη αποτελεί έναν καρβοκυκλικό νουκλεοσίδιο.[1]
Η αβακαβίρη κατοχυρώθηκε με δίπλωμα ευρεσιτεχνίας το 1988 και η χρήση της εγκρίθηκε στις Ηνωμένες Πολιτείες το 1998.[6][7] Περιλαμβάνεται στον Κατάλογο Βασικών Φαρμάκων του Παγκόσμιου Οργανισμού Υγείας.[8] Διατίθεται και ως γενόσημο φάρμακο.[1] Το κόστος χονδρικής στον αναπτυσσόμενο κόσμο το 2014 ήταν μεταξύ 0,36 και 0,83 δολαρίων ΗΠΑ ανά ημέρα.[9] Το 2016 το κόστος χονδρικής για ένα μήνα φαρμακευτικής αγωγής στις Ηνωμένες Πολιτείες ήταν 70,50 δολάρια ΗΠΑ.[10] Συνήθως, η αβακαβίρη πωλείται μαζί με άλλα φάρμακα για τον HIV, όπως αβακαβίρη/λαμιβουδίνη/ζιδοβουδίνη, αβακαβίρη/ντολουτεγκραβίρη/λαμιβουδίνη και αβακαβίρη/λαμιβουδίνη.[4][5] Ο συνδυασμός αβακαβίρης/λαμιβουδίνης περιλαμβάνεται επίσης στον κατάλογο βασικών φαρμάκων.[8]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 «Abacavir Sulfate». The American Society of Health-System Pharmacists. Αρχειοθετήθηκε από το πρωτότυπο στις 21 Αυγούστου 2017. Ανακτήθηκε στις 31 Ιουλίου 2015.
- ↑ «Drug Name Abbreviations Adult and Adolescent ARV Guidelines». AIDSinfo. Αρχειοθετήθηκε από το πρωτότυπο στις 9 Νοεμβρίου 2016. Ανακτήθηκε στις 8 Νοεμβρίου 2016.
- ↑ «What Not to Use Adult and Adolescent ARV Guidelines». AIDSinfo. Αρχειοθετήθηκε από το πρωτότυπο στις 9 Νοεμβρίου 2016. Ανακτήθηκε στις 8 Νοεμβρίου 2016.
- ↑ 4,0 4,1 4,2 4,3 «A review of the pharmacokinetics of abacavir.». Clinical Pharmacokinetics 47 (6): 351–71. 2008. doi:. PMID 18479171.
- ↑ 5,0 5,1 «Nucleoside reverse transcriptase inhibitors (NRTIs or 'nukes') - HIV/AIDS». www.hiv.va.gov. Αρχειοθετήθηκε από το πρωτότυπο στις 9 Νοεμβρίου 2016. Ανακτήθηκε στις 8 Νοεμβρίου 2016.
- ↑ Fischer, Janos· Ganellin, C. Robin (2006). Analogue-based Drug Discovery. John Wiley & Sons. σελ. 505. ISBN 9783527607495. Αρχειοθετήθηκε από το πρωτότυπο στις 8 Σεπτεμβρίου 2017.
- ↑ Kane, Brigid M. (2008). HIV/AIDS Treatment Drugs. Infobase Publishing. σελ. 56. ISBN 9781438102078. Αρχειοθετήθηκε από το πρωτότυπο στις 8 Σεπτεμβρίου 2017.
- ↑ 8,0 8,1 World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ «International Drug Price Indicator Guide». ERC. Αρχειοθετήθηκε από το πρωτότυπο στις 29 Μαρτίου 2019. Ανακτήθηκε στις 20 Νοεμβρίου 2016.
- ↑ «NADAC as of 2016-12-07 | Data.Medicaid.gov». Centers for Medicare and Medicaid Services. Αρχειοθετήθηκε από το πρωτότυπο στις 21 Δεκεμβρίου 2016. Ανακτήθηκε στις 12 Δεκεμβρίου 2016.
