Β κύτταρα
 Μικρογραφία ηλεκτρονικής διέλευσης ενός ανθρώπινου Β κυττάρου | |
| Σύστημα | Ανοσοποιητικό σύστημα |
|---|---|

Τα Β κύτταρα, επίσης γνωστά ως Β λεμφοκύτταρα, είναι τύπος λευκών αιμοσφαιρίων του υποτύπου λεμφοκυττάρων.[1] Λειτουργούν στη χημική ανοσία του προσαρμοστικού ανοσοποιητικού συστήματος.[1] Τα Β κύτταρα παράγουν μόρια αντισώματος. Ωστόσο, αυτά τα αντισώματα δεν εκκρίνονται. Μάλλον, εισάγονται στη πλασματική μεμβράνη όπου χρησιμεύουν ως μέρος των υποδοχέων Β κυττάρων.[2] Όταν ένα αφελές ή μνημονικό Β κύτταρο ενεργοποιείται από ένα αντιγόνο, πολλαπλασιάζεται και διαφοροποιείται σε ένα δραστικό κύτταρο που εκκρίνει αντισώματα, γνωστό ως πλασμαβλάστη ή πλασματοκύτταρο.[2] Επιπλέον, τα Β κύτταρα εμφανίζουν αντιγόνα (ταξινομούνται επίσης ως επαγγελματικά αντιγονοπαρουσιαστικά κύτταρα (APCs) και εκκρίνουν κυτοκίνες.[1] Στα θηλαστικά, τα Β κύτταρα ωριμάζουν στον μυελό των οστών, ο οποίος βρίσκεται στον πυρήνα των περισσότερων οστών.[3] Στα πτηνά, τα Β κύτταρα ωριμάζουν στο «θύλακα του Φαβρικίου» (λατ.: bursa Fabricii), ένα λεμφοειδές όργανο όπου ανακαλύφθηκαν για πρώτη φορά από τον Chang και τον Glick,[3] αυτός είναι ο λόγος για τον οποίο το «Β» σημαίνει θύλακας (λατ.: bursa) και όχι μυελός των οστών όπως κοινά πιστεύεται.
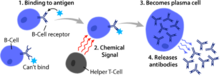
Τα Β κύτταρα, σε αντίθεση με τις άλλες δύο κατηγορίες λεμφοκυττάρων, Τ κύτταρα και τα φυσικά φονικά κύτταρα, εκφράζουν υποδοχείς κυττάρων Β (BCR) στην κυτταρική μεμβράνη τους.[1] Οι BCR επιτρέπουν στο Β κύτταρο να δεσμευτεί σε ένα συγκεκριμένο αντιγόνο, έναντι του οποίου θα ξεκινήσει μια αντίδραση αντισώματος.[1]
Ανάπτυξη[Επεξεργασία | επεξεργασία κώδικα]
Τα Β κύτταρα αναπτύσσονται από αιμοποιητικά βλαστοκύτταρα (HSCs) που προέρχονται από μυελό των οστών.[4][5] Τα HSCs πρώτα διαφοροποιούνται σε κύτταρα πολυδύναμων προγόνων (MPP), στη συνέχεια σε κύτταρα κοινών λεμφοειδών προγόνων (CLP).[5] Από εδώ, η ανάπτυξή τους σε Β κύτταρα συμβαίνει σε διάφορα στάδια (φαίνονται στην εικόνα προς τα δεξιά), καθένα από τα οποία χαρακτηρίζεται από διάφορα πρότυπα γονιδιακής έκφρασης και ρυθμίσεις γενετικών τόπων των αλυσίδων Η και L της ανοσοσφαιρίνης, που οφείλονται στα Β κύτταρα που υφίστανται ανασυνδυασμό V(D)J καθώς αναπτύσσονται.[6]

Τα Β κύτταρα υποβάλλονται σε δύο τύπους επιλογής ενώ αναπτύσσονται στο μυελό των οστών για να εξασφαλίσουν τη σωστή ανάπτυξη, και οι δύο περιλαμβάνουν υποδοχείς Β κυττάρων (BCR) στην επιφάνεια του κυττάρου. Η θετική επιλογή πραγματοποιείται μέσω σηματοδότησης ανεξάρτητης από αντιγόνο που περιλαμβάνει τόσο τον προ-BCR όσο και τον BCR. [7][8] Εάν αυτοί οι υποδοχείς δεν συνδέονται με τον συνδέτη τους, τα Β κύτταρα δεν λαμβάνουν τα κατάλληλα σήματα και παύουν να αναπτύσσονται.[7][8] Η αρνητική επιλογή συμβαίνει μέσω της σύνδεσης του αυτοαντιγόνου με το BCR. Εάν το BCR μπορεί να συνδεθεί ισχυρά με το αυτοαντιγόνο, τότε το Β κύτταρο υφίσταται μία από τις τέσσερις μοίρες: κλωνική απαλοιφή, επεξεργασία υποδοχέα, ανοσοαδράνεια ή άγνοια (το Β κύτταρο αγνοεί σήμα και συνεχίζει την ανάπτυξη).[8] Αυτή η αρνητική διαδικασία επιλογής οδηγεί σε μια κατάσταση κεντρικής ανοχής, στην οποία τα ώριμα Β κύτταρα δεν δεσμεύουν τα αυτοαντιγόνα που υπάρχουν στον μυελό των οστών.[6]
Για να ολοκληρωθεί η ανάπτυξη, τα ανώριμα Β κύτταρα μεταναστεύουν από το μυελό των οστών στη σπλήνα ως μεταβατικά Β κύτταρα, περνώντας από δύο μεταβατικά στάδια: Τ1 και Τ2.[9] Καθ 'όλη τη διάρκεια της μετανάστευσής τους στη σπλήνα και μετά την είσοδό τους στη σπλήνα, θεωρούνται Τ1 Β κύτταρα.[10] Μέσα στη σπλήνα, τα Τ1 Β κύτταρα μεταπίπτουν σε Τ2 Β κύτταρα.[10] Τα Τ2 Β κύτταρα διαφοροποιούνται είτε σε θυλακικοειδών (FO) Β κύτταρα είτε σε κύτταρα Β οριακής ζώνης (MZ) ανάλογα με τα σήματα που λαμβάνονται μέσω του BCR και άλλων υποδοχέων.[11] Μόλις διαφοροποιηθούν, τώρα θεωρούνται ώριμα Β κύτταρα ή αφελή Β κύτταρα.[10]

Ενεργοποίηση[Επεξεργασία | επεξεργασία κώδικα]

Η ενεργοποίηση των κυττάρων Β συμβαίνει στα δευτερογενή λεμφοειδή όργανα (SLOs), όπως στον σπλήνα και στους λεμφαδένες.[1] Αφού ωριμάσουν τα Β κύτταρα στο μυελό των οστών, μεταναστεύουν μέσω του αίματος σε SLOs, τα οποία λαμβάνουν σταθερή παροχή αντιγόνου μέσω της κυκλοφορίας της λέμφου.[12] Στο SLO, η ενεργοποίηση των Β κυττάρων ξεκινά όταν το Β κύτταρο συνδέεται με ένα αντιγόνο μέσω του BCR (υποδοχέα Β κυττάρων).[13] Αν και τα γεγονότα που λαμβάνουν χώρα αμέσως μετά την ενεργοποίηση δεν έχουν ακόμη προσδιοριστεί πλήρως, πιστεύεται ότι τα Β κύτταρα ενεργοποιούνται σύμφωνα με το πρότυπο του κινητικού διαχωρισμού, που αρχικά προσδιορίστηκε σε Τ λεμφοκύτταρα. Αυτό το πρότυπο υποδηλώνει ότι πριν από τη διέγερση του αντιγόνου, οι υποδοχείς διαχέονται μέσω της μεμβράνης και έρχονται σε επαφή με Lck και CD45 σε ίση συχνότητα, αποδίδοντας μια καθαρή ισορροπία φωσφορυλίωσης και μη φωσφορυλίωσης. Μόνο όταν το κύτταρο έρχεται σε επαφή με ένα αντιγονοπαρουσιαστικό κύτταρο, το μεγαλύτερο CD45 μετατοπίζεται λόγω της στενής απόστασης μεταξύ των δύο μεμβρανών. Αυτό επιτρέπει την καθαρή φωσφορυλίωση του BCR και την έναρξη της διαδρομής μεταγωγής του σήματος. Από τα τρία υποσύνολα Β κυττάρων, τα Β κύτταρα FO κατά προτίμηση υποβάλλονται σε Τ κύτταροεξαρτώμενη ενεργοποίηση ενώ τα ΜΖ Β κύτταρα και τα Β1 Β κύτταρα υπόκεινται κατά προτίμηση σε ανεξάρτητη ενεργοποίηση Τ κυττάρων.[14]
Η ενεργοποίηση των Β κυττάρων ενισχύεται μέσω της δραστηριότητας του CD21, ενός επιφανειακού υποδοχέα σε σύμπλοκο με τις επιφανειακές πρωτεΐνες CD19 και CD81 (και τα τρία είναι συλλογικά γνωστά ως σύμπλεγμα συνυποδοχέων Β κυττάρων ).[15] Όταν ένα BCR δεσμεύει ένα αντιγόνο επισημασμένο με ένα θραύσμα της πρωτεΐνης συμπληρώματος C3, το CD21 δεσμεύει το θραύσμα C3, συνδέεται με το δεσμευμένο BCR και τα σήματα μετάγονται μέσω CD19 και CD81 για να μειώσουν το κατώφλι ενεργοποίησης του κυττάρου. [16]
Ενεργοποίηση εξαρτώμενη από Τ κύτταρα[Επεξεργασία | επεξεργασία κώδικα]
Τα αντιγόνα που ενεργοποιούν τα Β κύτταρα με τη βοήθεια των Τ-κυττάρων είναι γνωστά ως αντιγόνα εξαρτώμενα από Τ κύτταρα (TD) και περιλαμβάνουν ξένες πρωτεΐνες.[1] Ονομάζονται έτσι επειδή δεν είναι σε θέση να προκαλέσουν χυμική αντίδραση σε οργανισμούς που στερούνται Τ κυττάρων.[1] Οι αποκρίσεις των Β κυττάρων σε αυτά τα αντιγόνα διαρκούν πολλές ημέρες, αν και τα αντισώματα που δημιουργούνται έχουν μεγαλύτερη συγγένεια και είναι πιο λειτουργικά πολυχρηστικά από αυτά που δημιουργούνται από ανεξάρτητη ενεργοποίηση των Τ κυττάρων[1]
Μόλις ένα BCR (υποδοχέας Β κυττάρων) δεσμεύσει ένα αντιγόνο TD, το αντιγόνο μεταφέρεται στο Β κύτταρο μέσω ενδοκυττάρωσης από υποδοχείς, υποβάθμισης και παρουσίασης στα Τ κύτταρα ως πεπτιδικά τεμάχια σε σύμπλοκο με MHC (μείζον σύμπλεγμα ιστοσυμβατότητας)-II μόρια στην κυτταρική μεμβράνη.[17] Τα βοηθητικά Τ κύτταρα (TH), συνήθως θυλακοειδή βοηθητικά Τ κύτταρα (TFH) αναγνωρίζουν και δεσμεύουν αυτά τα σύμπλοκα MHC-II-πεπτιδίου μέσω των υποδοχέων Τ κυττάρων (TCR).[18] Μετά τη δέσμευση του TCR-MHC-II-πεπτιδίου, τα Τ κύτταρα εκφράζουν την επιφανειακή πρωτεΐνη CD40L καθώς και κυτοκίνες όπως IL-4 και IL-21.[18] Το CD40L χρησιμεύει ως απαραίτητος συνδιεγερτικός παράγοντας για την ενεργοποίηση των Β κυττάρων συνδέοντας τον υποδοχέα της επιφάνειας των Β κυττάρων CD40, ο οποίος προάγει τον πολλαπλασιασμό των Β κυττάρων, την εναλλαγή τάξης της ανοσοσφαιρίνης, και τη σωματική υπερμετάλλαξη και διατηρεί την ανάπτυξη και τη διαφοροποίηση των Τ κυττάρων.[1] Οι προερχόμενες κυτοκίνες από τα Τ κύτταρα που δεσμεύονται από τους υποδοχείς κυτοκινών των Β κυττάρων προάγουν επίσης τον πολλαπλασιασμό των Β κυττάρων, την αλλαγή τάξης ανοσοσφαιρίνης και τη σωματική υπερμετάλλαξη, καθώς και τη διαφοροποίηση.[18] Αφού τα κύτταρα Β λάβουν αυτά τα σήματα, θεωρούνται ενεργοποιημένα.[18]

Μόλις ενεργοποιηθούν, τα Β κύτταρα συμμετέχουν σε μια διαδικασία διαφοροποίησης δύο σταδίων που αποδίδει τόσο βραχύβιους πλασμαβλάστες για άμεση προστασία όσο και μακροχρόνια κύτταρα πλάσματος και Β κύτταρα μνήμης για σταθερή προστασία.[14] Το πρώτο βήμα, γνωστό ως εξωθυλακική απόκριση, συμβαίνει έξω από τα λεμφοειδή θυλάκια, αλλά εξακολουθεί να βρίσκεται στο SLO (δευτερογενές λεμφοειδές όργανο).[14] Κατά τη διάρκεια αυτού του σταδίου τα ενεργοποιημένα Β κύτταρα πολλαπλασιάζονται, μπορεί να υποστούν αλλαγή τάξης ανοσοσφαιρίνης και να διαφοροποιηθούν σε πλασμαβλάστες που παράγουν πρώιμα, ασθενή αντισώματα κυρίως της κατηγορίας IgM.[19] Το δεύτερο βήμα αποτελείται από ενεργοποιημένα Β κύτταρα που εισέρχονται σε ένα λεμφοειδές θυλάκιο και σχηματίζουν ένα βλαστικό κέντρο (germinal center (GC)), το οποίο είναι ένα εξειδικευμένο μικροπεριβάλλον όπου τα Β κύτταρα υφίστανται εκτεταμένο πολλαπλασιασμό, αλλαγή τάξης ανοσοσφαιρίνης και ωρίμανση συγγένειας που κατευθύνεται από σωματική υπερμετάλλαξη.[20] Αυτές οι διεργασίες διευκολύνονται από τα ΤFH κύτταρα εντός του GC και παράγουν τόσο Β-κύτταρα μνήμης υψηλής συγγένειας όσο και μακροχρόνια πλασματοκύτταρα.[14] Τα πλασματοκύτταρα που προκύπτουν εκκρίνουν μεγάλες ποσότητες αντισωμάτων και είτε παραμένουν εντός της SLO είτε, προτιμότερα, μεταναστεύουν στον μυελό των οστών.[20]
Ενεργοποίηση ανεξάρτητη από Τ κύτταρα[Επεξεργασία | επεξεργασία κώδικα]
Τα αντιγόνα που ενεργοποιούν τα Β κύτταρα χωρίς τη βοήθεια των Τ κυττάρων είναι γνωστά ως αντιγόνα ανεξάρτητα από τα Τ κύτταρα (ΤΙ)[1] και περιλαμβάνουν ξένους πολυσακχαρίτες και μη μεθυλιωμένο CpG DNA.[14] Ονομάζονται έτσι επειδή είναι σε θέση να προκαλέσουν χυμική αντίδραση σε οργανισμούς που στερούνται Τ κυττάρων.[1] Η απόκριση των Β κυττάρων σε αυτά τα αντιγόνα είναι ταχεία, αν και τα αντισώματα που παράγονται τείνουν να έχουν χαμηλότερη συγγένεια και είναι λιγότερο ευέλικτα λειτουργικά από αυτά που δημιουργούνται από την ενεργοποίηση που εξαρτάται από τα Τ κύτταρα.[1]
Όπως και με τα αντιγόνα TD, τα Β κύτταρα που ενεργοποιούνται από τα αντιγόνα ΤΙ χρειάζονται επιπλέον σήματα για να ολοκληρώσουν την ενεργοποίηση, αλλά αντί να τα λαμβάνουν από τα Τ κύτταρα, αυτά παρέχονται είτε με αναγνώριση και σύνδεση ενός κοινού μικροβιακού συστατικού με υποδοχείς τύπου toll (TLR) ή με εκτεταμένη διασταύρωση των BCR (υποδοχείς Β κυττάρων) με επαναλαμβανόμενους επιτόπους σε ένα βακτηριακό κύτταρο.[1] Τα Β κύτταρα που ενεργοποιούνται από τα αντιγόνα TI συνεχίζουν να πολλαπλασιάζονται έξω από τα λεμφοειδή θυλάκια αλλά εξακολουθούν να βρίσκονται σε SLOs (οι GC δεν σχηματίζονται), ενδεχομένως υποβάλλονται σε αλλαγή τάξης ανοσοσφαιρίνης και διαφοροποιούνται σε βραχύβιους πλασμαβλάστες που παράγουν πρώιμα, αδύναμα αντισώματα κυρίως της κατηγορίας IgM, αλλά και ορισμένους πληθυσμούς μακρόβιων πλασματοκυττάρων.[21]
Ενεργοποίηση μνημονικών Β κυττάρων[Επεξεργασία | επεξεργασία κώδικα]
Η ενεργοποίηση των μνημονικών Β κυττάρων ξεκινά με την ανίχνευση και τη δέσμευση του αντιγόνου στόχου τους, το οποίο μοιράζεται το γονικό τους Β κύτταρο.[22] [23] Κατά τη δέσμευση αντιγόνου, το μνημονικό Β κύτταρο αναλαμβάνει το αντιγόνο μέσω ενδοκυττάρωσης που μεσολαβείται από υποδοχέα, το υποβαθμίζει και το παρουσιάζει στα Τ κύτταρα ως πεπτιδικά τεμάχια σε σύμπλοκο με μόρια MHC-II στην κυτταρική μεμβράνη.[22] Τα μνημονικά βοηθητικά Τ κύτταρα (TH), τυπικά μνημονικά θυλακοειδή βοηθητικά Τ κύτταρα (TFH), που προέρχονται από ενεργοποιημένα Τ κύτταρα με το ίδιο αντιγόνο αναγνωρίζουν και δεσμεύουν αυτά τα σύμπλοκα MHC-II-πεπτίδιο μέσω του TCR τους.[22] Μετά τη δέσμευση του TCR-MHC-II-πεπτιδίου και τη μετάδοση άλλων σημάτων από το μνημονικό Τ κύτταρο TFH, το Β κύτταρο μνήμης ενεργοποιείται και διαφοροποιείται είτε σε πλασμαβλάστες όσο και σε πλασμοκύτταρα μέσω μιας εξωθυλικοειδούς απόκρισης ή εισάγεται μια βλαστική αντίδραση κέντρου, όπου δημιουργούν πλασμοκύτταρα και περισσότερα μνημονικά Β κύτταρα[22][23] Δεν είναι σαφές εάν τα Β κύτταρα μνήμης υφίστανται περαιτέρω ωρίμανση συγγένειας εντός αυτών των δευτερογενών GC.[22]
Τύποι Β κυττάρων[Επεξεργασία | επεξεργασία κώδικα]
- Πλασμαβλάστες - Βραχύβια, πολλαπλασιαζόμενα κύτταρα που εκκρίνουν αντισώματα που προκύπτουν από τη διαφοροποίηση των Β κυττάρων.[1] Οι πλασμαβλάστες δημιουργούνται νωρίς σε μια λοίμωξη και τα αντισώματα τους τείνουν να έχουν ασθενέστερη συγγένεια προς το αντιγόνο-στόχο τους σε σύγκριση με τα πλασμοκύτταρα.[14] Οι πλασμαβλάστες μπορούν να προκύψουν από την ενεργοποίηση Β κυττάρων ανεξάρτητων από τα Τ κύτταρα ή την εξωθυλακοειδή απόκριση της ενεργοποίησης των Β κυττάρων που εξαρτώνται από τα Τ κύτταρα.[1]
- Πλασμοκύτταρα - Μακρόβια, μη πολλαπλασιαζόμενα κύτταρα που εκκρίνουν αντισώματα που προκύπτουν από τη διαφοροποίηση των κυττάρων Β.[1] Υπάρχουν ενδείξεις ότι τα Β κύτταρα αρχικά διαφοροποιούνται σε κύτταρα που μοιάζουν με πλασμαβλάστες και στη συνέχεια διαφοροποιούνται σε πλασματοκύτταρα.[14] Τα πλασματοκύτταρα δημιουργούνται αργότερα σε λοίμωξη και σε σύγκριση με τους πλασμαβλάστες, έχουν αντισώματα με μεγαλύτερη συγγένεια προς το αντιγόνο-στόχο τους λόγω της ωρίμανσης της συγγένειας στο βλαστικό κέντρο (GC) και παράγουν περισσότερα αντισώματα.[14] Τα πλασματοκύτταρα τυπικά προκύπτουν από την αντίδραση του βλαστικού κέντρου από την εξαρτώμενη από Τ κύτταρα ενεργοποίηση Β κυττάρων, ωστόσο μπορούν επίσης να προκύψουν από ανεξάρτητη από Τ κύτταρα ενεργοποίηση Β κυττάρων.[21]
- Λεμφοπλασματοκυτταροειδή κύτταρα - Κύτταρα με μίγμα μορφολογικών χαρακτηριστικών λεμφοκυττάρων Β και πλασματοκυττάρων που πιστεύεται ότι σχετίζεται στενά με έναν υποτύπο πλασματοκυττάρων. Αυτός ο τύπος κυττάρου βρίσκεται σε προ-κακοήθεις και κακοήθεις κυτταροπλασματικές δυσκρασίες που σχετίζονται με την έκκριση μονοκλωνικών πρωτεϊνών IgM. Αυτές οι δυσκρασίες περιλαμβάνουν μονοκλωνική γαμμαπάθεια IgM απροσδιόριστης σημασίας και μακροσφαιριναιμία του Waldenström.[24]
- Κύτταρα μνήμης Β - Λανθάνοντα Β κύτταρα που προκύπτουν από τη διαφοροποίηση των Β κυττάρων.[1] Η λειτουργία τους είναι να κυκλοφορούν στο σώμα και να ενεργοποιούν μια ισχυρότερη, ταχύτερη απόκριση αντισωμάτων (γνωστή ως αναμνηστική δευτερογενής αντισωματική απόκριση) εάν εντοπίσουν το αντιγόνο που είχε ενεργοποιήσει το γονικό τους κύτταρο Β (τα Β κύτταρα μνήμης και τα γονικά Β κύτταρά τους μοιράζονται τον ίδιο BCR (υποδοχέα Β κυττάρων), έτσι ανιχνεύουν το ίδιο αντιγόνο).[23] Τα Β κύτταρα μνήμης μπορούν να δημιουργηθούν από την εξαρτώμενη από Τ κύτταρα ενεργοποίηση τόσο μέσω της εξωθυλακικής απόκρισης όσο και της αντίδρασης του βλαστικού κέντρου, καθώς και από την ανεξάρτητη από τα Τ κύτταρα ενεργοποίηση των Β1 κυττάρων.[23]
- Κύτταρο Β-2 - FO Β κύτταρα και κύτταρα ΜΖ Β κύτταρα[25]
- Τα θυλακοειδή Β κύτταρα (επίσης γνωστά ως κύτταρα Β-2)-Ο πιο κοινός τύπος Β κυττάρου και όταν δεν κυκλοφορεί μέσω του αίματος, βρίσκεται κυρίως στα λεμφοειδή θυλάκια των δευτερογενών λεμφοειδών οργάνων (SLOs).[14] Είναι υπεύθυνα για τη δημιουργία της πλειοψηφίας των αντισωμάτων υψηλής συγγένειας κατά τη διάρκεια μιας μόλυνσης.[1]
- Β κύτταρα οριακής ζώνης (Marginal zone (MZ) B cells) -Βρίσκονται κυρίως στην οριακή ζώνη της σπλήνας και χρησιμεύουν ως η πρώτη γραμμή άμυνας έναντι των παθογόνων που μεταφέρονται από το αίμα, καθώς η περιθωριακή ζώνη λαμβάνει μεγάλες ποσότητες αίματος από τη γενική κυκλοφορία.[26] Μπορούν να υποστούν ενεργοποίηση τόσο ανεξάρτητη, όσο και εξαρτώμενη από Τ κύτταρα, αλλά κατά προτίμηση ενεργοποιούνται ανεξάρτητα από Τ κύτταρα.[14]
- Β-1 Κύτταρα - Προέρχονται από μια αναπτυξιακή οδό διαφορετική από τα FO Β κύτταρα και τα ΜΖ Β κύτταρα.[25] Στα ποντίκια, κυριαρχούν κυρίως στην περιτοναϊκή και την υπεζωκοτική κοιλότητα, παράγουν φυσικά αντισώματα (αντισώματα που παράγονται χωρίς μόλυνση), αμύνονται έναντι παθογόνων βλεννογόνων και εμφανίζουν κυρίως ενεργοποίηση ανεξάρτητη από τα Τ κύτταρα.[25] Πραγματικό ομόλογο Β-1 κυττάρων ποντικού δεν έχει ανακαλυφθεί στους ανθρώπους, αν και έχουν περιγραφεί διάφοροι πληθυσμοί κυττάρων παρόμοιοι με τα κύτταρα Β-1.[25]
- Ρυθμιστικά κύτταρα Β (Breg) - Ένας ανοσοκατασταλτικός τύπος κυττάρου Β που σταματά την επέκταση παθογόνων, προφλεγμονωδών λεμφοκυττάρων μέσω της έκκρισης IL-10, IL-35 και TGF-β.[27] Επίσης, προωθεί τη δημιουργία ρυθμιστικών Τ κυττάρων (Treg) αλληλεπιδρώντας άμεσα με Τ κύτταρα για να στρέψει τη διαφοροποίησή τους προς τα Tregs.[27] Δεν έχει περιγραφεί κοινή ταυτότητα κυττάρων Breg και δεν έχουν βρεθεί πολλά υποσύνολα κυττάρων Breg που να μοιράζονται ρυθμιστικές λειτουργίες τόσο σε ποντίκια όσο και σε ανθρώπους.[27] Προς το παρόν είναι άγνωστο εάν τα υποσύνολα κυττάρων Breg συνδέονται αναπτυξιακά και πώς ακριβώς γίνεται η διαφοροποίηση σε κύτταρα Breg.[27] Υπάρχουν στοιχεία που δείχνουν ότι σχεδόν όλοι οι τύποι Β κυττάρων μπορούν να διαφοροποιηθούν σε κύτταρα Breg μέσω μηχανισμών που περιλαμβάνουν φλεγμονώδη σήματα και αναγνώριση BCR.[27]
Παθολογία που σχετίζεται με τα Β κύτταρα[Επεξεργασία | επεξεργασία κώδικα]
Η αυτοάνοση ασθένεια μπορεί να προκύψει από την ανώμαλη αναγνώριση των Β κυττάρων των αυτοαντιγόνων που ακολουθείται από την παραγωγή αυτοαντισωμάτων.[28] Τα αυτοάνοσα νοσήματα όπου η δραστηριότητα της νόσου συσχετίζεται με τη δραστηριότητα των Β κυττάρων περιλαμβάνουν σκληροδερμία, πολλαπλή σκλήρυνση, συστηματικό ερυθηματώδη λύκο, διαβήτη τύπου 1, μεταλοιμώδης IBS και ρευματοειδή αρθρίτιδα.[28]
Κακοήθης μετασχηματισμός των Β κυττάρων και των προδρόμων τους μπορεί να προκαλέσουν ένα πλήθος καρκίνων, που συμπεριλαμβάνουν χρόνια λεμφοκυτταρική λευχαιμία (CLL), οξεία λεμφοβλαστική λευχαιμία (ALL), λευχαιμία τριχωτών κυττάρων, θυλακοειδές λέμφωμα, λέμφωμα μη Hodgkin, λέμφωμα Hodgkin και κακοήθειες των πλασματοκυττάρων όπως πολλαπλό μυέλωμα, μακροσφαιριναιμία του Waldenström και ορισμένες μορφές αμυλοείδωσης.[29][30]
Επιγενετική[Επεξεργασία | επεξεργασία κώδικα]
Μια μελέτη που διερεύνησε το μεθύλωμα των Β κυττάρων κατά τον κύκλο διαφοροποίησής τους, χρησιμοποιώντας την αλληλουχία διθειώδους όλου του γονιδιώματος (WGBS), έδειξε ότι υπάρχει υπομεθυλίωση από τα πρώτα στάδια έως τα πιο διαφοροποιημένα στάδια. Η μεγαλύτερη διαφορά μεθυλίωσης είναι μεταξύ των σταδίων των βλαστικών κέντρων Β κυττάρων και των Β κυττάρων μνήμης. Επιπλέον, αυτή η μελέτη έδειξε ότι υπάρχει ομοιότητα μεταξύ των όγκων Β κυττάρων και των μακρόβιων Β κυττάρων στις υπογραφές τους στη μεθυλίωση του DNA.[31]
References[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 1,17 1,18 Murphy, Kenneth (2012). Janeway's Immunobiology (8th έκδοση). New York: Garland Science. ISBN 9780815342434.
- ↑ 2,0 2,1 Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002). «B Cells and Antibodies» (στα αγγλικά). Molecular Biology of the Cell. 4th edition. https://www.ncbi.nlm.nih.gov/books/NBK26884/.
- ↑ 3,0 3,1 Cooper, Max D. (2015-01-01). «The early history of B cells». Nature Reviews Immunology 15 (3): 191–7. doi:. PMID 25656707.
- ↑ «Cell Fate Decisions: The Role of Transcription Factors in Early B-cell Development and Leukemia». Blood Cancer Discovery 1: 224–233. November 2020. doi:.
- ↑ 5,0 5,1 Kondo, Motonari (2010-11-01). «Lymphoid and myeloid lineage commitment in multipotent hematopoietic progenitors». Immunological Reviews 238 (1): 37–46. doi:. ISSN 1600-065X. PMID 20969583.
- ↑ 6,0 6,1 Pelanda, Roberta; Torres, Raul M. (2012-04-01). «Central B-Cell Tolerance: Where Selection Begins». Cold Spring Harbor Perspectives in Biology 4 (4): a007146. doi:. ISSN 1943-0264. PMID 22378602.
- ↑ 7,0 7,1 Martensson, Inga-Lill; Almqvist, Nina; Grimsholm, Ola; Bernardi, Angelina (2010). «The pre-B cell receptor checkpoint». FEBS Letters 584 (12): 2572–9. doi:. PMID 20420836.
- ↑ 8,0 8,1 8,2 LeBien, Tucker W.; Tedder, Thomas F. (2008-09-01). «B lymphocytes: how they develop and function». Blood 112 (5): 1570–1580. doi:. ISSN 0006-4971. PMID 18725575.
- ↑ Loder, Florienne; Mutschler, Bettina; Ray, Robert J.; Paige, Christopher J.; Sideras, Paschalis; Torres, Raul; Lamers, Marinus C.; Carsetti, Rita (1999-07-01). «B Cell Development in the Spleen Takes Place in Discrete Steps and Is Determined by the Quality of B Cell Receptor–Derived Signals». The Journal of Experimental Medicine 190 (1): 75–90. doi:. ISSN 0022-1007. PMID 10429672.
- ↑ 10,0 10,1 10,2 Chung, James B.; Silverman, Michael; Monroe, John G. (2003-01-06). «Transitional B cells: step by step towards immune competence». Trends in Immunology 24 (6): 342–348. doi:. ISSN 1471-4906. PMID 12810111.
- ↑ Cerutti, Andrea; Cols, Montserrat; Puga, Irene (2013-01-01). «Marginal zone B cells: virtues of innate-like antibody-producing lymphocytes». Nature Reviews Immunology 13 (2): 118–32. doi:. PMID 23348416.
- ↑ Harwood, Naomi E.; Batista, Facundo D. (2010-01-01). «Early Events in B Cell Activation». Annual Review of Immunology 28 (1): 185–210. doi:. PMID 20192804.
- ↑ Yuseff, Maria-Isabel; Pierobon, Paolo; Reversat, Anne; Lennon-Duménil, Ana-Maria (2013-01-01). «How B cells capture, process and present antigens: a crucial role for cell polarity». Nature Reviews Immunology 13 (7): 475–86. doi:. PMID 23797063.
- ↑ 14,00 14,01 14,02 14,03 14,04 14,05 14,06 14,07 14,08 14,09 Nutt, Stephen L.; Hodgkin, Philip D.; Tarlinton, David M.; Corcoran, Lynn M. (2015-01-01). «The generation of antibody-secreting plasma cells». Nature Reviews Immunology 15 (3): 160–71. doi:. PMID 25698678.
- ↑ Asokan, Rengasamy; Banda, Nirmal K.; Szakonyi, Gerda; Chen, Xiaojiang S.; Holers, V. Michael (2013-01-01). «Human complement receptor 2 (CR2/CD21) as a receptor for DNA: Implications for its roles in the immune response and the pathogenesis of systemic lupus erythematosus (SLE)». Molecular Immunology 53 (1–2): 99–110. doi:. PMID 22885687.
- ↑ Zabel, Mark D.; Weis, John H. (2001-03-01). «Cell-specific regulation of the CD21 gene». International Immunopharmacology. Unraveling Mechanisms and Discovering Novel Roles for Complement 1 (3): 483–493. doi:. PMID 11367532.
- ↑ Blum, Janice S.; Wearsch, Pamela A.; Cresswell, Peter (2013-01-01). «Pathways of Antigen Processing». Annual Review of Immunology 31 (1): 443–473. doi:. PMID 23298205.
- ↑ 18,0 18,1 18,2 18,3 Crotty, Shane (2015-01-01). «A brief history of T cell help to B cells». Nature Reviews Immunology 15 (3): 185–9. doi:. PMID 25677493.
- ↑ MacLennan, Ian C. M.; Toellner, Kai-Michael; Cunningham, Adam F.; Serre, Karine; Sze, Daniel M.-Y.; Zúñiga, Elina; Cook, Matthew C.; Vinuesa, Carola G. (2003-08-01). «Extrafollicular antibody responses». Immunological Reviews 194: 8–18. doi:. ISSN 0105-2896. PMID 12846803.
- ↑ 20,0 20,1 Shlomchik, Mark J.; Weisel, Florian (2012-05-01). «Germinal center selection and the development of memory B and plasma cells». Immunological Reviews 247 (1): 52–63. doi:. ISSN 1600-065X. PMID 22500831. https://zenodo.org/record/1064236.
- ↑ 21,0 21,1 Bortnick, Alexandra; Chernova, Irene; Quinn, William J.; Mugnier, Monica; Cancro, Michael P.; Allman, David (2012-06-01). «Long-Lived Bone Marrow Plasma Cells Are Induced Early in Response to T Cell-Independent or T Cell-Dependent Antigens». The Journal of Immunology 188 (11): 5389–5396. doi:. ISSN 0022-1767. PMID 22529295.
- ↑ 22,0 22,1 22,2 22,3 22,4 McHeyzer-Williams, Michael; Okitsu, Shinji; Wang, Nathaniel; McHeyzer-Williams, Louise (2011-01-01). «Molecular programming of B cell memory». Nature Reviews Immunology 12 (1): 24–34. doi:. PMID 22158414.
- ↑ 23,0 23,1 23,2 23,3 Kurosaki, Tomohiro; Kometani, Kohei; Ise, Wataru (2015-01-01). «Memory B cells». Nature Reviews Immunology 15 (3): 149–59. doi:. PMID 25677494.
- ↑ «Plasma cell morphology in multiple myeloma and related disorders». Morphologie: Bulletin de l'Association des Anatomistes 99 (325): 38–62. 2015. doi:. PMID 25899140.
- ↑ 25,0 25,1 25,2 25,3 Baumgarth, Nicole (2010-01-01). «The double life of a B-1 cell: self-reactivity selects for protective effector functions». Nature Reviews Immunology 11 (1): 34–46. doi:. PMID 21151033.
- ↑ Pillai, Shiv; Cariappa, Annaiah; Moran, Stewart T. (2005-01-01). «Marginal Zone B Cells». Annual Review of Immunology 23 (1): 161–196. doi:. PMID 15771569.
- ↑ 27,0 27,1 27,2 27,3 27,4 Rosser, Elizabeth C.; Mauri, Claudia (2015). «Regulatory B Cells: Origin, Phenotype, and Function». Immunity 42 (4): 607–612. doi:. ISSN 1074-7613. PMID 25902480.
- ↑ 28,0 28,1 Yanaba, Koichi; Bouaziz, Jean-David; Matsushita, Takashi; Magro, Cynthia M.; St.Clair, E. William; Tedder, Thomas F. (2008-06-01). «B-lymphocyte contributions to human autoimmune disease». Immunological Reviews 223 (1): 284–299. doi:. ISSN 1600-065X. PMID 18613843.
- ↑ III, Arthur L. Shaffer; Young, Ryan M.; Staudt, Louis M. (2012-01-01). «Pathogenesis of Human B Cell Lymphomas». Annual Review of Immunology 30 (1): 565–610. doi:. PMID 22224767.
- ↑ «Plasma Cell Disorders». Primary Care 43 (4): 677–691. 2016. doi:. PMID 27866585.
- ↑ Kulis, Marta; Merkel, Angelika; Heath, Simon; Queirós, Ana C.; Schuyler, Ronald P.; Castellano, Giancarlo; Beekman, Renée; Raineri, Emanuele και άλλοι. (2015-07-01). «Whole-genome fingerprint of the DNA methylome during human B cell differentiation» (στα αγγλικά). Nature Genetics 47 (7): 746–756. doi:. ISSN 1061-4036. PMID 26053498.
|
