Κίρρωση
| Κίρρωση | |
|---|---|
 Διατομή πτωματικού παρασκευάσματος - ήπαρ με κίρρωση | |
| Ειδικότητα | γαστρεντερολογία και ηπατολογία |
| Ταξινόμηση | |
| ICD-10 | K70.3, K71.7, K74 |
| ICD-9 | 571 |
| MedlinePlus | 000255 |
| eMedicine | med/3183 radio/175 |
| MeSH | D008103 |
Η κίρρωση είναι η ιστοπαθολογική συνέπεια της χρόνιας ηπατικής νόσου. Χαρακτηρίζεται από αντικατάσταση του ηπατικού παρεγχύματος από ουλώδη ιστό και αναγεννητικά οζίδια («εξογκώματα» που εμφανίζονται ως αποτέλεσμα αναγέννησης κατεστραμμένου ιστού ),[1][2][3] και οδηγεί σε ηπατική ανεπάρκεια. Η κίρρωση πιο συχνά προκαλείται από χρόνιο αλκοολισμό, ηπατίτιδα Β, ηπατίτιδα C, λιπώδη διήθηση του ήπατος, ιδιοπαθή αιτία (δηλ. από άγνωστη αιτία) αλλά και από πολλές άλλες πιθανές αιτίες.
Ο ασκίτης (συλλογή ελεύθερου υγρού στην περιτοναϊκή κοιλότητα[4]) είναι η πιο κοινή επιπλοκή της κίρρωσης, και σχετίζεται με αυξημένο κίνδυνο λοίμωξης με κακή ποιότητα ζωής και κακή μακροχρόνια πρόβλεψη. Άλλες δυνητικά απειλητικές για τη ζωή επιπλοκές είναι: η ηπατική εγκεφαλοπάθεια (με συμπτώματα από σύγχυση μέχρι κώμα) και οι κιρσοί οισοφάγου (προκαλείται συχνά αιμορραγία του ανώτερου πεπτικού συστήματος). Η κίρρωση είναι γενικά μη αναστρέψιμη, και η θεραπεία εστιάζεται συνήθως στην πρόληψη της εξέλιξης και των επιπλοκών. Σε προχωρημένα στάδια της κίρρωσης η μόνη λύση είναι η μεταμόσχευση ήπατος.

Η λέξη «κίρρωση» προέρχεται από το αρχαιοελληνικό κιρρός (:κιτρινωπός, καστανόξανθος) από το κίτρινο χρώμα του ασθενούς με ίκτερο, συνηθισμένη επιπλοκή της ηπατικής ανεπάρκειας. Η κλινική εικόνα ήταν γνωστή από πριν, αλλά η ονομασία «κίρρωση» δόθηκε από τον René Laennec το 1819 (στο έργο του επίσης περιγράφει και το στηθοσκόπιο).[5]
Επιδημιολογία[Επεξεργασία | επεξεργασία κώδικα]

Η κίρρωση και η χρόνια ηπατική νόσος ήταν η 10η κύρια αιτία θανάτου για τους άνδρες και η 12η για τις γυναίκες στις Ηνωμένες Πολιτείες το 2001, σκοτώνοντας περίπου 27.000 ανθρώπους κάθε χρόνο.[7] Επίσης, το κόστος της κίρρωσης από την άποψη του ανθρώπινου πόνου, των νοσοκομειακών δαπανών, και την απώλεια της παραγωγικότητας είναι υψηλό.
Η υπάρχουσα κίρρωση έχει 10-ετή θνησιμότητα σε ποσοστό 34-66%, και σε μεγάλο βαθμό εξαρτάται από την αιτία της κίρρωσης. Η αλκοολική κίρρωση έχει χειρότερη πρόγνωση από τη πρωτοπαθή χολική κίρρωση και αυτήν που οφείλεται στον ιό της ηπατίτιδας. Ο κίνδυνος θανάτου από όλες τις αιτίες αυξάνεται στο δωδεκαπλάσιο, ενώ αν εξαιρέσουμε τις άμεσες συνέπειες της νόσου του ήπατος, εξακολουθεί να υπάρχει μια πενταπλάσια αύξηση της θνησιμότητας σε όλες τις κατηγορίες ασθενών.[8]
Λίγα είναι γνωστά σχετικά με τους προδιαθεσιακούς παράγοντες της κίρρωσης, εκτός από τις άλλες ασθένειες που προκαλούν ηπατική βλάβη (όπως το ότι ο συνδυασμός της αλκοολικής ηπατικής νόσου και της χρόνιας ιογενούς ηπατίτιδας, οι οποίες μπορεί να ενεργούν συνεργικά και να οδηγούν σε κίρρωση). Μελέτες έχουν πρόσφατα προτείνει ότι η κατανάλωση καφέ μπορεί να προστατεύσει από κίρρωση του ήπατος, ειδικά στην αλκοολική κίρρωση.[9]
Συμπτωματολογία[Επεξεργασία | επεξεργασία κώδικα]
Μερικά από τα ακόλουθα συμπτώματα μπορεί να εμφανιστούν με την παρουσία της κίρρωσης ή ως αποτέλεσμα των επιπλοκών της κίρρωσης. Πολλά είναι μη ειδικά και μπορεί να υπάρχουν και σε άλλες ασθένειες (δεν είναι απαραίτητη ένδειξη για κίρρωση). Ομοίως, η απουσία κάποιου συμπτώματος από τα παρακάτω δεν αποκλείει την πιθανότητα της κίρρωσης.
- Αραχνοειδή αγγειώματα: Αγγειακές βλάβες, λόγω αύξησης της οιστραδιόλης, που αποτελούνται από ένα κεντρικό αρτηρίδιο που περιβάλλεται από πολλά μικρότερα αγγεία[ σε περίπου 1/3 των περιπτώσεων].[10]

- Ηπατικές παλάμες: Το θέναρ και οπισθέναρ εμφανίζεται εξέρυθρο μαζί με μικρές ωχρότερες κηλίδες.
- μεταβολές στους όνυχες (νύχια):
- γραμμές Μέρκε (Muehrcke's lines): Ζεύγη οριζόντιων γραμμών που χωρίζονται από κανονικό χρώμα, προκύπτουν από υπολευκωματιναιμία (ανεπαρκής παραγωγή αλβουμίνης).
- ονυχές τύπου Τέρι (Terry’s nails): Τα εγγύς δύο τρίτα του νυχιού εμφανίζονται λευκά και το άπω ένα τρίτο ερυθρό, επίσης λόγω της υπολευκωματιναιμίας.
- πληκτροδακτυλία: Η γωνία μεταξύ της επιφάνεια του νυχιού και της εγγύς φάλλαγας είναι > 180 μοίρες.
- Υπερτροφική οστεοαρθρίτιδα. Χρόνια αρθρίτιδα των μακρών οστών που μπορεί να προκαλέσει έντονο άλγος.
- Χείρα Dupuytren: Ρίκνωση της παλαμιαία απονεύρωσης, που οδηγεί σε αδυναμία πλήρους έκτασης των δακτύλων. Πιστεύεται ότι προκαλείται από υπερλειτουργία των ινοβλαστών και άτακτη εναπόθεση κολλαγόνου. Είναι σχετικά κοινό (33% των ασθενών).

- Γυναικομαστία: Καλοήθης πολλαπλασιασμός του αδενικού ιστού των μαστών σε άνδρες, εκτείνεται ομόκεντρα από τις θηλές. Προκαλείται από την αυξημένη οιστραδιόλη και συμβαίνει μέχρι και στο 66% των ασθενών.
- Υπογοναδισμός: Εκδηλώνεται ως ανικανότητα, στειρότητα, μειωμένη λίμπιντο, και ατροφία των όρχεων, λόγω πρωτοπαθούς τραυματισμού των γονάδων ή καταστολή του άξονα υποθαλάμου-υπόφυσης.
- Το μέγεθος του ήπατος: Μπορεί να είναι διευρυμένο (ηπατομεγαλία), κανονικό, ή συρρικνωμένο.
- Σπληνομεγαλία (αύξηση στο μέγεθος του σπληνός): Αποτέλεσμα της συμφόρησης του αίματος εξαιτίας της πυλαίας υπέρτασης.
- Ασκίτης: Συλλογή υγρού στην περιτοναϊκή κοιλότητα, προκαλεί διόγκωση της κοιλίας (χρειάζεται περίπου 1L για την ανίχνευση του με επίκρουση).
- Επίφλεβο δίκην κεφαλής μέδουσας: Το επιπολής περιομφάλιο φλεβικό δίκτυο διαστέλλεται λόγω της αυξημένης παράπλευρης κυκλοφορίας που προκαλεί η πυλαία υπέρταση. Απαραίτητο είναι να μείνει ανοιχτή η ομφαλική φλέβα (η οποία αποφράσεται φυσιολογικά μετά τον τοκετό)[11]
- Φύσημα Cruveilhier-Baumgarten: Φλεβικό φύσημα στο επιγάστριο (εξέταση με στηθοσκόπιο), λόγω της παράπλευρης κυκλοφορίας μεταξύ πυλαίου συστήματος και περιομφάλιου φλεβικού δικτύου στην πυλαία υπέρταση.
- Ηπατική δυσοσμία: Οσμή μούχλας στην αναπνοή ως αποτέλεσμα του αυξημένου διμεθυλοσουλφιδίου.
- Ίκτερος: Κιτρινόχροος αποχρωματισμός του δέρματος, των οφθαλμών, και των βλεννογόνων λόγω της αυξημένης χολερυθρίνης (τουλάχιστον 2-3 mg/dL ή 30 mmol/L). Τα ούρα μπορεί επίσης να εμφανίζουν σκούρο χρώμα.
- Τρόμος: Διπολικά ασύγχρονα σπασμωδικά χτυπήματα του χεριού όταν αυτά βρίσκονται σε πρόσθια έκταση και πρηνισμό. Παρατηρείται σε ασθενείς που έχουν αναπτύξει ηπατική εγκεφαλοπάθεια.
- Άλλα: Αδυναμία, κόπωση, ανορεξία, απώλεια βάρους.
Καθώς η νόσος εξελίσσεται εμφανίζονται επιπλοκές, οι οποίες είναι συχνά και τα πρώτα συμπτώματα της νόσου.
- αιμορραγία και μώλωπες από την διαταραχή του μηχανισμού πήξης.
- Ίκτερος
- Κνησμό (φαγούρα): λόγω εναπόθεσης χολικών αλάτων στο δέρμα.
- Ηπατική εγκεφαλοπάθεια: Η έκπτωση της ηπατικής λειτουργίας μειώνει τον μεταβολισμό της αμμωνίας και τον αζωτούχων ενώσεων στο αίμα, τα οποία μεταφέρονται στον εγκέφαλο και επηρεάζουν την εγκεφαλική λειτουργία: παραμέληση της προσωπικής εμφάνισης, απάθεια, απώλεια μνήμης, πρόβλημα συγκέντρωσης, ή αλλαγές στις συνήθειες του ύπνου.
- Υπερευαισθησία σε φάρμακα που προκαλείται από μειωμένο μεταβολισμό των δραστικών ενώσεων λόγω της έκπτωσης της ηπατικής λειτουργίας.
- Ηπατοκυτταρικό καρκίνωμα: πρωτοπαθής καρκίνος του ήπατος, μια συχνή επιπλοκή της κίρρωσης. Έχει υψηλό ποσοστό θνησιμότητας.
- Πυλαία υπέρταση: Το αίμα ρέει πιο αργά από τον εντερικό σωλήνα και τον σπλήνα, μέσω της ηπατικής πυλαίας φλέβας, προς το ήπαρ οδηγώντας σε αύξηση της πίεσης. Αυτό οδηγεί στις ακόλουθες επιπλοκές:
- Ασκίτης: συλλογή υγρού στην περιτοναϊκή κοιλότητα λόγω της αυξημένης αγγειακής πίεσης που προκαλεί εξαγγείωση υγρού.
- Κιρσοί οισοφάγου: λόγω της πυλαίας υπέρτασης σχηματίζεται ένα δίκτυο παράπλευρης κυκλοφορίας από το ήπαρ προς τον στόμαχο και τον οισοφάγο (Πυλαιοσυστηματική αναστόμωση). Αυτές οι φλέβες διευρύνονται σχηματίζοντας κιρσούς και είναι πολύ πιθανή η ρήξη τους, προκαλώντας αιμορραγία στο ανώτερο πεπτικό (αιματέμεση, υπογκοαιμία, μέλανα κένωση).

- Προβλήματα σε άλλα όργανα:
- Η κίρρωση μπορεί να προκαλέσει ανοσοανεπάρκεια, θέτοντας τον ασθενή επιρρεπή σε λοιμώξεις. Τα συμπτώματα της λοίμωξης συχνά είναι μη ειδικά και είναι δύσκολο να αναγνωριστούν (π.χ., επιδείνωση της εγκεφαλοπάθειας αλλά όχι πυρετό).
- Στην ασκητική συλλογή μπορεί να προκληθεί επιμόλυνση με βακτήρια του εντερικού σωλήνα (αυθόρμητη βακτηριακή περιτονίτιδα).
- Ηπατονεφρικό σύνδρομο: Η ανεπαρκή παροχή αίματος προς τους νεφρούς, προκαλώντας οξεία νεφρική ανεπάρκεια. Αυτή η επιπλοκή έχει ένα πολύ υψηλό ποσοστό θνησιμότητας (πάνω από 50%).
- Ηπατοπνευμονικό σύνδρομο: Παράκαμψη της φυσιολογικής πνευμονικής κυκλοφορίας, που οδηγεί σε κυάνωση και δύσπνοια (δυσκολία στην αναπνοή), με επιδείνωση σε καθιστή θέση.[12]
- Πυλαιοπνευμονική υπέρταση: Αύξηση της πίεσης στην πνευμονική κυκλοφορία ως αποτέλεσμα της πυλαίας υπέρτασης.[12]
- Πυλαία υπερτασική γαστροπάθεια: αναφέρεται σε διαταραχές στο βλεννογόνο του στομάχου σε ασθενείς με πυλαία υπέρταση, και σχετίζεται με τη σοβαρή κίρρωση.[13]
Αιτιοπαθογένεια[Επεξεργασία | επεξεργασία κώδικα]
Η κίρρωση έχει πολλές πιθανές αιτίες. Μερικές φορές περισσότερες από μία αιτίες είναι παρούσες στον ίδιο ασθενή. Στο δυτικό κόσμο, ο χρόνιος αλκοολισμός και ηπατίτιδα C είναι οι πιο κοινές αιτίες.
- Αλκοολική κίρρωση (ALD) . Η αλκοολική κίρρωση αναπτύσσεται μεταξύ 10-20% των ατόμων που κάνουν κατάχρηση αλκοόλ για πάνω από μία δεκαετία.[14] Το αλκοόλ φαίνεται να τραυματίζει το ήπαρ, αναστέλλοντας τον κανονικό μεταβολισμό πρωτεϊνών, λιπών, και υδατανθράκων. Οι ασθενείς μπορεί επίσης να εκδηλώσουν πυρετό, ηπατομεγαλία, ίκτερο, και ανορεξία. Οι AST και ALT είναι υψηλές, αλλά <300IU/L με λόγο AST: ALT >2,0, τιμή σπάνια σε άλλες ασθένειες του ήπατος. Βιοψία ήπατος μπορεί να δείξει ηπατοκυτταρική νέκρωση, σωμάτια Mallory, ουδετεροφιλική διήθηση με περιαγγειακή φλεγμονή.
- Μη αλκοολική λιπώδης διήθηση του ήπατος ή στεάτωση (NASH) . Στην NASH, το λίπος συσσωρεύεται στο ήπαρ και τελικά δημιουργείται ουλώδης ιστός. Αυτό το είδος της ηπατίτιδας φαίνεται να σχετίζεται με τον διαβήτη, τον πρωτεϊνικό υποσιτισμό, την παχυσαρκία, τη στεφανιαία νόσο, και τη θεραπεία με κορτικοστεροειδη. Η διαταραχή αυτή είναι παρόμοια με εκείνη της αλκοολικής ηπατικής νόσου, αλλά ο ασθενής δεν έχει ιστορικό κατάχρησης αλκοόλ. Η βιοψία είναι απαραίτητη για τη διάγνωση.
- Χρόνια ηπατίτιδα C. Η μόλυνση με τον ιό της ηπατίτιδας C προκαλεί φλεγμονή του ήπατος και ένα ποικίλο βαθμό βλάβης στο όργανο που μετά από δεκαετίες οδηγεί σε κίρρωση. Η κίρρωση που προκαλείται από ηπατίτιδα C είναι η πιο κοινή αιτία για μεταμόσχευση ήπατος. Μπορεί να διαγνωστεί με ορολογικές δοκιμασίες που ανιχνεύουν αντισώματα της ηπατίτιδας C ή το ιικό RNA. Η συχνότερα χρησιμοποιούμενη εξέταση πρώτης εκλογής στις ΗΠΑ είναι η ανοσοδοκιμασία ενζύμου, ΕΙΑ-2.
- Χρόνια ηπατίτιδα Β. Ο ιός της ηπατίτιδας Β προκαλεί φλεγμονή του ήπατος και τραυματισμό του, που μετά από δεκαετίες οδηγεί σε κίρρωση . Ο ιός της ηπατίτιδας D εξαρτάται από την παρουσία της ηπατίτιδας Β και επιταχύνει την κίρρωση σε συνλοίμωξη. Η χρόνια ηπατίτιδα Β μπορεί να διαγνωσθεί με ανίχνευση της HBsAG περισσότερο από 6 μήνες μετά την αρχική μόλυνση. Ανίχνευση HBeAg και του HBV DNA καθορίζουν κατά πόσο ο ασθενής θα χρειαστεί να αντιιική θεραπεία.
- Πρωτοπαθής χολική κίρρωση. Μπορεί να είναι ασυμπτωματική ή να συνοδεύεται από κόπωση, κνησμό, και μη ικτερική υπέρχρωση του δέρματος με ηπατομεγαλία. Ανιχνεύεται έντονη αύξηση της αλκαλικής φωσφατάσης καθώς και αυξήσεις στην χοληστερόλη και χολερυθρίνης. Επιβεβαιωτικό εύρημα διάγνωσης αποτελεί η εντόπιση αντιμιτοχονδριακών αντισωμάτων με βιοψία ήπατος και ύπαρξη βλαβών στον χοληδόχο πόρο. Είναι πιο συχνή στις γυναίκες.
- Πρωτοπαθής σκληρυντική χολαγγειίτιδα (PSC) . Η PSC είναι μια προοδευτική χολοστατική διαταραχή. Παρουσιάζει κνησμό, στεατόρροια, ανεπάρκεια λιποδιαλυτών βιταμινών, και μεταβολική νόσος των οστών. Υπάρχει μία συσχέτιση με τη φλεγμονώδη νόσο του εντέρου (IBD), ιδιαίτερα την ελκώδη κολίτιδα. Η διάγνωση γίνεται με χολαγγειογραφία (κοντράστ) που δείχνει διάχυτες, πολυεστιακές στενώσεις και διαστολή των χοληφόρων πόρων (“εικόνα κομπολογιού”). Μπορούν επίσης να είναι αυξημένες μη-ειδικές ανοσοσφαιρίνες του ορού.
- Αυτοάνοση ηπατίτιδα. Η ασθένεια προκαλείται από την αυτοανοσολογική βλάβη στο ήπαρ που προκαλεί φλεγμονή και τελικά ουλοποίηση και κίρρωση. Τα ευρήματα περιλαμβάνουν αύξηση τιμών σε σφαιρίνες ορού, ειδικά γ-σφαιρίνες. Η θεραπεία με πρεδνιζόνη και/ή αζαθειοπρίνη είναι ευεργετική. Η κίρρωση που οφείλεται σε αυτοάνοση ηπατίτιδα εξακολουθεί να έχει 10-ετή επιβίωση + 90%. Δεν υπάρχει ειδική εξέταση για τη διάγνωση της αυτοάνοσης ηπατίτιδας αλλά μπορεί να είναι ωφέλιμη η χορήγηση κορτικοστεροειδών.
- Κληρονομική αιμοχρωμάτωση (HHC). Συνήθως παρουσιάζεται με οικογενειακό ιστορικό κίρρωσης, υπέρχρωσης του δέρματος, σακχαρώδη διαβήτη, αρθροπάθεια, και/ή μυοκαρδιοπάθεια, όλα οφείλονται στην υπερφόρτωση σιδήρου. Αιματολογικές εξετάσεις θα δείξουν κορεσμένη τρανσφερρίνη νηστείας > 60% και φερριτίνη> 300 ng/mL. Γενετικές δοκιμές μπορούν να χρησιμοποιηθούν για τον εντοπισμό μεταλλάξεων του HFE. Αν όλα αυτά ανιχνευτούν η βιοψία δεν είναι απαραίτητη. Η θεραπεία γίνεται με φλεβοτομία για να μειωθούν τα επίπεδα σιδήρου στον οργανισμό.
- Νόσος του Wilson. Αυτοσωματική υπολειπόμενη διαταραχή που χαρακτηρίζεται από χαμηλή σερουλοπλασμίνη ορού και αυξημένη ηπατική περιεκτικότητα σε χαλκό σε βιοψία ήπατος. Μπορεί επίσης να έχει δακτύλιους Kayser-Fleischer στον κερατοειδή χιτώνα και διαταραχή της νοητικής κατάστασης.
- Ανεπάρκεια Α1-αντιτρυψίνης (A1AD) . Αυτοσωμικός υπολειπόμενος χαρακτήρας. Οι ασθενείς μπορούν επίσης να έχουν χρόνια αποφρακτική πνευμονοπάθεια (ΧΑΠ), ιδιαίτερα εάν έχουν ιστορικό καπνίσματος. Τα επίπεδα ΑΑΤ ορού είναι χαμηλά. Χρησιμοποιείται ανασυνδυασμένο ΑΑΤ για την πρόληψη της νόσου των πνευμόνων λόγω της ανεπάρκειας σε ΑΑΤ.
- Καρδιακή κίρρωση. Λόγω χρόνιας δεξιά καρδιακής ανεπάρκειας η οποία οδηγεί σε συμφόρηση αίματος στο ήπαρ.
- Γαλακτοζαιμία
- Νόσος της αποθήκευσης γλυκογόνου τύπου IV
- Κυστική ίνωση
- Ηπατοτοξικά φαρμάκα ή τοξίνες
- Ανεπάρκεια λυσοσωματικής λιπάσης (ανεπάρκεια LAL) είναι μια σπάνια αυτοσωματική υπολειπόμενη γενετική πάθηση και χαρακτηρίζεται από ηπατομεγαλία, διαταραγμένη LFTs και υπερλιπιδαιμία τύπου ΙΙ. Σε ορισμένους ασθενείς εμφανίζεται σπληνομεγαλία και ένδειξη ήπιου υπερσπληνισμού. Η ανεπάρκεια λυσοσωματικής λιπάσης αν δεν υποκατασταθεί μπορεί να οδηγήσει σε ίνωση, κίρρωση, ηπατική ανεπάρκεια και θάνατο.
Παθοφυσιολογία[Επεξεργασία | επεξεργασία κώδικα]
Το ήπαρ παίζει ζωτικό ρόλο στη σύνθεση των πρωτεϊνών (π.χ. αλβουμίνη, παράγοντες πήξης και σύστημα συμπληρώματος), στην αποτοξίνωση και την αποθήκευση ουσιών(π.χ. βιταμίνης Α). Επιπλέον, συμμετέχει στο μεταβολισμό των λιπιδίων και των υδατανθράκων.
Η κίρρωση συχνά προηγείται της ηπατίτιδας και της λιπώδους διήθησης ήπατος (στεάτωση), ανεξάρτητα από την αιτία. Εάν η αιτία απομακρυνθεί στο στάδιο αυτό, οι αλλαγές είναι ακόμα πλήρως αναστρέψιμες.
Το παθολογικό χαρακτηριστικό της κίρρωσης είναι η ανάπτυξη ουλώδους ιστού, που αντικαθιστά το φυσιολογικό παρέγχυμα, εμποδίζοντας την πυλαία κυκλοφορία και προκαλώντας διαταραχή της λειτουργίας. Πρόσφατες έρευνες δείχνουν τον κεντρικό ρόλο στην ανάπτυξη της κίρρωσης, που παίζει το αστεροειδές κύτταρο, ένα είδος κυττάρου, που κανονικά αποθηκεύει βιταμίνη Α. Βλάβη στο ηπατικό παρέγχυμα οδηγεί στην ενεργοποίηση του αστεροειδούς κυττάρου σε μυοϊνοβλάστη και αποφράσσεται η κυκλοφορία του αίματος. Επιπλέον, εκκρίνεται TGF-β1, η οποία οδηγεί σε μια ινώδη αντίδραση και πολλαπλασιασμό του συνδετικού ιστού. Επιπλέον, εκκρίνεται ΤΙΜΡ 1 και 2, φυσικώς απαντώμενοι αναστολείς της μεταλλοπρωτεϊνάσης, πράγμα που παρεμποδίζει την διάσπαση ινωτικού υλικού στον εξωκυττάριο χώρο.[15]
Οι ινώδεις ζώνες (διαφραγμάτια) ξεχωρίζουν τα ηπατοκυτταρικά οζίδια, τα οποία αντικαθιστούν τελικά το σύνολο της αρχιτεκτονικής του ήπατος, με αποτέλεσμα τη μείωση της ροής του αίματος σε αυτό. Στο σπλήνα γίνεται συμφόρηση του αίματος, πράγμα που οδηγεί σε υπερσπληνισμό και αυξημένη παγίδευση αιμοπεταλίων . Η πυλαία υπέρταση είναι υπεύθυνη για τις πιο σοβαρές επιπλοκές της κίρρωσης.
Διάγνωση[Επεξεργασία | επεξεργασία κώδικα]
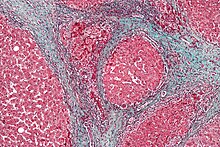
Η επιβεβαίωση της διάγνωσης της κίρρωσης γίνεται με βιοψία ήπατος. Η προσέγγιση γίνεται διαδερμικά, διασφαγιτιδικά, λαπαροσκοπικά, ή μέσω λεπτής βελόνης. Η βιοψία δεν είναι απαραίτητη, εάν τα κλινικά, εργαστηριακά, και ακτινολογικά δεδομένα δείχνουν κίρρωση. Επιπλέον, υπάρχει ένας μικρός αλλά σημαντικός κίνδυνος στην βιοψία ήπατος, και η ίδια η κίρρωση προδιαθέτει επιπλοκές στην βιοψία ήπατος.[16] Ο ασκίτης, ο χαμηλός αριθμός αιμοπεταλίων , και τα αραχνοειδή αιμαγγειώματα είναι χρήσιμα ευρήματα.[17]
Εργαστηριακά Ευρήματα[Επεξεργασία | επεξεργασία κώδικα]
Τα ακόλουθα ευρήματα είναι τυπικά σε κίρρωση:
- Αμινοτρανσφεράσες -AST και ALT είναι μετρίως αυξημένα, με AST> ALT. Ωστόσο, η φυσιολογικές αμινοτρανσφεράσες δεν αποκλείουν την κίρρωση.
- Αλκαλική φωσφατάση - συνήθως ελαφρώς αυξημένη.
- γ-Γλουταμυλοτρανσφεράση (GGT) - συσχετίζεται με τα επίπεδα ΑΡ. Τυπικά πολύ υψηλότερη σε αλκοολική ηπατίτιδα.
- Χολερυθρίνη - μπορεί να αυξηθεί καθώς η κίρρωση εξελίσσεται.
- Αλβουμίνη - τα επίπεδα πέφτουν καθώς η ηπατική λειτουργία μειώνεται με την επιδείνωση της κίρρωσης, δεδομένου ότι η αλβουμίνη συντίθεται αποκλειστικά στο ήπαρ
- Χρόνος προθρομβίνης – αυξημένος εφόσον το ήπαρ συνθέτει παράγοντες πήξης.
- Σφαιρίνη - αυξημένη λόγω της μετακίνησης των βακτηριακών αντιγόνων από το ήπαρ στο λεμφικό ιστό.
- Νάτριο ορού - υπονατριαιμία λόγω της αδυναμίας νεφρικής απέκκρισης ελεύθερου νερό που προκύπτει από τα υψηλά επίπεδα της ADH και της αλδοστερόνης.
- Θρομβοκυτταροπενία - τόσο λόγω συμφορητικής σπληνομεγαλίας καθώς και μειωμένης θρομβοποιητίνης. Εν τούτοις, αυτό σπάνια καταλήγει σε αριθμό αιμοπεταλίων < 50,000/mL.
- Λευκοπενία και ουδετεροπενία - λόγω σπληνομεγαλίας με σπληνική οριοποίηση.
- Διαταραχή πήξης - το ήπαρ παράγει τους περισσότερους από τους παράγοντες πήξεως και έτσι συσχετίζεται με διαταραχή της πηκτικότητας επιδεινώνοντας την ηπατική νόσο.
Το Fibrotest αποτελεί ένα καινούργιο μη επεμβατικό βιοδείκτης της ίνωσης του ήπατος (και έτσι της κίρρωσης) που αποτελεί συνδυασμό 6 δεικτών.[18]
Άλλες εργαστηριακές μελέτες, που πραγματοποιήθηκαν σε νεοδιαγνωσθέντες ασθενείς με κίρρωση μπορεί να περιλαμβάνουν:
Ορολογικές για ιούς ηπατίτιδας, αυτοαντισωμάτων ( ANA, αντι-λείων μυικών ινών αντίσωμα, αντι-μιτοχονδριακό αντίσωμα, anti-LKM)
- Φερριτίνη ορού και κορεσμό τρανσφερρίνης (δείκτες της υπερσιδήροσης), χαλκό ορού και σερουλοπλασμίνη (δείκτες της υπερφόρτωσης του χαλκού)
- Επίπεδα ανοσοσφαιρίνης (IgG, IgM, IgA) - αυτές είναι μη-ειδικές, αλλά μπορούν να βοηθήσουν στην διάκριση διάφορων αιτιών
- Χοληστερόλη και γλυκόζη
- Α1-αντιθρυψίνη
Απεικονιστικά Ευρήματα[Επεξεργασία | επεξεργασία κώδικα]

Οι υπέρηχοι χρησιμοποιούνται συνήθως για την αξιολόγηση της κίρρωσης. Σε προχωρημένη κίρρωση το ήπαρ εμφανίζεται μικρό και οζώδες με αυξημένη ηχογενεία και ακανόνιστες περιοχές. Άλλα απεικονιστικά ευρήματα που υποδηλώνουν κίρρωση είναι η διεύρυνση του κερκοφόρου λοβού και η διεύρυνση του σπλήνα. Ένας διευρυμένος σπλήνας (σπληνομεγαλία), ο οποίος είναι κανονικά λιγότερο από 11 -12cm σε ενήλικες, είναι ενδεικτικό της κίρρωσης με πυλαία υπέρταση. Οι υπέρηχοι μπορούν επίσης να ελέγξουν το ηπατοκυτταρικό καρκίνωμα, την πυλαία υπέρταση και το σύνδρομο Budd-Chiari (με την εκτίμηση της κυκλοφορίας στην ηπατική φλέβα).
Ένας νέος τύπος συσκευής, το FibroScan (παροδική ελαστογραφία), χρησιμοποιεί ελαστικά κύματα για να προσδιορίσει την ακαμψία του ήπατος, που θεωρητικά μπορεί να μετατραπεί σε ένα «σκορ» ήπατος με βάση την κλίμακα METAVIR. Το FibroScan παράγει μια εικόνα υπερήχων του ήπατος (20 με 80 mm) μαζί με μια ένδειξη της πίεσης (σε kPa.) Η εξέταση είναι πολύ ταχύτερη από μια βιοψία (διαρκεί συνήθως 2,5-5 λεπτά) και είναι εντελώς ανώδυνη. Υποδηλώνει μία συσχέτιση με τη σοβαρότητα της κίρρωσης.[19]
Άλλες δοκιμές που πραγματοποιούνται σε ειδικές περιπτώσεις περιλαμβάνουν Αξονική τομογραφία κοιλίας και Μαγνητική Χολλαγγειοπαγκρεατογραφία (MRCP).
Ενδοσκόπηση[Επεξεργασία | επεξεργασία κώδικα]
Γαστροσκόπηση (ενδοσκοπική εξέταση του οισοφάγου, του στομάχου και δωδεκαδακτύλου) εκτελείται σε ασθενείς με εγκατεστημένη κίρρωση ώστε να αποκλειστεί η πιθανότητα να έχουν κιρσούς οισοφάγου. Αν εντοπισθούν, μπορεί να εφαρμοστεί προφυλακτική τοπική θεραπεία (σκληροθεραπεία ή τοποθέτηση Stent) και θεραπεία με β-αναστολείς.
Σπάνιες αιτίες της κίρρωσης είναι οι ασθένειες των χοληφόρων οδών, όπως η πρωτοπαθής σκληρυντική χολαγγειίτιδα. Η απεικόνιση των χοληφόρων οδών με ενδοσκοπική παλίνδρομη χολαγγειοπαγκρεατογραφία (ERCP) ή μαγνητική χολαγγειοπαγκρεατογραφία (MRCP) (MRI των χοληφόρων οδών και του παγκρεατικού πόρου) μπορεί να δείξει ανωμαλίες σε αυτούς τους ασθενείς και να βοηθήσει στη διάγνωση.


Παθολογοανατομία[Επεξεργασία | επεξεργασία κώδικα]

Μακροσκοπικά, το ήπαρ αρχικά διευρύνεται, αλλά με την πρόοδο της νόσου, γίνεται μικρότερο. Η επιφάνειά του είναι ακανόνιστη, έχει σταθερή συνοχή και το χρώμα είναι συχνά κιτρινόχρου (αν σχετίζεται με στεάτωση). Ανάλογα με το μέγεθος των οζιδίων υπάρχουν τρεις μακροσκοπικοί τύποι : μικροοζιδιακή, μακροοζιδιακή και μικτή κίρρωση. Στην μικροοζιδιακή μορφή (κίρρωση Laennec ή πυλαία κίρρωση) τα οζίδια είναι κάτω των 3 mm. Στην μακροοζιδιακή κίρρωση (μετανεκρωτική κίρρωση), τα οζίδια είναι μεγαλύτερα από 3 mm. Η μικτή κίρρωση συνίσταται σε μια ποικιλία των οζιδίων με διαφορετικά μεγέθη.
Τα μικροσκοπικά χαρακτηριστικά της κίρρωσης είναι: (1) η παρουσία των αναγεννητικών οζιδίων των ηπατοκυττάρων και (2) η παρουσία ίνωσης, ή η εναπόθεση συνδετικού ιστού μεταξύ αυτών των οζιδίων. Η αρχιτεκτονική της ίνωσης μπορεί να εξαρτάται από την υποκείμενη προσβολή, που οδήγησε στην κίρρωση. Ο ινωτικός μηχανισμός μπορεί να συνεχιστεί και μετά από την διακοπή της αρχικής υποκείμενης διαδικασίας, που την προκάλεσε. Η ίνωση στην κίρρωση μπορεί να οδηγήσει σε καταστροφή και άλλων φυσιολογικών ιστών στο ήπαρ: συμπεριλαμβανομένων των κολποειδών, το χώρο του Disse, και άλλες αγγειακές δομές, οι οποίες οδηγούν σε αύξηση της αντίστασης στην κυκλοφορία του αίματος στο ήπαρ και την πυλαία υπέρταση.[20]
Η κίρρωση μπορεί να προκληθεί από διαφορετικά αίτια, που προσβάλουν το ήπαρ με διαφορετικούς τρόπους, προκαλώντας παραλλαγές στην κιρρωτική αρχιτεκτονική του παρεγχύματος. Για παράδειγμα, στη χρόνια ηπατίτιδα Β, υπάρχει διήθηση του παρεγχύματος του ήπατος με λεμφοκύτταρα, στην καρδιακή κίρρωση υπάρχουν ερυθροκύτταρα και έντονη ίνωση στον ιστό, που περιβάλλει τις ηπατικές φλέβες, στην πρωτοπαθή χολική κίρρωση, υπάρχει ίνωση γύρω από τους χολικούς πόρους και στην αλκοολική κίρρωση, υπάρχει διήθηση του ήπατος με ουδετερόφιλα.[20]
Σταδιοποίηση[Επεξεργασία | επεξεργασία κώδικα]
Το στάδιο της κίρρωσης συνήθως ταξινομείται με την κλίμακα Child-Pugh. Η κλίμακα αυτή χρησιμοποιεί τις τιμές χολερυθρίνης, λευκωματίνης, INR, την παρουσία και τη σοβαρότητα του ασκίτη και την ύπαρξη εγκεφαλοπάθειας. Η ταξινόμηση των ασθενών γίνεται στις κατηγορίες Α, Β ή Γ. Η κατηγορία Α έχει ευνοϊκή πρόγνωση, ενώ η κατηγορία Γ έχει υψηλό κίνδυνο θανάτου. Η κλίμακα αυτή επινοήθηκε το 1964 από τους Child and Turcotte και τροποποιήθηκε το 1973 από τον Pugh.
Πιο σύγχρονες κλίμακες, που χρησιμοποιούνται για την κατανομή των προς μεταμόσχευση ήπατος ασθενών, αλλά και σε άλλες περιπτώσεις, είναι το μοντέλο των παθήσεων του ήπατος τελικού σταδίου (MELD)και το παιδιατρικό ομόλογό του (PELD).
Η βαθμίδωση της φλεβικής ανεπάρκειας, δηλ. η διαφορά πίεσης μεταξύ της προσαγωγού και απαγωγού φλεβικής αιμάτωσης του ήπατος, καθορίζει επίσης τη σοβαρότητα της κίρρωσης, αν και είναι δύσκολο να μετρηθεί. Μια διαφορά 16mm ή περισσότερο υποδεικνύει αυξημένο κίνδυνο θανάτου.[21]
Θεραπεία[Επεξεργασία | επεξεργασία κώδικα]
Σε γενικές γραμμές, η ηπατική βλάβη, που προκαλεί η κίρρωση είναι μη αντιστρέψιμη, αλλά η θεραπεία μπορεί να σταματήσει ή να καθυστερήσει την περαιτέρω εξέλιξη και να μειώσει τις επιπλοκές. Η υγιεινή διατροφή ενθαρρύνεται, αφού η κίρρωση μπορεί να είναι μια ενεργοβόρος διαδικασία. Τακτική παρακολούθηση είναι συχνά απαραίτητη. Θα πρέπει να συνταγογραφούνται αντιβιοτικά για τις «λοιμώξεις», καθώς και διάφορα φάρμακα βοηθητικά για τον «κνησμό». Καθαρτικά, όπως λακτουλόζη, μειώνουν τον κίνδυνο της δυσκοιλιότητας, αλλά ο ρόλος τους στην πρόληψη της εγκεφαλοπάθειας είναι περιορισμένος.
Η «αλκοολική κίρρωση» που προκαλείται από κατάχρηση αλκοόλ αντιμετωπίζεται με αποχή από το αλκοόλ. Η θεραπεία για την κίρρωση σχετιζόμενη με «ηπατίτιδα» περιλαμβάνει φάρμακα, που χρησιμοποιούνται για τη θεραπεία των διαφόρων τύπων ηπατίτιδας, όπως ιντερφερόνη για «ιογενή ηπατίτιδα» και κορτικοστεροειδή για «αυτοάνοση ηπατίτιδα». Η κίρρωση, που προκαλείται από την «νόσο του Wilson» (χαλκός συσσωρεύεται σε διάφορα όργανα) αντιμετωπίζεται με θεραπεία αποχάλκωσης (π.χ. πενικιλλαμίνη).
Η πρόληψη περαιτέρω ηπατικής βλάβης[Επεξεργασία | επεξεργασία κώδικα]
Ανεξάρτητα από την υποκείμενη αιτία της κίρρωσης, αποθαρρύνεται η χρήση αλκοόλ, παρακεταμόλης (Depon, Panadol), καθώς και άλλων βλαπτικών ουσιών. Θα πρέπει να λαμβάνεται υπ' όψη ο εμβολιασμός των ευπαθών ασθενών για την ηπατίτιδα Α και ηπατίτιδα Β.
Μεταμόσχευση[Επεξεργασία | επεξεργασία κώδικα]
Η μεταμόσχευση ήπατος είναι απαραίτητη, όταν οι επιπλοκές είναι μη ελεγχόμενες ή όταν υπάρχει σοβαρή ηπατική ανεπάρκεια. Η επιβίωση μετά από μεταμόσχευση ήπατος έχει βελτιωθεί κατά τη δεκαετία του 1990, και το ποσοστό πενταετούς επιβίωσης είναι τώρα γύρω στο 80% (το ποσοστό εξαρτάται σε μεγάλο βαθμό από τη βαρύτητα της νόσου και άλλα ιατρικά προβλήματα του λήπτη).[22] Η μεταμόσχευση απαιτεί τη χρήση των ανοσοκατασταλτικών (π.χ. κυκλοσπορίνη).
Υποτροπή της κίρρωσης[Επεξεργασία | επεξεργασία κώδικα]
Σε ασθενείς με σταθεροποιημένη κίρρωση, μπορεί να προκύψει ανεπάρκεια εξαιτίας διαφόρων αιτιών, όπως η δυσκοιλιότητα, λοίμωξη (από οποιαδήποτε πηγή), κατάχρηση αλκοόλ, φάρμακα, αιμορραγία από κιρσούς οισοφάγου ή αφυδάτωση. Η υποτροπή λαμβάνει την μορφή των επιπλοκών της κίρρωσης που απαριθμούνται ανωτέρω.
Οι ασθενείς με υποτροπιάζουσα κίρρωση γενικά χρειάζονται εισαγωγή στο νοσοκομείο, στενή παρακολούθηση της ενυδάτωσης, της ψυχικής κατάστασης και με έμφαση στην επαρκή διατροφή και ιατρική περίθαλψη (συχνά με αντιβιοτικά, διουρητικά, καθαρτικά και/ή κλύσματα, θειαμίνη και περιστασιακά στεροειδή, ακετυλοκυστεΐνη και πεντοξυφυλλίνη). Χορήγηση αλατούχου διαλύματος γενικά αποφεύγεται καθώς θα προστεθεί στην ήδη υψηλή συνολική περιεκτικότητα σε νάτριο του σώματος.
Αντιμετώπιση επιπλοκών[Επεξεργασία | επεξεργασία κώδικα]
Ασκίτης[Επεξεργασία | επεξεργασία κώδικα]
Περιορισμός του νατρίου είναι συχνά αναγκαίος, καθώς η κίρρωση οδηγεί στην κατακράτηση νατρίου. Συχνά είναι απαραίτητη η χορήγηση διουρητικών για να καταστείλουν τον ασκίτη. Για ενδονοσοκομειακή νοσηλεία χορηγούνται ανταγωνιστές της αλδοστερόνης (συνήθως σπειρονολακτόνη) και διουρητικά της αγκύλης. Οι ανταγωνιστές της αλδοστερόνης προτιμούνται για ασθενείς, που μπορούν να λαμβάνουν από του στόματος φάρμακα και δεν έχουν ανάγκη από επείγουσα μείωση του όγκου, και με τα διουρητικά της αγκύλης ως επιπρόσθετη θεραπεία.[23]
Αν απαιτείται ταχεία μείωση του όγκου, η «παρακέντηση» είναι μέθοδος εκλογής. Η παρακέντηση γίνεται με την εισαγωγή παροχετευτικού σωλήνα εντός της περιτοναϊκής κοιλότητας. «Διάλυμα ανθρώπινης λευκωματίνης» συνήθως δίνεται για την πρόληψη των επιπλοκών από την ταχεία μείωση του όγκου. Εκτός του ότι είναι ταχύτερη από τα διουρητικά, είναι αποτελεσματικότερη στην απομάκρυνση μεγάλου όγκου (4-5 λίτρα).[23]
Αιμορραγία του οισοφάγου (Κιρσοι Οισοφάγου)[Επεξεργασία | επεξεργασία κώδικα]
Σε περίπτωση πυλαίας υπέρτασης, η προπρανολόλη είναι ένα συνηθισμένο φάρμακο. που χρησιμοποιείται για την μείωση της πίεσης στο πυλαίο σύστημα. Σε σοβαρές επιπλοκές από πυλαία υπέρταση, πυλαιοσφαγιτιδική αναστόμωση ενδείκνυται μερικές φορές, για να μειωθεί η πίεση στην πυλαία φλέβα. Δεδομένου ότι αυτό μπορεί να επιδεινώσει κάποια εγκεφαλοπάθεια, ενδείκνυται σε ασθενείς με μικρό κίνδυνο εγκεφαλοπάθειας, και γενικά θεωρείται μόνο ως μεταβατικό στάδιο πριν τη μεταμόσχευση ήπατος ή ως παρηγορητική θεραπεία.
Ηπατική εγκεφαλοπάθεια[Επεξεργασία | επεξεργασία κώδικα]
Τροφές υψηλής πρωτεϊνικής αξίας αυξάνουν το ισοζυγίου αζώτου, και αυξάνεται, θεωρητικά, η πιθανότητα εγκεφαλοπάθειας. Κατά το παρελθόν, συνεπώς, συνιστούσαν προσαρμογή της διατροφής και μείωση της πρόσληψης πρωτεϊνών. Πρόσφατες μελέτες δείχνουν ότι η υπόθεση αυτή ήταν εσφαλμένη, και ενθαρρύνεται η κατανάλωση τροφών υψηλής πρωτεϊνικής αξίας για να διατηρηθεί επαρκής διατροφή.[24]
Ηπατονεφρικό σύνδρομο[Επεξεργασία | επεξεργασία κώδικα]
Το ηπατονεφρικό σύνδρομο ορίζεται ως νάτριο ούρων μικρότερη από 10 mmol/L και κρεατινίνη ορού> 1.5 mg/dl (ή ούρων 24ώρου λιγότερο από 40 ml/min), χωρίς την χορήγηση διουρητικών.[25]
Αυθόρμητη βακτηριακή περιτονίτιδα[Επεξεργασία | επεξεργασία κώδικα]
Κιρρωτικοί ασθενείς με ασκίτη βρίσκονται σε κίνδυνο αυθόρμητης βακτηριακής περιτονίτιδας.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «Cirrhosis – MayoClinic.com».
- ↑ «Liver Cirrhosis». Review of Pathology of the Liver.
- ↑ «Pathology Education: Gastrointestinal». Αρχειοθετήθηκε από το πρωτότυπο στις 15 Ιουνίου 2010. Ανακτήθηκε στις 25 Νοεμβρίου 2012.
- ↑ Παθολογική Φυσιολογία, Α.Π.Θ. ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ - ΤΟΜΕΑΣ ΠΑΘΟΛΟΓΙΑΣ, Συλλογικό Έργο, University Studio Press 2009, ISBN 978-960-12-1278-4
- ↑ Roguin A (2006). «Rene Theophile Hyacinthe Laënnec (1781–1826): The Man Behind the Stethoscope». Clinical medicine & research 4 (3): 230–5. doi:. PMID 17048358.
- ↑ «WHO Disease and injury country estimates». World Health Organization. 2009. Ανακτήθηκε στις 11 Νοεμβρίου 2009.
- ↑ Anderson RN, Smith BL (2003). «Deaths: leading causes for 2001». National vital statistics reports: from the Centers for Disease Control and Prevention, National Center for Health Statistics, National Vital Statistics System 52 (9): 1–85. PMID 14626726.
- ↑ Sørensen HT, Thulstrup AM, Mellemkjar L, et al. (2003). «Long-term survival and cause-specific mortality in patients with cirrhosis of the liver: a nationwide cohort study in Denmark». Journal of Clinical Epidemiology 56 (1): 88–93. doi:. PMID 12589875. https://archive.org/details/sim_journal-of-clinical-epidemiology_2003-01_56_1/page/88.
- ↑ Klatsky AL, Morton C, Udaltsova N, Friedman GD (2006). «Coffee, cirrhosis, and transaminase enzymes». Archives of Internal Medicine 166 (11): 1190–5. doi:. PMID 16772246.
- ↑ Li CP, Lee FY, Hwang SJ, et al. (1999). «Spider angiomas in patients with liver cirrhosis: role of alcoholism and impaired liver function». Scand. J. Gastroenterol. 34 (5): 520–3. doi:. PMID 10423070. https://archive.org/details/sim_scandinavian-journal-of-gastroenterology_1999-05_34_5/page/520.
- ↑ Κλινική Εξέταση και Διάγνωση, Α.Π.Θ. Ιατρική Σχολή - Τομέας Παθολογίας, Δ.Καραμήτσος, Μ.Σιών, Γ.Γιαννόγλου, University Studio Press 2007, ISBN 960-12-1560-3
- ↑ 12,0 12,1 Rodríguez-Roisin R, Krowka MJ, Hervé P, Fallon MB (2004). «Pulmonary-Hepatic vascular Disorders (PHD)». Eur. Respir. J. 24 (5): 861–80. doi:. PMID 15516683.
- ↑ Kim MY, Choi H, Baik SK, et al. (April 2010). «Portal Hypertensive Gastropathy: Correlation with Portal Hypertension and Prognosis in Cirrhosis». Dig Dis Sci 55 (12): 3561–7. doi:. PMID 20407828. https://archive.org/details/sim_digestive-diseases-and-sciences_2010-12_55_12/page/3561.
- ↑ Alcohol-Induced Liver Disease; http://www.liverfoundation.org/abouttheliver/info/alcohol/
- ↑ Iredale JP (2003). «Cirrhosis: new research provides a basis for rational and targeted treatments». BMJ 327 (7407): 143–7. doi:. PMID 12869458. PMC 1126509. http://bmj.bmjjournals.com/cgi/content/full/327/7407/143.
- ↑ Grant, A; Neuberger J (1999). «Guidelines on the use of liver biopsy in clinical practice». Gut 45 (Suppl 4): 1–11. doi:. PMID 10485854. PMC 1766696. http://gut.bmj.com/cgi/content/full/45/suppl_4/IV1. «The main cause of mortality after percutaneous liver biopsy is intraperitoneal haemorrhage as shown in a retrospective Italian study of 68,000 percutaneous liver biopsies in which all six patients who died did so from intraperitoneal haemorrhage. Three of these patients had had a laparotomy, and all had either cirrhosis or malignant disease, both of which are risk factors for bleeding.».
- ↑ Udell, JA; Wang, CS, Tinmouth, J, FitzGerald, JM, Ayas, NT, Simel, DL, Schulzer, M, Mak, E, Yoshida, EM (2012 Feb 22). «Does this patient with liver disease have cirrhosis?». JAMA: the Journal of the American Medical Association 307 (8): 832–42. doi:. PMID 22357834.
- ↑ Halfon P, Munteanu M, Poynard T (2008). «FibroTest-ActiTest as a non-invasive marker of liver fibrosis». Gastroenterol Clin Biol 32 (6): 22–39. doi:. PMID 18973844.
- ↑ Foucher J, Chanteloup E, Vergniol J, et al. (2006). «Diagnosis of cirrhosis by transient elastography (FibroScan): a prospective study». Gut 55 (3): 403–8. doi:. PMID 16020491. PMC 1856085. https://archive.org/details/sim_gut_2006-03_55_3/page/403.
- ↑ 20,0 20,1 Brenner, David (2003). «Pathogenesis of Hepatic Fibrosis». Στο: Tadataka Yamada. Textbook of Gastroenterology. 2 (4th έκδοση). Lippincott Williams & Wilkins. ISBN 978-0-7817-2861-4. Unknown parameter
|coauthors=ignored (|author=suggested) (βοήθεια) - ↑ Patch D, Armonis A, Sabin C, et al. (1999). «Single portal pressure measurement predicts survival in cirrhotic patients with recent bleeding». Gut 44 (2): 264–9. doi:. PMID 9895388. PMC 1727391. http://gut.bmj.com/cgi/content/abstract/44/2/264.
- ↑ «E-medicine liver transplant outlook and survival rates». Emedicinehealth.com. 9 Ιουνίου 2009. Ανακτήθηκε στις 6 Σεπτεμβρίου 2009.
- ↑ 23,0 23,1 Moore KP, Aithal GP (October 2006). «Guidelines on the management of ascites in cirrhosis». Gut 55 Suppl 6: vi1–12. doi:. PMID 16966752.
- ↑ Sundaram V, Shaikh OS (July 2009). «Hepatic encephalopathy: pathophysiology and emerging therapies». Med. Clin. North Am. 93 (4): 819–36, vii. doi:. PMID 19577116. https://archive.org/details/sim_medical-clinics-of-north-america_2009-07_93_4/page/819.
- ↑ Ginés P, Arroyo V, Quintero E, et al. (1987). «Comparison of paracentesis and diuretics in the treatment of cirrhotics with tense ascites. Results of a randomized study». Gastroenterology 93 (2): 234–41. PMID 3297907. https://archive.org/details/sim_gastroenterology_1987-08_93_2/page/234.
|
