Θρομβοφιλία
| θρομβοφιλία | |
|---|---|
 Μια εικόνα από υπερηχογράφημα που δείχνει έναν θρόμβο αίματος στην αριστερή κοινή μηριαία φλέβα | |
| Ειδικότητα | αιματολογία |
| Ταξινόμηση | |
| ICD-10 | D69.1 |
| ICD-9 | 286.9 |
| MedlinePlus | 000681 |
| eMedicine | άρθρο/211039 |
| MeSH | D019851 |
Η θρομβοφιλία (ορισμένες φορές υπερπηκτικότητα ή προθρομβωτική κατάσταση) αποτελεί ανωμαλία στην πήξη του αίματος, η οποία αυξάνει τον κίνδυνο θρόμβωσης (δημιουργία θρόμβου μέσα σε αγγείο).[1][2] Τέτοιου είδους ανωμαλίες πιστοποιούνται στο 50% των ατόμων που εμφανίζουν θρομβωτικό επεισόδιο (π.χ. θρόμβωση στις εν τω βάθει φλέβες του κάτω άκρου) το οποίο δεν προκλήθηκε από άλλο αίτιο.[3] Ένα σημαντικό ποσοστό του πληθυσμού εμφανίζει ανιχνεύσιμες ανωμαλίες, οι περισσότερες από τις οποίες όμως οδηγούν σε θρόμβωση μόνο υπό την παρουσία κάποιου επιπρόσθετου παράγοντα κινδύνου.[2] Δεν υπάρχει κάποια συγκεκριμένη θεραπεία για τις περισσότερες περιπτώσεις, αλλά υποτροπιάζοντα επεισόδια θρόμβωσης αποτελούν ένδειξη για μακροπρόθεσμη προληπτική αντιπηκτική αγωγή.[2] Το πρώτο βασικό είδος θρομβοφιλίας ταυτοποιήθηκε το 1965, ενώ οι πιο κοινές ανωμαλίες (συμπεριλαμβανομένου του παράγοντα V Leiden) περιγράφησαν τη δεκαετία του 1990.[4][5]
Σημεία και συμπτώματα[Επεξεργασία | επεξεργασία κώδικα]
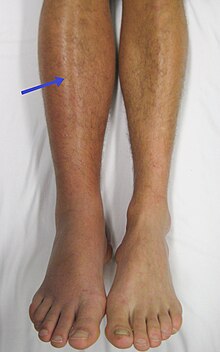
Οι πιο κοινές παθήσεις που συνδέονται με τη θρομβοφιλία είναι οι θρομβώσεις των εν τω βάθει φλεβών και η πνευμονική εμβολή, οι οποίες αναφέρονται συνολικά με τον όρο «φλεβική θρομβοεμβολή». Οι θρομβώσεις των εν τω βάθει φλεβών συχνά εντοπίζονται στα κάτω άκρα και χαρακτηρίζονται από πόνο, οίδημα και ερυθρότητα στο άκρο. Μπορεί να οδηγήσουν μακροπρόθεσμα σε οίδημα και αίσθημα βάρους εξαιτίας της καταστροφής των φλεβικών βαλβίδων.[6] Ο θρόμβος ενδέχεται επίσης να μεταναστεύσει προς κάποια αρτηρία στον πνεύμονα και να την αποφράξει. Ανάλογα με το μέγεθος και την τοποθεσία του θρόμβου, αυτό μπορεί να οδηγήσει σε αιφνίδια έναρξη βραχύπνοιας, στηθάγχης, αίσθησης των παλμών ή ακόμα και σε κατάρρευση, σοκ και καρδιακή ανακοπή.[2][7]
Η φλεβική θρόμβωση ενδέχεται επίσης να συμβεί σε πιο ασυνήθιστες περιοχές: στις εγκεφαλικές φλέβες, στις ηπατικές (θρόμβωση της πυλαίας ή της ηπατικής φλέβας) , στη μεσεντέρια, στις νεφρικές, αλλά και στις φλέβες του άνω άκρου.[2] Δεν έχει ακόμα εξακριβωθεί το εάν η θρομβοφιλία αυξάνει τον κίνδυνο εμφάνισης αρτηριακής θρόμβωσης (η οποία αποτελεί υποβόσκουσα αιτία καρδιακής ανακοπής ή αποπληξίας).[2][8][9]
Η θρομβοφιλία έχει συνδεθεί με επαναλαμβανόμενες αποβολές [10] και πιθανώς με ποικίλες επιπλοκές κατά την εγκυμοσύνη, όπως είναι η περιορισμένη ενδομήτρια ανάπτυξη του εμβρύου, η θνησιγένεια, σοβαρή προεκλαμψία ή και πρόωρη αποκόλληση του πλακούντα.[2]
Η έλλειψη πρωτεΐνης C μπορεί να προκαλέσει κεραυνοβόλο πορφύρα, μία σοβαρή θρομβωτική ανωμαλία των νεογέννητων που οδηγεί τόσο σε ιστικό θάνατο αλλά και σε αιμορραγία στο δέρμα και σε άλλα όργανα. Έχουνε παρατηρηθεί περιστατικά και σε ενήλικες. Έλλειψη πρωτεϊνών C ή S έχει επίσης συσχετισθεί με αυξημένο κίνδυνο για νέκρωση του δέρματος κατά την έναρξη αντιπηκτικής αγωγής με ουαρφαρίνη ή άλλα παρεμφερή φάρμακα.[2][11]
Αιτίες[Επεξεργασία | επεξεργασία κώδικα]
Η θρομβοφιλία είναι είτε συγγενής είτε επίκτητη. Η συγγενής θρομβοφιλία αφορά σύμφυτες καταστάσεις (συχνά κληρονομήσιμες, οπότε μπορεί να χρησιμοποιηθεί ο όρος «κληρονομική θρομβοφιλία») που αυξάνουν την πιθανότητα να αναπτυχθεί θρόμβωση, ενώ, από την άλλη πλευρά, η επίκτητη θρομβοφιλία σχετίζεται με καταστάσεις που προκύπτουν αργότερα στη ζωή κάποιου.
Συγγενής θρομβοφιλία[Επεξεργασία | επεξεργασία κώδικα]
Οι πιο συχνοί τύποι συγγενούς θρομβοφιλίας είναι εκείνοι που εμφανίζονται ως αποτέλεσμα της υπερβολικής δραστηριότητας κάποιων πηκτικών παραγόντων. Είναι σχετικά ήπιες παθήσεις και ως εκ τούτου χαρακτηρίζονται ως «τύπου ΙΙ».[12] Οι πιο κοινές από αυτές είναι ο παράγοντας V Leiden (μία μετάλλαξη του γονιδίου F5 στη θέση 1691) και η μετάλλαξη της προθρομβίνης (στη θέση 20210, στην περιοχή του υποκινητή του εν λόγω γονιδίου).[1][13]
Οι σπάνιες μορφές συγγενούς θρομβοφιλίας συνήθως προκαλούνται από έλλειψη φυσικών αντιπηκτικών. Χαρακτηρίζονται ως «τύπου Ι» και είναι πιο πιθανό να προκαλέσουν θρόμβωση.[12] Οι βασικές είναι η έλλειψη αντιθρομβίνης ΙΙΙ, η έλλειψη πρωτεΐνης C ή S.[1][13] Ηπιότερες σπάνιες συγγενείς θρομβοφιλίες είναι η μετάλλαξη του παράγοντα ΧΙΙΙ[13] και η οικογενής dysfibrinofenemia (ένα μη φυσιολογικό ινωδογόνο).[13] Δεν έχει αποσαφηνιστεί το αν οι συγγενείς διαταραχές της ινωδόλυσης (του συστήματος που καταστρέφει τους θρόμβους) αποτελούν βασικοί παράγοντες κινδύνου για τη θρόμβωση.[12] Για παράδειγμα, η συγγενής έλλειψη του πλασμινογόνου εμφανίζει κυρίως συμπτώματα στον οφθαλμό και ορισμένες φορές προβλήματα σε άλλα όργανα, αλλά η συσχέτιση της με τη θρόμβωση είναι ακόμη αβέβαιη.[14]
Η ομάδα αίματος καθορίζει τον ποσοστό κινδύνου για θρόμβωση σε μεγάλο βαθμό. Τα άτομα τα όποια που δεν έχουν ομάδα αίματος 0 έχουν διπλάσιο με τετραπλάσιο σχετικό κίνδυνο, ενώ αυτοί που έχουν εμφανίζουν χαμηλότερα επίπεδα 2 πρωτεϊνών του αίματος, του παράγοντα Von Willebrand και του παράγοντα VIII, οι οποίες παρέχουν προστασία απέναντι στη θρόμβωση.[5]
Επίκτητη θρομβοφιλία[Επεξεργασία | επεξεργασία κώδικα]
Ένας αριθμός επίκτητων θρομβοφιλιών αυξάνουν τον κίνδυνο θρόμβωσης. Ένα εξέχον παράδειγμα είναι το αντιφωσφολιπιδικό σύνδρομο,[1][13] το οποίο προκαλείται από αντισώματα ενάντια σε συστατικά της κυτταρικής μεμβράνης, κυρίως το αντιπηκτικό (αντίσωμα) του λύκου (το οποίο αρχικά εντοπίστηκε σε άτομα που έπασχαν από συστηματικό ερυθηματώδη λύκο, αλλά συχνά ανιχνεύεται και σε υγιή άτομα), αντισώματα της αντί-καρδιολιπίνης και το αντίσωμα της αντί-β2-γλυκοπρωτεΐνης. Ως εκ τούτου, το αντιφωσφολιπιδικό σύνδρομο θεωρείται αυτοάνοσο νόσημα. Σε ορισμένες περιπτώσεις, το σύνδρομο αυτό μπορεί να προκαλέσει αρτηριακή ή φλεβική θρόμβωση. Σχετίζεται στενά με αποβολές και μπορεί να εμφανίσει πολλά ακόμη συμπτώματα, όπως δικτυωτή πελίδνωση του δέρματος και ημικρανία.[15]
Η προκαλούμενη από ηπαρίνη (ηπαρινοεπαγόμενη) θρομβοκυτοπενία οφείλεται στη συστηματική ανοσοποιητική αντίδραση απέναντι στο αντιπηκτικό φάρμακο ηπαρίνη ή τα παράγωγά του.[1] Ενώ, σύμφωνα με το όνομά του, συνδέεται με χαμηλό αριθμό θρομβοκυττάρων (αιμοπεταλίων) το νόσημα αυτό σχετίζεται με υψηλό κίνδυνο θρόμβωσης.[16] Η παροξυσμική νυκτερινή αιμοσφαιρινουρία είναι μία σπάνια πάθηση που προκύπτει από επίκτητες μεταλλάξεις στο γονίδιο PIGA, το οποίο παίζει ρόλο στην προστασία των κυττάρων του αίματος από το σύστημα του συμπληρώματος. Η ασθένεια αυτή αυξάνει τον κίνδυνο φλεβικής θρόμβωσης, αλλά συνδέεται επίσης με την αιμολυτική αναιμία, η οποία προκύπτει από την καταστροφή των κυττάρων του αίματος. Και τα δύο προαναφερθέντα νοσήματα απαιτούν ειδική αγωγή.[17] Both HIT and PNH require particular treatment.[16][17]
Αιματολογικές εξετάσεις που επίσης σχετίζονται με αργή ροή αίματος μπορεί επίσης να αυξήσουν τις πιθανότητες θρόμβωσης. Για παράδειγμα, η δρεπανοκυτταρική αναιμία (προκαλούμενη από μετάλλαξη στο γονίδιο της αιμοσφαιρίνης) θεωρείται ως ήπια προθρομβωτική κατάσταση που προκαλείται από την παρεμπόδιση της ροής του αίματος.[1] Παρομοίως, οι μυελοϋπερπλαστικές διαταραχές, στις οποίες ο μυελός των οστών παράγει κύτταρα του αίματος σε μεγαλύτερο βαθμό από τον κανονικό, προδιαθέτουν την εμφάνιση θρόμβωσης, ιδιαιτέρως στην ιδιοπαθή πολυερυθραιμία (μεγάλος αριθμός ερυθροκυττάρων) και στη βασική θρομβοκύτωση (μεγάλος αριθμός θρομβοκυττάρων). Αυτές οι παθήσεις, όταν διαγνωστούν, απαιτούν ειδική αγωγή, όπως και προηγουμένως.[18]
Ο καρκίνος, ειδικά ο μεταστατικός (που εξαπλώνεται σε άλλα μέρη του σώματος), αποτελεί αναγνωρισμένο παράγοντα κινδύνου για τη θρόμβωση.[2][13] Έχει προταθεί ένας αριθμός μηχανισμών για την εξήγηση αυτού, όπως η ενεργοποίηση του συστήματος πήξης από τα καρκινικά κύτταρα ή η έκκριση προπηκτικών ουσιών. Επιπροσθέτως, ορισμένες αντικαρκινικές θεραπείες (όπως η χρήση κεντρικών φλεβικών καθετήρων για χημειοθεραπεία) μπορεί να αυξήσουν περαιτέρω τον κίνδυνο για θρόμβωση.[19]
Το νεφρωσικό σύνδρομο, στο οποίο πρωτεΐνες από την κυκλοφορία του αίματος αποβάλλονται μέσω των ούρων λόγω ασθενειών των νεφρών, προδιαθέτει την εμφάνιση θρόμβωσης.[1] Αυτό συμβαίνει ιδιαίτερα στις πιο σοβαρές παθήσεις (όπως υποδεικνύεται από το επίπεδο λευκωματίνης στο αίμα που είναι κάτω από 25g/l) και σε περιπτώσεις όπου το σύνδρομο οφείλεται στη μεμβρανώδη νεφροπάθεια.[20] Οι φλεγμονώδεις εντερικές ασθένειες (ελκώδης κολίτιδα και νόσος του Crohn) προδιαθέτουν την εμφάνιση θρόμβωσης, ειδικά όταν η ασθένεια είναι ενεργός. Ποικίλοι μηχανισμοί έχουν προταθεί για την εξήγηση αυτού.[2][21]
Η εγκυμοσύνη συσχετίζεται με αυξημένο κίνδυνο θρόμβωσης. Αυτό προφανώς απορρέει από τη φυσιολογική υπερπηκτικότητα της εγκυμοσύνης, η οποία προστατεύει τη μητέρα από αιμορραγία μετά τη γέννηση.[22]
Η γυναικεία ορμόνη οιστρογόνο, όταν χρησιμοποιείται στο συνδυασμένο αντισυλληπτικό χάπι (για από του στόματος χρήση) και στην ορμονική θεραπεία για περιεμμηνοπαυσιακές γυναίκες έχει συσχετισθεί με διπλάσιο έως εξαπλάσιο κίνδυνο φλεβικής θρόμβωσης. Ο κίνδυνος εξαρτάται από τον τύπο των χρησιμοποιούμενων ορμονών, τη δόση του οιστρογόνου και την παρουσία άλλων θρομβοφιλικών παραγόντων κινδύνου.[23] Ποικίλοι μηχανισμοί, όπως η έλλειψη πρωτεΐνης S και το πολυπεπτίδιο αναστολέας της οδού του ιστικού παράγοντα (TFPI) λέγεται πως ευθύνονται.[24]
Η παχυσαρκία θεωρείται εδώ και πολύ καιρό ως παράγοντας κινδύνου για τη φλεβική θρόμβωση. Υπερδιπλασιάζει τον κίνδυνο, σύμφωνα με πολλές μελέτες, ιδιαιτέρως σε συνδυασμό με τη χρήση αντισυλληπτικού χαπιού ή σε περίοδο μετά από εγχείρηση. Πολλές ανωμαλίες της πήξης έχουν περιγραφεί σε παχύσαρκα άτομα. Ο αναστολέας του ενεργοποιητή του πλασμινογόνου (PAI-1), ένας αναστολέας της ινωδόλυσης, υπάρχει σε υψηλότερο επίπεδο σε παχύσαρκα άτομα, τα οποία επίσης παρουσιάζουν μεγαλύτερο αριθμό κυκλοφορούντων μικροκυστών (θραύσματα κατεστραμμένων κυττάρων). Μπορεί επίσης να αυξηθούν οι συσσωρεύσεις αιμοπεταλίων καθώς και τα επίπεδα πηκτικών πρωτεϊνών, όπως ο παράγοντας von Willebrand, το ινωδογόνο, οι παράγοντες VII και VIII. Η παχυσαρκία επίσης αυξάνει τον κίνδυνο επανάληψης ενός επεισοδίου θρόμβωσης.[25]
Θρομβοφιλία με αδιευκρίνιστα αίτια[Επεξεργασία | επεξεργασία κώδικα]
Ένας αριθμός παθήσεων που έχουν συνδεθεί με τη φλεβική θρόμβωση είναι πιθανώς συγγενείς και πιθανώς επίκτητες.[13] Αυτές περιλαμβάνουν: υψηλά επίπεδα των παραγόντων VIII, IX, XI, του ινωδογόνου, του αναστολέα της ινωδόλυσης μέσω ενεργοποίησης της θρομβίνης, αλλά και μειωμένα επίπεδα του αναστολέα της οδού του ιστικού παράγοντα. Η αντίσταση στην ενεργοποιημένη βιταμίνη C που δεν οφείλεται σε μετάλλαξης του παράγοντα V προκαλείται προφανώς από άλλους παράγοντες και εγκυμονεί κίνδυνο θρόμβωσης.[13]
Υπάρχει συσχέτιση μεταξύ του επιπέδου της ομοκυστεΐνης στο αίμα και της θρόμβωσης,[13] ωστόσο δεν αναφέρεται σταθερά σε όλες τις μελέτες.[5] Τα επίπεδα ομοκυστεΐνης καθορίζονται από μεταλλάξεις στα γονίδια MTHFR και CBS, αλλά επίσης και από τα επίπεδα του φολικού οξέος, των βιταμινών Β6 και Β12, τα οποία εξαρτώνται από τη διατροφή.[12]
Μηχανισμός[Επεξεργασία | επεξεργασία κώδικα]
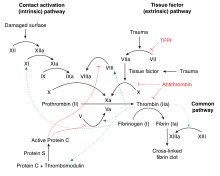
Η θρόμβωση είναι ένα πολυλειτουργικό πρόβλημα, καθώς υπάρχουν συχνά πολλαπλοί λόγοι για τους οποίους ένα άτομο αναπτύσσει την ασθένεια αυτή. Οι λόγοι αυτοί περιλαμβάνουν οποιονδήποτε συνδυασμό ανωμαλιών στα τοιχώματα των αγγείων (όπως στη στάση του αίματος) και ανωμαλιών στη σύσταση του αίματος. Η θρομβοφιλία οφείλεται σε ανωμαλίες της σύστασης του αίματος, η οποία καθορίζεται από το επίπεδο πηκτικών παραγόντων και άλλων κυκλοφορούντων πρωτεϊνών του αίματος που συμμετέχουν στη διαδικασία της πήξης.[13]
Η φυσιολογική πήξη πυροδοτείται από την απελευθέρωση του ιστικού παράγοντα από τον κατεστραμμένο ιστό. Ο ιστικός παράγοντας συνδέεται με τον παράγοντα VIIa, ο οποίος κυκλοφορεί στο αίμα. Η σύνδεση αυτή μετατρέπει τον παράγοντα Χ στον ενεργό Χa και τον παράγοντα ΙΧ στον ενεργό IXa. Ο παράγοντας Xa (υπό την παρουσία του παράγοντα V) μετατρέπει την προθρομβίνη στην ενεργή θρομβίνη. Η θρομβίνη αποτελεί κεντρικό ένζυμο στη διαδικασία της πήξης: παράγει ινώδες από το ινωδογόνο και ενεργοποιεί ορισμένα άλλα ένζυμα και συμπαράγοντες (παράγοντες XII, IX, V, VIII και ΤΑFI) που διευκολύνουν την πήξη του ινωδογόνου.[12] Η διαδικασία αναστέλλεται από το ΤFPI (το οποίο παρεμποδίζει τη δράση του παράγοντα VIIa / του ιστικού παράγοντα), από την αντιθρομβίνη (απενεργοποιεί τη θρομβίνη και τους παράγοντες IXa, Xa και Xia), από την πρωτεΐνη C (η οποία αναστέλλει τη δράση των παραγόντων Va και VIIIa υπό την παρουσία της πρωτεΐνης S) και από την πρωτεΐνη Ζ (η οποία αναστέλλει τη δράση του παράγοντα Xa).[12]
Στη θρομβοφιλία, η ισορροπία μεταξύ προπηκτικής και αντιπηκτικής δραστηριότητας διαταράσσεται. Η σοβαρότητα της ανισορροπίας καθορίζει την πιθανότητα ανάπτυξης θρόμβωσης. Ακόμα και μικρές ελλείψεις πρωτεϊνών, όπως η μείωση της αντιθρομβίνης σε ποσοστό 70-80% σε σχέση με το φυσιολογικό, μπορεί να αυξήσει τον κίνδυνο θρόμβωσης, σε αντιπαράθεση με την αιμοφιλία, η οποία προκύπτει μόνο αν οι παράγοντες πήξης μειωθούν σημαντικά.[12]
Εκτός από τη δημιουργία θρόμβωσης, η υπερπηκτικότητα μπορεί να επιταχύνει την ανάπτυξη αθηροσκλήρωσης, της αρτηριακής ασθένειας που προδιαθέτει για έμφραγμα του μυοκαρδίου και άλλες καρδιαγγειακές νόσους.[26][27]
Διάγνωση[Επεξεργασία | επεξεργασία κώδικα]

Οι εξετάσεις για τη θρομβοφιλία περιλαμβάνουν την πλήρη εξέταση αίματος (από επίχρισμα αίματος του ασθενούς), του χρόνου προθρομβίνης, του μερικού χρόνου θρομβοπλαστίνης, του χρόνου θρομβίνης, του χρόνου ρεπτιλάσης, του αντιπηκτικού του λύκου, του αντικαρδιολιπιδικού αντισώματος, του αντισώματος της αντι-β2-γλυκοπρωτεΐνης-1, της αντίστασης της ενεργοποιημένης πρωτεΐνης C, του ινωδογόνου, του παράγοντα V Leiden, της μετάλλαξης της προθρομβίνης και των επιπέδων της βασικής ομοκυστεΐνης.[2] Οι εξετάσεις μπορεί να είναι περισσότερο ή λιγότερο εκτενείς, ανάλογα με την κρίση του ιατρού κατά την κλινική εξέταση και τις εντοπιζόμενες ανωμαλίες στην αρχική εκτίμηση.[2]
Υπάρχουν διαφορετικές απόψεις σχετικά με το αν πρέπει κάθε άτομο με απρόκλητα επεισόδια θρόμβωσης να ερευνά την ύπαρξη θρομβοφιλίας. Ακόμα και αυτοί που έχουν κάποιο τύπο θρομβοφιλίας μπορεί να μη βρίσκονται απαραίτητα σε κίνδυνο για επανεμφάνιση θρόμβωσης, ενώ οι επαναλαμβανόμενες θρομβώσεις είναι πιο πιθανές σε αυτούς που είχαν προηγουμένως επεισόδιο θρόμβωσης, ακόμα και σε αυτούς που δεν έχουν ανιχνεύσιμες θρομβοφιλικές ανωμαλίες.[8][11][28] Επαναλαμβανόμενες θρομβοεμβολές ή θρομβώσεις σε ασυνήθιστες περιοχές (π.χ. στην ηπατική φλέβα στο σύνδρομο Budd-Chiarri) αποτελούν γενικά αποδεκτές ενδείξεις για εξέταση. Είναι πιο πιθανό να συμφέρει οικονομικά σε σχέση με αυτά που προσφέρει αυτή η εξέταση σε άτομα με αξιοσημείωτο προσωπικό ή οικογενειακό ιστορικό θρομβώσεων.[29] Από την άλλη πλευρά, ο συνδυασμός θρομβοφιλίας με άλλους παράγοντες κινδύνου μπορεί να αποτελεί ένδειξη προληπτικής αγωγής και αυτός είναι ο λόγος για τον οποίο τα άτομα εξετάζονται για θρομβοφιλία ακόμα και όταν δεν πληρούνται αυστγρώς τα κριτήρια.[28] Η αναζήτηση για ανωμαλίες στην πήξη δε διενεργούνται σε ασθενείς στους οποίους είναι προφανές το αίτιο που πυροδότησε τη θρόμβωση. Παραδείγματος χάριν, αν η θρόμβωση προκύπτει μετά από στάση του αίματος λόγω πρόσφατης ορθοπεδικής εγχείρισης, θεωρείται πως πυροδοτήθηκε από την εγχείριση και τη στάση του αίματος και περαιτέρω έλεγχος δύσκολα θα αποκαλύψει σημαντικά στοιχεία.[11][28]
Στο Ηνωμένο Βασίλειο, σύμφωνα με επαγγελματικές οδηγίες υπάρχουν συγκεκριμένες ενδείξεις για εξέταση ενός ατόμου σχετικά με τη θρομβοφιλία. Η εξέταση πρέπει να γίνεται μόνο μετά από κατάλληλη σύσκεψη ασθενούς – ιατρού και, ως εκ τούτου, συνήθως η διερεύνηση δεν πραγματοποιείται αμέσως μόλις διαγνωσθεί η θρόμβωση, αλλά μετά από κάποιο χρονικό διάστημα.[11] Σε ειδικές περιστάσεις (όπως στη θρόμβωση φλέβας του αμφιβληστροειδή) η εξέταση δεν ενδείκνυται, καθώς η θρομβοφιλία δε θεωρείται σημαντικός παράγοντας κινδύνου. Σε άλλες σπάνιες καταστάσεις συνδεδεμένες με την υπερπηκτικότητα, όπως η θρόμβωση εγκεφαλικών φλεβών ή της πυλαίας φλέβας, δεν υπάρχουν αρκετά στοιχεία για να διευκρινιστεί εάν η εξέταση για θρομβοφιλία θα αποβεί χρήσιμη και, επομένως, τέτοιες αποφάσεις κρίνεται πως δε στηρίζονται σε στοιχεία.[11] Αν ληφθεί υπόψη το κόστος των εξετάσεων αυτών σε σχέση με τα οφέλη τους, δεν είναι σίγουρο το ότι δικαιολογούν το υψηλό τους κόστος,[30] εκτός από τις περιπτώσεις στις οποίες περιορίζονται σε επιλεγμένες περιπτώσεις.[31]
Οι πολλαπλές αποβολές αποτελούν ένδειξη για διερεύνηση ενός ατόμου για θρομβοφιλία, ιδίως για εξέταση αντιφωσφολιπιδικών αντισωμάτων (αντικαρδιολιπίνης IgG και IgM, αλλά και αντιπηκτικού του λύκου), παράγοντα V Leiden, μετάλλαξης της προθρομβίνης, αντίστασης της ενεργοποιημένης πρωτεΐνης C και γενική εκτίμηση της πήξης μέσω εξέτασης γνωστής ως «θρομβοελαστογραφία».[10]
Οι γυναίκες που σκοπεύουν να χρησιμοποιήσουν από του στόματος αντισυλληπτικά χάπια δε θα επωφεληθούν από έλεγχο για τη θρομβοφιλία, καθώς ο απόλυτος κίνδυνος εμφάνισης θρομβωτικού επεισοδίου είναι χαμηλός. Εάν αυτή η γυναίκα ή κάποιος συγγενής πρώτου βαθμού έχει υποστεί θρόμβωση, τότε ο κίνδυνος εμφάνισης τέτοιου επεισοδίου είναι υψηλότερος. Ο έλεγχος αυτός των επιλεγμένων γυναικών μπορεί να είναι ωφέλιμος,[24] ωστόσο ακόμη και αρνητικό αποτέλεσμα στις εξετάσεις δεν αποκλείει εντελώς την ύπαρξη κινδύνου.[11] Οι επαγγελματικές οδηγίες προτείνουν, λοιπόν, τη χρήση εναλλακτικών τρόπων αντισύλληψης, ακόμα και σε αρνητικό αποτέλεσμα της διερεύνησης.[11]
Ο έλεγχος για θρομβοφιλία σε άτομα με αρτηριακή θρόμβωση θεωρείται γενικά άκαρπος και αποδοκιμάζεται,[11] εκτός πιθανόν από τις περιπτώσεις ασυνήθιστα νέων ασθενών (ειδικά όταν οφείλεται σε κάπνισμα ή χρήση ορμονικών αντισυλληπτικών που περιέχουν οιστρογόνο) και περιπτώσεις ατόμων στα οποία η επαναγγείωση, όπως η παράκαμψη (bypass) στεφανιαίων αρτηριών, αποτυγχάνει λόγω ταχείας απόφραξης του μοσχεύματος.[9]
Θεραπεία[Επεξεργασία | επεξεργασία κώδικα]
Σε όσους ασθενείς ο κίνδυνος θρόμβωσης εξαιτίας θρομβοφιλίας είναι αυξημένος, συνίσταται η χορήγηση ουαρφαρίνης(warfarin) για μακρά χρονικά διαστήματα ή και για πάντα. Δεν υπάρχει κάποια συγκεκριμένη θεραπεία για τη θρομβοφιλία εκτός κι αν οφείλεται σε άλλη ασθένεια(νεφρωσικό σύνδρομο) οπότε σε αυτή την περίπτωση ακολουθούμε τη θεραπεία για τη συγκεκριμένη ασθένεια. Σε ασθενείς με απρόκλητα ή/και επαναλαμβανόμενα θρομβωτικά επεισόδια η πιο σημαντική απόφαση είναι εάν θα χορηγήσουμε αντιπηκτικά φάρμακα, όπως η warfarin, για μεγάλο χρονικό διάστημα για να μειώσουμε τον κίνδυνο επανεμφάνισης θρομβωτικών επεισοδίων.[3] Ο κίνδυνος αυτός θα πρέπει να εκτιμηθεί σε σχέση με τον κίνδυνο που υπάρχει να προκληθεί αιμορραγία από τα αντιπηκτικά φάρμακα. Ο συγκεκριμένος κίνδυνος για τους ασθενείς σε θεραπεία είναι 3% τον χρόνο και 11% αυτών με σημαντική αιμορραγία πεθαίνουν.[3]
Ο κίνδυνος επανεμφάνισης ενός θρομβωτικού επεισοδίου εξαρτάται από παράγοντες όπως: α)η έκταση και η σοβαρότητα της θρόμβωσης, β)η αιτία πρόκλησης(π.χ. ακινησία, εγκυμοσύνη), γ)ο αριθμός των θρομβωτικών επεισοδίων, δ)το φύλο, ε)η ύπαρξη φίλτρου στην κάτω κοίλη φλέβα, στ) η παρουσία καρκίνου, ζ)συμπτώματα μετά-θρομβωτικού επεισοδίου και η)η παχυσαρκία.[3] Αυτοί οι παράγοντες φαίνεται να είναι πιο σημαντικά στοιχεία σε σχέση με την απουσία ή παρούσία μίας ανιχνεύσιμιμης θρομβοφιλίας.[11][32]
Σε όσους πάσχουν από αντιφωσφολιπιδικό σύνδρομο συνίσταται η μακρόχρονη χορήγηση αντιπηκτικών φαρμάκων μετά από ένα απρόκλητο επεισόδιο θρόμβωσης. Ο κίνδυνος εξαρτάται από τον τύπο του αντισώματος, από τον τίτλο(ποσότητα) του αντισώματος από την παρουσία πολλαπλών αντισωμάτων κι από το εάν πρόκειται για μεμονωμένο επεισόδιο ή για επαναλαμβανόμενα.[15]
Έγκυες γυναίκες με θρομβοφιλία παίρνουν άλλα φάρμακα αντί για ουαρφαρίνη, ειδικά τις πρώτες 13 εβδομάδες της εγκυμοσύνης επειδή μπορεί να προκληθούν ανωμαλίες στο έμβρυο. Η χαμηλού μοριακού βάρους ηπαρίνη(LMWH, όπως η enoxaparin) χρησιμοποιείται ευρύτατα σαν εναλλακτική λύση.[33] Η ουαρφαρίνη και η LMWH μπορούν να χορηγηθούν άφοβα κατά τον θηλασμό.[33]
Πρόγνωση[Επεξεργασία | επεξεργασία κώδικα]
Σε ανθρώπους χωρίς ανιχνεύσιμη θρομβοφιλία ο κίνδυνος να αναπτυχθεί θρόμβωση μέχρι την ηλικία των 60 είναι 12%. Περίπου 60% όσων έχουν ανεπάρκεια αντιθρομβίνης θα εμφανίσουν θρόμβωση τουλάχιστον μια φορά μέχρι τα 60. Το ίδιο θα συμβεί με το 50% όσων έχουν ανεπάρκεια της πρωτεΐνης S, Αντίθετα, όσοι εμφανίζουν αντίσταση στην ενεργοποιημένη πρωτεΐνη C(εξαιτίας του παράγοντα V Leiden) εμφανίζουν μια ελάχιστη αύξηση κινδύνου να πάθουν θρόμβωση, με το 15% να έχει τουλάχιστον ένα θρομβωτικό επεισόδιο μέχρι τα 60.[12] Γενικώς οι άνδρες είναι πιο πιθανό να εμφανίσουν επαναλαμβανόμενα επεισόδια θρόμβωσης στις φλέβες.[5]
Οι άνθρωποι με τον παράγοντα V Leiden είναι σε σχετικά μικρό κίνδυνο να εμφανίσουν θρόμβωση αλλά ίσως αναπτύξουν με την παρουσία κάποιου άλλου παράγοντα, όπως η ακινησία. Οι περισσότεροι με μετάλλαξη στο γονίδιο της προθρομβίνης(G20210A) δεν αναπτύσσουν θρόμβωση.[12]
Επιδημιολογία[Επεξεργασία | επεξεργασία κώδικα]
Οι σοβαρότερες θρομβοφιλίες(τύπου I) είναι σπάνιες. Ανεπάρκεια στην αντιθρομβίνη εμφανίζει μόνο το 0,2% του γενικού πληθυσμού και 0,5-7,5% των ανθρώπων με θρόμβωση στις φλέβες. Ανεπάρκεια στην πρωτεΐνη C εμφανίζει επίσης το 0.2% του πληθυσμού και 2,5-6% των ανθρώπων με θρόμβωση. Ανεπάρκεια στην πρωτεΐνη S εμφανίζει το 1,3-5% των ανθρώπων με θρόμβωση, ενώ το ποσοστό στον γενικό πληθυσμό είναι άγνωστο.[12]
Οι ηπιότερες θρομβοφιλίες(τύπου II) είναι πολύ συχνότερες. Ο παράγοντας V Leiden υπάρχει στο 5% του πληθυσμού της Βόρειας Ευρώπης ενώ είναι πολύ σπανιότερος στην Ασία και την Αφρική. Από τους ανθρώπους με θρόμβωση 10% έχουν τον παράγοντα V Leiden ενώ από αυτούς που παραπέμφθηκαν για θρομβοφιλικό τεστ 30-50%. Η μετάλλαξη της προθρομβίνης υπάρχει στο 1-4% του γενικού πληθυσμού, στο 5-10% των ανθρώπων με θρόμβωση και στο 15% όσων έκαναν το θρομβοφιλικό τεστ. Όπως και ο παράγοντας V Leiden, η μετάλλαξη στη προθρομβίνη είναι σπάνια στην Ασία και στην Αφρική.[12] Στον ελληνικό πληθυσμό η συχνότητα της κληρονομικής προδιάθεσης για θρομβοφιλία θεωρείται ότι είναι περίπου 10-15%.[34][35][36]
Για το αντιφωσφολιπιδικό σύνδρομο δεν είναι γνωστά τα ακριβή ποσοστά. Τα αντιφωσφολιπιδικά αντισώματα ανευρίσκονται στο 24% όσων παραπέμπονται για θρομβοφιλικό τεστ.[15]
Ιστορική αναδρομή[Επεξεργασία | επεξεργασία κώδικα]

Ο Γερμανός παθολόγος Rudolf Virchow ενοχοποίησε τις ανωμαλίες στη σύσταση του αίματος για την ανάπτυξη θρόμβωσης, το 1856. Η ακριβής όμως φύση αυτών των ανωμαλιών παρέμεινε αβέβαιη μέχρι το 1965, όταν ο Νορβηγός αιματολόγος Olav Egeberg περιέγραψε την έλλειψη αντιθρομβίνης.[37] Ακολούθησαν η έλλειψη πρωτεΐνης C to 1981(από το Scripps Research Institute και από το Centers of Disease Control)[38] και η έλλειψη πρωτεΐνης S το 1984( από το University of Oklahoma).[4][5][39]
Το αντιφωσφολιπιδικό σύνδρομο περιγράφηκε πλήρως τη δεκαετία του 80 μετά από πολλές αναφορές για συγκεκριμένα αντισώματα σε άτομα με συστηματικό ερυθηματώδη λύκο και θρόμβωση.[15][40] Η ανακάλυψη του συνδρόμου αποδίδεται στον Βρετανό ρευματολόγο Graham R.V. Hughes και για αυτό πολλές φορές αναφέρεται σαν σύνδρομο Hughes.[41]
Οι πιο συχνές γενετικές θρομβοφιλίες περιγράφηκαν στη δεκαετία του 90. Πολλές έρευνες έδειχναν ότι άνθρωποι με θρόμβωση εμφανίζουν αντίσταση στην ενεργοποιημένη πρωτεΐνη C. Το 1994 μια ομάδα στο Leiden(Λέιντεν),στην Ολλανδία, ανέδειξε μια σημαντική μετάλλαξη στον παράγοντα V που τον έκανε να αντιστέκεται στην ενεργοποιημένη πρωτεΐνη C.Για αυτόν τον λόγο, ο μεταλλαγμένος αυτός παράγοντας ονομάστηκε παράγοντας V Leiden.[42] Δύο χρόνια αργότερα, η ίδια ομάδα περιέγραψε μια κοινή μετάλλαξη στο γονίδιο της προθρομβίνης που προκαλεί αύξηση των επιπέδων προθρομβίνης και μια ήπια αύξηση του κινδύνου ανάπτυξης θρόμβωσης.[4][5][43]
Στο μέλλον, περισσότερα μπορούν να ανακαλυφθούν σχετικά με τις θρομβώσεις με έρευνες σε όλον τον γενετικό κώδικα, ψάχνοντας για μικρές μεταλλάξεις στα γονίδια.[4][5]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Mitchell RS· Kumar V· Abbas AK· Fausto N (2007). «Chapter 4». Robbins Basic Pathology (Eighth έκδοση). Philadelphia: Saunders. ISBN 1-4160-2973-7.
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 Heit JA (2007). «Thrombophilia: common questions on laboratory assessment and management». Hematology Am. Soc. Hematol. Educ. Program 2007 (1): 127–35. doi:. PMID 18024620. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-10-03. https://web.archive.org/web/20111003222726/http://asheducationbook.hematologylibrary.org/cgi/content/full/2007/1/127. Ανακτήθηκε στις 2011-11-27.
- ↑ 3,0 3,1 3,2 3,3 Kyrle PA, Rosendaal FR, Eichinger S (December 2010). «Risk assessment for recurrent venous thrombosis». Lancet 376 (9757): 2032–9. doi:. PMID 21131039.
- ↑ 4,0 4,1 4,2 4,3 Dahlbäck B (July 2008). «Advances in understanding pathogenic mechanisms of thrombophilic disorders». Blood 112 (1): 19–27. doi:. PMID 18574041. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-12-08. https://web.archive.org/web/20101208105640/http://bloodjournal.hematologylibrary.org/cgi/content/full/112/1/19. Ανακτήθηκε στις 2011-11-27.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 5,6 Rosendaal FR, Reitsma PH (July 2009). «Genetics of venous thrombosis». J. Thromb. Haemost. 7 Suppl 1: 301–4. doi:. PMID 19630821. http://onlinelibrary.wiley.com/doi/10.1111/j.1538-7836.2009.03394.x/full.
- ↑ Scarvelis D, Wells PS (October 2006). «Diagnosis and treatment of deep-vein thrombosis». CMAJ 175 (9): 1087–92. doi:. PMID 17060659. PMC 1609160. http://www.cmaj.ca/cgi/content/full/175/9/1087.
- ↑ Agnelli G, Becattini C (July 2010). «Acute pulmonary embolism». N. Engl. J. Med. 363 (3): 266–74. doi:. PMID 20592294.
- ↑ 8,0 8,1 Middeldorp S, van Hylckama Vlieg A (August 2008). «Does thrombophilia testing help in the clinical management of patients?». Br. J. Haematol. 143 (3): 321–35. doi:. PMID 18710381. http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2141.2008.07339.x/full.
- ↑ 9,0 9,1 de Moerloose P, Boehlen F (April 2007). «Inherited thrombophilia in arterial disease: a selective review». Semin. Hematol. 44 (2): 106–13. doi:. PMID 17433903.
- ↑ 10,0 10,1 Rai R, Regan L (August 2006). «Recurrent miscarriage». Lancet 368 (9535): 601–11. doi:. PMID 16905025.
- ↑ 11,0 11,1 11,2 11,3 11,4 11,5 11,6 11,7 11,8 Baglin T, Gray E, Greaves M, et al. (April 2010). «Clinical guidelines for testing for heritable thrombophilia». Br. J. Haematol. 149 (2): 209–20. doi:. PMID 20128794. http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2141.2009.08022.x/full.
- ↑ 12,00 12,01 12,02 12,03 12,04 12,05 12,06 12,07 12,08 12,09 12,10 Crowther MA, Kelton JG (2003). «Congenital thrombophilic states associated with venous thrombosis: a qualitative overview and proposed classification system». Ann. Intern. Med. 138 (2): 128–34. PMID 12529095. http://www.annals.org/cgi/reprint/138/2/128. Lay summary.
- ↑ 13,00 13,01 13,02 13,03 13,04 13,05 13,06 13,07 13,08 13,09 Rosendaal FR (2005). «Venous thrombosis: the role of genes, environment, and behavior». Hematology Am. Soc. Hematol. Educ. Program 2005 (1): 1–12. doi:. PMID 16304352. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-10-03. https://web.archive.org/web/20111003222500/http://asheducationbook.hematologylibrary.org/cgi/content/full/2005/1/1. Ανακτήθηκε στις 2011-11-27.
- ↑ Mehta R, Shapiro AD (November 2008). «Plasminogen deficiency». Haemophilia 14 (6): 1261–8. doi:. PMID 19141167. http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2516.2008.01825.x/full.
- ↑ 15,0 15,1 15,2 15,3 Ruiz-Irastorza G, Crowther M, Branch W, Khamashta MA (October 2010). «Antiphospholipid syndrome». Lancet 376 (9751): 1498–509. doi:. PMID 20822807.
- ↑ 16,0 16,1 Keeling D, Davidson S, Watson Η (May 2006). «The management of heparin-induced thrombocytopenia». Br. J. Haematol. 133 (3): 259–69. doi:. PMID 16643427. Αρχειοθετήθηκε από το πρωτότυπο στις 2012-12-10. https://archive.today/20121210042249/http://www3.interscience.wiley.com/cgi-bin/fulltext/118607806/HTMLSTART. Ανακτήθηκε στις 2011-11-27.
- ↑ 17,0 17,1 Brodsky RA (April 2008). «Narrative review: paroxysmal nocturnal hemoglobinuria: the physiology of complement-related hemolytic anemia». Ann. Intern. Med. 148 (8): 587–95. PMID 18413620. http://www.annals.org/content/148/8/587.full.
- ↑ Papadakis E, Hoffman R, Brenner B (Νοέμβριος 2010). «Thrombohemorrhagic complications of myeloproliferative disorders». Blood Rev. 24 (6): 227–32. doi:. PMID 20817333.
- ↑ Prandoni P., Falanga A., Piccioli A. (Ιούνιος 2005). «Cancer and venous thromboembolism». Lancet Oncol. 6 (6): 401–10. doi:. PMID 15925818.
- ↑ Hull RP, Goldsmith DJ (Μάιος 2008). «Nephrotic syndrome in adults». BMJ 336 (7654): 1185–9. doi:. PMID 18497417.
- ↑ Quera R., Shanahan F. (Οκτώβριος 2004). «Thromboembolism--an important manifestation of inflammatory bowel disease». Am. J. Gastroenterol. 99 (10): 1971–3. doi:. PMID 15447758. https://archive.org/details/sim_american-journal-of-gastroenterology_2004-10_99_10/page/1971.
- ↑ Bourjeily G., Paidas M., Khalil H., Rosene-Montella K., Rodger M. (Φεβρουάριος 2010). «Pulmonary embolism in pregnancy». Lancet 375 (9713): 500–12. doi:. PMID 19889451.
- ↑ Gomes M.P., Deitcher S.R. (Οκτώβριος 2004). «Risk of venous thromboembolic disease associated with hormonal contraceptives and hormone replacement therapy: a clinical review». Arch. Intern. Med. 164 (18): 1965–76. doi:. PMID 15477430. http://archinte.ama-assn.org/cgi/content/full/164/18/1965.
- ↑ 24,0 24,1 Tchaikovski S.N., Rosing J. (July 2010). «Mechanisms of estrogen-induced venous thromboembolism». Thromb. Res. 126 (1): 5–11. doi:. PMID 20163835. https://archive.org/details/sim_thrombosis-research_2010-07_126_1/page/n12.
- ↑ Stein P.D., Goldman J. (Σεπτέμβριος 2009). «Obesity and thromboembolic disease». Clin. Chest Med. 30 (3): 489–93, viii. doi:. PMID 19700047. https://archive.org/details/sim_clinics-in-chest-medicine_2009-09_30_3/page/489.
- ↑ Borissoff JI, Spronk HM, Heeneman S, ten Cate Η (2009). «Is thrombin a key player in the 'coagulation-atherogenesis' maze?». Cardiovasc Res. 820 (3): 392–403. doi:. PMID 19228706. http://cardiovascres.oxfordjournals.org/content/82/3/392.long.
- ↑ Borissoff JI, Spronk HM, ten Cate Η (2011). «The hemostatic system as a modulator of atherosclerosis». N. Engl. J. Med. 364 (18): 1746–1760. doi:. PMID 21542745.
- ↑ 28,0 28,1 28,2 Dalen JE (June 2008). «Should patients with venous thromboembolism be screened for thrombophilia?». Am. J. Med. 121 (6): 458–63. doi:. PMID 18501222. https://archive.org/details/sim_american-journal-of-medicine_2008-06_121_6/page/458.
- ↑ Wu O, Robertson L, Twaddle S, et al. (October 2005). «Screening for thrombophilia in high-risk situations: a meta-analysis and cost-effectiveness analysis». Br. J. Haematol. 131 (1): 80–90. doi:. PMID 16173967. http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2141.2005.05715.x/full.
- ↑ Simpson EL, Stevenson MD, Rawdin A, Papaioannou D (January 2009). «Thrombophilia testing in people with venous thromboembolism: systematic review and cost-effectiveness analysis». Health Technol. Assess. 13 (2): iii, ix–x, 1–91. doi:. PMID 19080721. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-07-24. https://web.archive.org/web/20110724095108/http://www.hta.ac.uk/execsumm/summ1302.htm. Ανακτήθηκε στις 2011-11-27.
- ↑ Wu O, Greer IA (September 2007). «Is screening for thrombophilia cost-effective?». Curr. Opin. Hematol. 14 (5): 500–3. doi:. PMID 17934357.
- ↑ Kearon C, Kahn SR, Agnelli G, Goldhaber S, Raskob GE, Comerota AJ (June 2008). «Antithrombotic therapy for venous thromboembolic disease: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition)». Chest 133 (6 Suppl): 454S–545S. doi:. PMID 18574272. Αρχειοθετήθηκε από το πρωτότυπο στις 2013-01-12. https://archive.today/20130112193314/http://chestjournal.chestpubs.org/content/133/6_suppl/454S.full. Ανακτήθηκε στις 2011-11-27.
- ↑ 33,0 33,1 Bates SM, Greer IA, Pabinger I, Sofaer S, Hirsh J (June 2008). «Venous thromboembolism, thrombophilia, antithrombotic therapy, and pregnancy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition)». Chest 133 (6 Suppl): 844S–886S. doi:. PMID 18574280. Αρχειοθετήθηκε από το πρωτότυπο στις 2013-01-12. https://archive.today/20130112124653/http://chestjournal.chestpubs.org/content/133/6_suppl/844S.long. Ανακτήθηκε στις 2011-11-27.
- ↑ Maniadakis, Nikos; Kourlaba, Georgia; Fragoulakis, Vasileios (2011-04-14). «Self-reported prevalence of atherothrombosis in a general population sample of adults in Greece; a telephone survey». BMC cardiovascular disorders 11: 16. doi:. ISSN 1471-2261. PMID 21492471. PMC PMC3104943. https://www.ncbi.nlm.nih.gov/pubmed/21492471.
- ↑ Gialeraki, Argyri; Politou, Marianna; Rallidis, Loukianos; Merkouri, Efrosyni; Markatos, Christos; Kremastinos, Dimitrios; Travlou, Anthi (2008-12-01). «Prevalence of prothrombotic polymorphisms in Greece». Genetic Testing 12 (4): 541–547. doi:. ISSN 1090-6576. PMID 19072566. https://www.ncbi.nlm.nih.gov/pubmed/19072566.
- ↑ Yapijakis, Christos; Serefoglou, Zoe; Nixon, Alexander M.; Vylliotis, Antonis; Ragos, Vassilis; Vairaktaris, Eleftherios (2012-11-01). «Prevalence of thrombosis-related DNA polymorphisms in a healthy Greek population». In Vivo (Athens, Greece) 26 (6): 1095–1101. ISSN 1791-7549. PMID 23160700. https://www.ncbi.nlm.nih.gov/pubmed/23160700.
- ↑ Egeberg Ο (June 1965). «Inherited antithrombin deficiency causing thrombophilia». Thromb. Diath. Haemorrh. 13: 516–30. PMID 14347873.
- ↑ Griffin JH, Evatt B, Zimmerman TS, Kleiss AJ, Wideman C (November 1981). «Deficiency of protein C in congenital thrombotic disease». J. Clin. Invest. 68 (5): 1370–3. doi:. PMID 6895379. PMC 370934. http://www.jci.org/articles/view/110385.
- ↑ Comp PC, Esmon CT (December 1984). «Recurrent venous thromboembolism in patients with a partial deficiency of protein S». N. Engl. J. Med. 311 (24): 1525–8. doi:. PMID 6239102.
- ↑ Hughes GR (October 1983). «Thrombosis, abortion, cerebral disease, and the lupus anticoagulant». Br. Med. J. (Clin Res Ed) 287 (6399): 1088–9. doi:. PMID 6414579.
- ↑ Sanna G, D'Cruz D, Cuadrado MJ (August 2006). «Cerebral manifestations in the antiphospholipid (Hughes) syndrome». Rheum. Dis. Clin. North Am. 32 (3): 465–90. doi:. PMID 16880079.
- ↑ Bertina RM, Koeleman BP, Koster T, et al. (May 1994). «Mutation in blood coagulation factor V associated with resistance to activated protein C». Nature 369 (6475): 64–7. doi:. PMID 8164741.
- ↑ Poort SR, Rosendaal FR, Reitsma PH, Bertina RM (November 1996). «A common genetic variation in the 3'-untranslated region of the prothrombin gene is associated with elevated plasma prothrombin levels and an increase in venous thrombosis» (PDF). Blood 88 (10): 3698–703. PMID 8916933. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-12-26. https://web.archive.org/web/20091226182405/http://bloodjournal.hematologylibrary.org/cgi/reprint/88/10/3698. Ανακτήθηκε στις 2011-11-27.
