Αβιδίνη
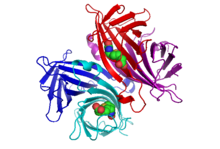

Η αβιδίνη (avidin) είναι μια τετραμερής πρωτεΐνη, που παράγεται στους ωαγωγούς των πτηνών, των ερπετών και των αμφιβίων, και αποτίθεται στο ασπράδι των αβγών τους. Διμερή μέλη της οικογένειας της αβιδίνης βρίσκονται επίσης σε ορισμένα βακτήρια.[1] Στο ασπράδι του αβγού της όρνιθας η αβιδίνη αποτελεί περίπου το 0,05% του συνολικού περιεχομένου σε πρωτεΐνες (περί το 1,8 χιλιοστό του γραμμαρίου ανά αβγό). Η αβιδίνη αποτελείται από 4 πανομοιότυπες υπομονάδες (ομοτετραμερές), η καθεμιά από τις οποίες μπορεί να δεσμεύσει από ένα μόριο βιοτίνης (βιταμίνης B7 ή H) με υψηλό βαθμό χημικής συγγένειας: Η σταθερά διάστασης του συμπλέγματος αβιδίνης-βιοτίνης είναι KD ≈ 10−15 M, γεγονός που φανερώνει ότι είναι ένας από τους ισχυρότερους γνωστούς μη-ομοιοπολικούς δεσμούς.[2]
Στην τετραμερή μορφή της η αβιδίνη εκτιμάται ότι έχει μοριακό βάρος 66.000 έως 69.000 Da.[3] Το 10% αυτού του βάρους αποτελείται από υδατάνθρακες, συγκεκριμένα από 4 έως 5 μονάδες μαννόζης και τρία υπόλοιπα N-ακετυλογλυκοζαμίνης.[4] Τα υδατανθρακικά μέρη του μορίου της αβιδίνης περιέχουν τουλάχιστον τρεις μοναδικούς δομικούς τύπους ολιγοσακχαριτών, που μοιάζουν μεταξύ τους στη δομή και τη σύσταση.[5]
Λειτουργική αβιδίνη βρίσκεται μόνο στα ωμά αβγά, καθώς η χημική συγγένειά της με τη βιοτίνη καταστρέφεται με το μαγείρεμα. Η αβιδίνη καταστρέφεται και με ακτινοβόληση. Στη δέσμευση της βιοτίνης από την αβιδίνη οφείλονται οι ελαφρές δερματίτιδες που παρουσιάζονται μετά τη λήψη ωμού ασπραδιού του αβγού.
Η φυσική λειτουργία της αβιδίνης στα ίδια τα αβγά είναι άγνωστη, αλλά έχει υποτεθεί ότι χρησιμεύει ως αναστολέας της αναπτύξεως βακτηρίων, δεσμεύοντας βιοτίνη που βοηθεί τη βακτηριακή ανάπτυξη. Πράγματι, η στρεπταβιδίνη, μια συγγενική πρωτεΐνη με ίση δεσμευτικότητα της βιοτίνης και πολύ παρόμοια θέση δεσμεύσεως, παρασκευάζεται από ορισμένα στελέχη βακτηρίων του γένους Streptomyces και πιστεύεται ότι χρησιμεύει στο να εμποδίζει την ανάπτυξη ανταγωνιστικών βακτηρίων.[6]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «Rhizavidin from Rhizobium etli: the first natural dimer in the avidin protein family». The Biochemical Journal 405 (3): 397–405. August 2007. doi:. PMID 17447892.
- ↑ «Avidin. 1. The Use of (14-C)Biotin for Kinetic Studies and for Assay». The Biochemical Journal 89 (3): 585–91. December 1963. doi:. PMID 14101979. PMC 1202466. https://archive.org/details/sim_biochemical-journal_1963-12_89_3/page/585.
- ↑ «Avidin, a high affinity biotin-binding protein, as a tool and subject of biological research». Medical Biology 62 (1): 5–26. 1984. PMID 6379329. https://archive.org/details/sim_medical-biology_1984_62_1/page/5.
- ↑ «Avidin». Advances in Protein Chemistry 29: 85–133. 1975. doi:. ISBN 978-0-12-034229-7. PMID 237414. https://books.google.com/books?id=sMgpDLCl2z8C&pg=PA85.
- ↑ «Compositional and structural heterogeneity of avidin glycopeptides». Biochemistry 21 (21): 5334–41. October 1982. doi:. PMID 6816268.
- ↑ «Crystal structure of core streptavidin determined from multiwavelength anomalous diffraction of synchrotron radiation». Proceedings of the National Academy of Sciences of the United States of America 86 (7): 2190–4. April 1989. doi:. PMID 2928324. Bibcode: 1989PNAS...86.2190H.
Πηγές
[Επεξεργασία | επεξεργασία κώδικα]- Το ομώνυμο λήμμα στην Εγκυκλοπαίδεια Πάπυρος-Larousse-Britannica, έκδ. 2006, τόμος 1, σελ. 105
