Διαμόρφωση (χημεία)

Διαμόρφωση (conformation)[Σημ. 1] είναι όρος της στερεοχημείας που υποδηλώνει τον κλάδο της χημείας, ειδικότερα της οργανικής, που ασχολείται με τις διάφορες μορφές που αποκτά ένα μόριο κατά την περιστροφή του γύρω από έναν απλό χημικό δεσμό (σ-δεσμό) μεταξύ δύο ατόμων άνθρακα[1].
Οι διαφορετικές διευθετήσεις-διατάξεις των ατόμων που μπορούν να μετατραπούν από τη μια μορφή στην άλλη με περιστροφή γύρω από απλούς δεσμούς ονομάζονται διαμορφώσεις[2].
Παλιότερα γινόταν δεκτό ότι μεταξύ δύο ατόμων άνθρακα ενωμένων με απλό δεσμό, υπάρχει δυνατότητα απολύτως ελεύθερης περιστροφής, προκειμένου να υπάρξει συμφωνία μεταξύ των διατάξεων που βρισκόντουσαν πειραματικά και αυτών που υπολογίζονταν θεωρητικά. Από πολλά δεδομένα όμως διαπιστώθηκε ότι αυτή η δυνατότητα περιστροφής δε γινόταν ανεμπόδιστα άλλα έπρεπε να υπερπηδηθεί ένα ορισμένο μικρό ενεργειακό φράγμα, συνήθως της τάξης των 20 KJ/mol, ενώ η απαιτούμενη ενέργεια για την περιστροφή του μορίου ονομάστηκε ενέργεια περιστροφής. Επομένως οι διάφορες επιμέρους μορφές-διατάξεις, θα έχουν διαφορετική εσωτερική ενέργεια. Επειδή όμως η κινητική ενέργεια των μορίων λόγω θερμικής κίνησης είναι πολύ μεγαλύτερη από την ενέργεια περιστροφής, αυτές οι διατάξεις δεν είναι κατά κανόνα απομονώσιμες στη συνηθισμένη θερμοκρασία[3]. Εφόσον οι διαμορφώσεις δε μπορούν να απομονωθούν, δεν πρόκειται περί ισομερών. Άλλωστε, τα διαμορφομερή διαφέρουν από τα ισομερή που έχουν διαφορετική σειρά υποκαταστατών κατά το ότι τα τελευταία αλληλομετατρέπονται μόνο με διάσπαση και σχηματισμό δεσμών. Η ενέργεια που χρειάζεται για τέτοιες μετατροπές είναι της τάξης των 200 έως 250 KJ/mol και είναι αρκετά μεγάλη για να επιτρέψει την απομόνωση των ισομερών. Η ενέργεια αυτή είναι πολύ μεγαλύτερη από την ενέργεια που απαιτείται για την αλληλομετατροπή των διαμορφομερών[4].
Οι διαφορετικές διαμορφώσεις που αντιστοιχούν στα ενεργειακά ελάχιστα ονομάζονται διαμορφομερή[5] (ή και διαμορφωμερή)[2] ή στροφομερή[Σημ. 2]. Ο όρος "στροφομερή" χρησιμοποιείται ακριβώς για να υποδηλώσει διαμορφομερή που προκύπτουν με περιστροφή γύρω από έναν μόνο απλό δεσμό π.χ. τα στροφομερή του βουτανίου εκ περιστροφής περί τον μεσαίο δεσμό μεταξύ των ανθράκων C2-C3. Ο όρος "διαμορφομερή" χρησιμοποιείται πολλές φορές και για να υποδηλώσει το σύνολο των επιμέρους διατάξεων[3].
Πρέπει να τονιστεί ότι τα στερεοϊσομερή είναι συστήματα με ορισμένη διάταξη των υποκαταστατών στο χώρο, η οποία καλείται απεικόνιση (configuration). Αντίθετα, τα διαμορφομερή αντιστοιχούν σε μια ορισμένη στερεοχημική διάταξη και σ' αυτά δεν αλλάζει η σχετική θέση των υποκαταστατών[3].
Ο όρος "διαμόρφωση" καθιερώθηκε και ο αντίστοιχος κλάδος αναπτύχθηκε κυρίως με τις πρωτοποριακές εργασίες των θεωρητικών χημικών Κένεθ Πίτζερ (Kenneth Sanborn Pitzer), Βλαντιμίρ Πρέλογκ (Vladimir Prelog) και Ντέρεκ Μπάρτον (Derek Barton)[Σημ. 3] από τη δεκαετία του 1930 και μετά αν και αναφορές σε διαμορφομερή είχαν γίνει ήδη από τα τέλη του 19ου αιώνα[6].
Για την εποπτική αναπαράσταση των διαμορφομερών χρησιμοποιούνται τα διαφόρων ειδών μοριακά μοντέλα τα οποία χειρίζεται ο ενδιαφερόμενος ως φυσικά αντικείμενα. Ο χειρισμός "ιδεατών" μοντέλων με την χρήση κατάλληλου λογισμικού οπτικοποίησης είναι επίσης πολύ χρήσιμος για την κατανόηση των διαμορφωτικών κινήσεων των μορίων.
Σταθερότητα των διαμορφομερών - Αλληλομετατροπή[Επεξεργασία | επεξεργασία κώδικα]
Επειδή ως διαμορφομερή εννοούνται εκείνες οι διαμορφώσεις οι οποίες αντιστοιχούν σε ενεργειακά ελάχιστα, η κινητική σταθερότητα ενός διαμορφομερούς εξαρτάται (σε μια δεδομένη θερμοκρασία) από το ύψος των δύο φραγμάτων δυναμικού που το περιβάλουν και κάνουν δυνατή την ύπαρξή του. Στις περισσότερες περιπτώσεις τα φράγματα αυτά (torsional barriers) έχουν ύψος που κυμαίνεται μεταξύ ελάχιστου και έως 45-50 kJ/mol. Η αντίστοιχη ενέργεια ενεργοποίησης Ε# που απαιτείται για την υπερπήδησή τους είναι προσιτή στη συνήθη θερμοκρασία μέσω της θερμικής κίνησης των μορίων, και συνεπώς τα διαμορφομερή που ορίζονται από αυτά τα φράγματα αλληλομετατρέπονται ταχύτατα ήδη σε θερμοκρασία δωματίου και συνεπώς βρίσκονται σε κατάσταση θερμοδυναμικής ισορροπίας.

Τα δύο ανάκλιντρα του κυκλοεξανίου που χωρίζονται από φράγμα δυναμικού ύψους περίπου 46 kJ/mol αλληλομετατρέπονται 106φορές κάθε δευτερόλεπτο. Σε προοδευτικά χαμηλότερη θερμοκρασία η ταχύτητα αλληλομετατροπής των διαμορφομερών μειώνεται επίσης προοδευτικά και σε αρκετά χαμηλή θερμοκρασία η ισορροπία "παγώνει" και το κάθε διαμορφομερές διατηρεί την δομή του για σχετικά μεγάλο χρονικό διάστημα.
Από διάλυμα κυκλοεξυλοχλωρίδιου, για παράδειγμα, σε πολύ χαμηλή θερμοκρασία (–100°C ) αποβάλλεται σε κρυσταλλική μορφή το ισημερινό διαμορφομερές ενώ το αξονικό παραμένει εν διαλύσει. Τα δύο διαχωρισμένα διαμορφομερή όταν αφεθούν να επανέλθουν σε υψηλότερη θερμοκρασία μετατρέπονται στο ίδιο μείγμα διαμορφομερών που απαρτίζουν την ένωση που ονομάζουμε κυκλοεξυλοχλωρίδιο.

Αν η ενέργεια περιστροφής είναι μεγαλύτερη από περίπου 84 KJ/mol, τότε η περιστροφή θεωρείται παρεμποδισμένη (Hintered Rotation) και τα διαμορφομερή είναι απομονώσιμα στη συνήθη (20°C) θερμοκρασία[3]. Παράδειγμα αποτελούν τα ο,ο'-διυποκατεστημένα διαρύλια όπου τα φράγματα δυναμικού που χωρίζουν τα δυο διαμορφομερή είναι υψηλά και έτσι, σε κατάλληλες περιπτώσεις ογκωδών υποκαταστατών όπως π.χ. –SO3H, καθιστούν εφικτή την απομόνωση των δυο διαμορφομερών ως ανεξάρτητων ουσιών, ήδη στην συνήθη θερμοκρασία και χωρίς να υπάρχει ανάγκη για ψύξη. Η ιδιαιτερότητα αυτή των διαρυλίων είναι γνωστή ως ατροπισομέρεια δηλαδή ισομέρεια λόγω αδυναμίας στρέψης (τροπής). Ώστε, κατά την ατροπισομέρεια παρεμποδίζεται η περιστροφή σ’ έναν απλό δεσμό μιας χημικής οργανικής ένωσης, που έχει ως αποτέλεσμα να απομονωθούν οπτικά διαμορφομερή ισομερή, όπως π.χ. τα ορθοϋποκατεστημένα διφαινύλια. Το φαινόμενο αυτό εμφανίζεται, όταν η ενέργεια περιστροφής πάρει ορισμένες σε κάθε περίπτωση τιμές.
Τα δύο ατροπισομερή είναι συνήθως ένα ζεύγος εναντιομερών αλλά μπορεί να είναι και διαστερεομερή αν το μόριο περιέχει πρόσθετα χειρικά κέντρα. Πρέπει ακόμα να επισημανθεί ότι η σταθερότητα των ατροπισομερών είναι μόνο σχετική καθώς έχουν την τάση (σε διάφορους βαθμούς) να υφίστανται ρακεμίωση δηλαδή σταδιακή επάνοδο στο αρχικό μείγμα της θερμοδυναμικής ισορροπίας. Με αύξηση της θερμοκρασίας αυξάνεται και η ταχύτητα ρακεμίωσης και σε αρκετά υψηλή θερμοκρασία είναι πλέον αδύνατο να απομονωθούν ως διακριτές ουσίες.
Πληθυσμοί διαμορφομερών και δυναμικές ισορροπίες[Επεξεργασία | επεξεργασία κώδικα]
Οι πληθυσμοί των διάφορων διαμορφομερών τα οποία απαρτίζουν το μείγμα της θερμοδυναμικής ισορροπίας ακολουθούν την κατανομή Boltzmann:
όπου :
- είναι το πλήθος των διαμορφομερών.
- είναι το πλήθος όλων των διαμορφομερών.
- είναι η ενεργειακή διαφορά του διαμορφομερούς από το σταθερότερο διαμορφομερές.
- είναι η παγκόσμια σταθερά των αερίων = 8,31 J/(mol·K)
- είναι η θερμοκρασία σε βαθμούς Kelvin.
- είναι η συνάρτηση κατανομής.
Απομόνωση είτε παρατήρηση των διαμορφωτικών ισομερών[Επεξεργασία | επεξεργασία κώδικα]
Χαρακτηριστικά παραδείγματα διαμορφώσεων[Επεξεργασία | επεξεργασία κώδικα]
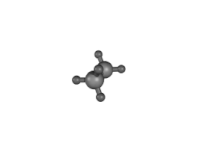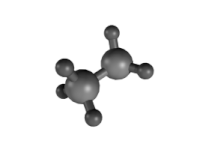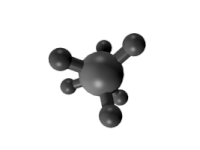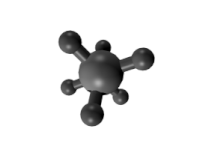


- Για τα αλκάνια αναφέρθηκε ήδη η απλή περίπτωση του βουτανίου που είναι ένα μείγμα τριών ταχύτατα αλληλομετατρεπόμενων διαμορφομερών : δύο εναντιόμορφων gauche δομών και μιας αχειρικής anti. Για τα ανώτερα μέλη της σειράς ο αριθμός των διαμορφομερών είναι κατά πολύ μεγαλύτερος.
- Από τα κυκλοαλκάνια ο εξαμελής δακτύλιος του απλού κυκλοεξανίου εμφανίζει ως μοναδικό σχεδόν διαμορφομερές το γνωστό κυκλοεξανικό ανάκλιντρο (Chair) ενώ ο στρεβλός λουτήρας (Boat)[7] είναι κατά πολύ ασταθέστερος και αντιπροσωπεύεται σε ποσοστό περίπου 0,1%.
- Ένα μονουποκατεστημένο κυκλοεξάνιο όπως π.χ. το χλωροκυκλοεξάνιο εμφανίζει δυο διαμορφομερή ανάκλιντρα , το ισημερινό και το αξονικό,τα οποία έχουν σχέση διαστερεοϊσομερών εκ διαμορφώσεως και έχουν διαφορετικό ενεργειακό περιεχόμενο.
- Ένα συμμετρικά διυποκατεστημένο κυκλοεξανικό παράγωγο όπως π.χ. το cis-1,2-διμεθυλοκυκλοεξάνιο, εμφανίζει επίσης δύο διαμορφομερή ανάκλιντρα τα οποία αλληλομετατρέπονται με αναστροφή (flip) του δακτυλίου και τα οποία έχουν σχέση εναντιομερών εκ διαμορφώσεως, έχουν το ίδιο ενεργειακό περιεχόμενο και συμμετέχουν εξ ίσου στο μείγμα της δυναμικής ισορροπίας.
- Στα διαρύλια ,όπως π.χ. στο απλό διφαινύλιο, η περιστροφή των δύο αρωματικών δακτυλίων περί τον απλό δεσμό που τους συνδέει παρεμποδίζεται από τους ορθο-υποκαταστάτες οι οποίοι στην επίπεδη διάταξη των δακτυλίων έρχονται σε στενή επαφή μεταξύ τους (ανά δύο). Η διάταξη αυτή αντιστοιχεί σε ένα ενεργειακό μέγιστο ενώ το ενεργειακό ελάχιστο επιτυγχάνεται όταν οι δακτύλιοι βρίσκονται υπό γωνία (απλουστευτικά δεχόμαστε την ορθή γωνία χωρίς όμως αυτό να είναι απολύτως ακριβές). Έτσι τα δύο ορθογωνικά διαμορφομερή του διφαινυλίου είναι ταυτιζόμενες δομές.
Σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Σπάνια αναφέρεται και ο όρος διαμορφωτική ισομέρεια, Conformational Isomerism
- ↑ Μερικές φορές αναφέρονται και ως ισομερή λόγω διαμόρφωσης ή και ισομερή εκ περιστροφής
- ↑ Kenneth Sanborn Pitzer (1914 – 1997). Αμερικανός φυσικός και θεωρητικός χημικός. Vladimir Prelog (1906 – 1998). Κροάτης χημικός, βραβείο Nobel Χημείας 1975. Sir Derek Harold Richard Barton (1918 – 1998). Βρετανός οργανικός χημικός, βραβείο Nobel Χημείας 1969
Αναφορές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «IUPAC Gold Book. Conformation». Αρχειοθετήθηκε από το πρωτότυπο στις 21 Δεκεμβρίου 2010. Ανακτήθηκε στις 22 Ιουλίου 2010.
- ↑ 2,0 2,1 Robert T. Morrison, Robert N. Boyd (1992). Organic Chemistry (6η έκδοση). Prentice Hall. ISBN 0136436692.
- ↑ 3,0 3,1 3,2 3,3 Αλεξάνδρου Νικόλαος Ε. (1995). Γενική οργανική χημεία. Δομή, φάσματα, μηχανισμοί. Τόμος 1. Ζήτη. ISBN 960-431-178-6.
- ↑ Meislich H.· Nechamkin H.· Sharefkin J. (1983). Οργανική Χημεία. Μτφρ. Α. Βάρβογλης. McGraw-Hill, New York, ΕΣΠΙ, Αθήνα. ISBN 0-07-041457-2.
- ↑ IUPAC Gold Book. conformer
- ↑ H. Sachse, Chem. Ber, 1890, 23, 1363; Z. Physik. Chem, 1892, 10, 203; Z. Physik. Chem., 1893, 11, 185-219.
- ↑ IUPAC Gold Book. chair, boat, twist
Επιλεγμένη βιβλιογραφία[Επεξεργασία | επεξεργασία κώδικα]
- McMurry John (2005). Οργανική χημεία. Πανεπιστημιακές Εκδόσεις Κρήτης. ISBN 978-960-524-055-4.
- Morrison R. T., Boyd R. N (Μετάφραση:Σακαρέλλος-Πηλίδης-Γεροθανάσης) (1991). Οργανική χημεία. Πανεπιστήμιο Ιωαννίνων. ISBN 0-13-643669-2.
- Meislich H.· Nechamkin H.· Sharefkin J. (1983). Οργανική Χημεία. Μτφρ. Αναστάσιος Βάρβογλης. McGraw-Hill, New York, ΕΣΠΙ, Αθήνα. ISBN 0-07-041457-2.










