Ασπαρτάμη
| Ασπαρτάμη |
|---|
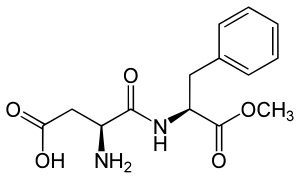 Ο χημικός τύπος της ασπαρτάμης
|
| Συστηματική ταξινόμηση |
|
|
Η ασπαρτάμη είναι ένα από τα πιο διαδεδομένα «ολιγοθερμιδικά» ή «μη θερμιδογόνα» ή «έντονης γλυκύτητας» γλυκαντικά που προστίθενται ως υποκατάστατα της ζάχαρης σε τρόφιμα και ποτά με βάση τη σχετική νομοθεσία. Στην Ευρωπαϊκή Ένωση ανήκει στα Πρόσθετα Τροφίμων, έχει Κωδικό Αριθμό Ε951 και η χρήση της ρυθμίζεται από τον Ευρωπαϊκό Κανονισμό ΕΚ 1333/2009[1].
Η ασπαρτάμη συντίθεται από δύο αμινοξέα (δομικά συστατικά των πρωτεϊνών), το ασπαρτικό οξύ και τη φαινυλαλανίνη. Αποδίδει 4 θερμίδες ανά γραμμάριο, αλλά έχει πολύ έντονη γλυκαντική δράση, οπότε προστίθεται σε πολύ μικρές ποσότητες και τελικά προσδίδει ελάχιστες θερμίδες. Εξαιτίας αυτής της ιδιότητας συχνά προτείνεται η χρήση της στη θέση της ζάχαρης στα άτομα που θέλουν να μειώσουν ή να διατηρήσουν το βάρος τους ή που έχουν σακχαρώδη διαβήτη[2][3].
Η ασφάλεια της ασπαρτάμης έχει υπάρξει αντικείμενο επιστημονικών και πολιτικών αντιπαραθέσεων, αμφισβήτησης από μέσα μαζικής ενημέρωσης και καταναλωτές, αλλά και διαδικτυακής παραπληροφόρησης (Internet hoaxes)[4][5]. Οι επιστημονικοί φορείς που αξιολόγησαν την ασφάλειά της, όπως είναι η Ευρωπαϊκή Αρχή Ασφάλειας Τροφίμων της Ε.Ε. (European Food Safety Authority, EFSA) και ο Αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων των Η.Π.Α. (Food and Drug Administration, FDA), έχουν επιβεβαιώσει ότι είναι ασφαλής για κατανάλωση από το γενικό πληθυσμό (μεταξύ των οποίων περιλαμβάνονται έγκυες και θηλάζουσες γυναίκες και παιδιά) εντός των τιμών Αποδεκτής Ημερήσιας Πρόσληψης (Acceptable Daily Intake, ADI), με την εξαίρεση των ατόμων με το κληρονομικό μεταβολικό νόσημα φαινυλκετονουρία (PKU).
Ιστορικά στοιχεία και εγκρίσεις της ασπαρτάμης[Επεξεργασία | επεξεργασία κώδικα]
Η ασπαρτάμη ανακαλύφθηκε τυχαία το 1965 από τον James Schlatter των ερευνητικών εργαστηρίων G. D. Searle ο οποίος προσπαθούσε να συνθέσει ένα τετραπεπτίδιο που θα ανέστειλε τη λειτουργία ενός πεπτικού ενζύμου. Κατά τη διάρκεια της σύνθεσης του τετραπεπτιδίου και ενώ προσπαθούσε να κρυσταλλοποιήσει ένα ενδιάμεσο προϊόν, τον ασπαρτυλφαινυλαλανίνομεθυλικό εστέρα, ένας μέρος του διαλύματος χύθηκε για λίγο στα χέρια του. Ενάντια σε κάθε πρακτική ασφάλειας, ο Schlatter έβαλε τα δάχτυλα στο στόμα του και ανακάλυψε την έντονη γλυκιά γεύση[6]. Οι Cloninger and Baldwin πρότειναν τη χρήση της ασπαρτάμης ως γλυκαντικού το 1970[7]. Ακολούθησε η αξιολόγηση της ασφάλειάς της από εθνικές και διεθνείς αρχές για την ασφάλεια των τροφίμων[8]:
- το 1980 από την Κοινή Επιτροπή για τα Πρόσθετα Τροφίμων του Παγκόσμιου Οργανισμού Υγείας και του Οργανισμού Γεωργίας (JEFCA World Health Organization & Food and Agricultural Organization),
- το 1984 από τον Οργανισμό Τροφίμων και Φαρμάκων των Η.Π.Α. (U.S. Food and Drug Administration, FDA),
- το 1985 από την Επιστημονική Επιτροπή για τα Τρόφιμα της Ευρωπαϊκής Ένωσης (Scientific Committee on Food, SCF),
- το 1992 από την Επιτροπή για την Τοξικότητα του Ηνωμένου Βασιλείου (UK Committee on Toxicity, COT) [9], κ.λπ.
Τις αρχικές εγκρίσεις για τη χρήση της ασπαρτάμης ακολούθησαν αξιολογήσεις νεότερων δεδομένων από την Επιστημονική Επιτροπή για τα Τρόφιμα της Ε.Ε. (SCF, 2002), την Ευρωπαϊκή Αρχή Ασφάλειας Τροφίμων (EFSA, 2006, 2009, 2011), και τον Οργανισμό Τροφίμων και Φαρμάκων των Η.Π.Α. (FDA, 2007), που επιβεβαίωσαν εκ νέου την ασφάλεια χρήσης της εντός των προκαθορισμένων τιμών ADI [10].
Στην Ευρωπαϊκή Ένωση, αρμόδιος φορέας για την έγκριση των γλυκαντικών είναι η Ευρωπαϊκή Επιτροπή (European Commission, EC), και η χρήση της ασπαρτάμης ρυθμίζεται από τον Ευρωπαϊκό Κανονισμό ΕΚ 1333/2008[11].
Μεταξύ άλλων, η σχετική Νομοθεσία καθορίζει τις συνθήκες χρήσης, τα κριτήρια καθαρότητας, καθώς και τη μέγιστη ποσότητα ασπαρτάμης που επιτρέπεται να προστίθεται σε κάθε κατηγορία τροφίμου και ποτού.
Ιδιότητες και χρήση[Επεξεργασία | επεξεργασία κώδικα]
Η ασπαρτάμη είναι κατά προσέγγιση 200 φορές γλυκύτερη από τη ζάχαρη. Εξαιτίας αυτής της ιδιότητας, και παρά το ότι αποδίδει 4 θερμίδες ανά γραμμάριο, χρησιμοποιείται σε πολύ μικρές ποσότητες και αποδίδει σχεδόν μηδενικές θερμίδες στα τρόφιμα και ροφήματα στα οποία χρησιμοποιείται. Η γεύση της είναι πιο κοντά στο γευστικό προφίλ της ζάχαρης σε σύγκριση με άλλα γλυκαντικά, αλλά συχνά συνδυάζεται με κάποια από αυτά, όπως το ακεσουλφαμικό κάλιο, ώστε να μοιάζει περισσότερο με τη ζάχαρη[12].
Η ασπαρτάμη χρησιμοποιείται σήμερα σε περισσότερες από 90 χώρες και σε περισσότερα από 6.000 προϊόντα, μεταξύ των οποίων τσίχλες, καραμέλες, δημητριακά, σιρόπια για καφέ, παγωτά, ανθρακούχα αναψυκτικά, ζελέ χωρίς ζάχαρη, παγωτά και άλλα επιδόρπια χωρίς ζάχαρη, υποκατάστατα γεύματος, μπάρες, μπισκότα χωρίς ζάχαρη, κ.λπ., αλλά και σε επιτραπέζια υποκατάστατα ζάχαρης και ορισμένα φάρμακα, όπως σιρόπια και καραμέλες για το βήχα. Χρησιμοποιείται κυρίως σε τρόφιμα και ροφήματα που δεν ζεσταίνονται ή ψήνονται, καθώς με τη θερμότητα χάνει μέρος της γλυκύτητάς της.
Σε μελέτη για την παγκόσμια αγορά γλυκαντικών φάνηκε ότι η κύρια αγορά της ασπαρτάμης είναι οι οικονομικά αναπτυγμένες χώρες, όπως στην Αμερική και την Ευρώπη, κυρίως λόγω του υψηλότερου κόστους της σε σχέση με τα άλλα γλυκαντικά έντονης γλυκύτητας.[13]
Περιγραφή, σύνθεση και χημικές ιδιότητες[Επεξεργασία | επεξεργασία κώδικα]
Περιγραφή και σύνθεση[Επεξεργασία | επεξεργασία κώδικα]
Η ξηρά μορφή της ασπαρτάμης έχει λευκό χρώμα, είναι άοσμη και εξαιρετικά γλυκιά για τον άνθρωπο αλλά όχι άλλα είδη. Είναι ελαφρώς διαλυτή στο νερό και την αιθανόλη και αδιάλυτη σε λίπη και έλαια. Στην ξηρά της μορφή είναι πολύ σταθερή, αλλά αποικοδομείται σε υψηλές θερμοκρασίες, και σε υδατικά διαλύματα με την πάροδο του χρόνου[14]. Η γενική περιγραφή, οι προδιαγραφές και τα κριτήρια καθαρότητας της ασπαρτάμης καθορίζεται από τη σχετική νομοθεσία τροφίμων και ποτών.[15]
Από χημικής πλευράς, η ασπαρτάμη είναι ένας μεθυλεστέρας του διπεπτιδίου που σχηματίζεται από τα φυσικά αμινοξέα L-ασπαρτικό οξύ και L-φαινυλαλανίνη[14]. Η σύνθεσή της γίνεται με σύζευξη του μεθυλεστέρα της L-φαινυλαλανίνης και του L-ασπαρτικού οξέος οπότε σχηματίζεται ο μεθυλεστέρας του διπεπτιδίου[16]. Όταν η σύνδεση γίνεται με χημικό τρόπο παράγονται δύο μορφές του διπεπτιδίου, η μορφή α που έχει γλυκιά γεύση, και η μορφή β που δεν έχει γλυκιά γεύση, τα οποία στη συνέχεια διαχωρίζονται. Με την ενζυματική διαδικασία παρασκευής της παράγεται μόνο α-ασπαρτάμη για τη λήψη της οποίας ακολουθείται περεταίρω επεξεργασία[17]. Αν και έχουν περιγραφεί πολλές μέθοδοι για την απευθείας παραγωγής α-ασπαρτάμης, μόνο λίγες προτιμούνται τελικά στη βιομηχανική παραγωγή.
Σταθερότητα της ασπαρτάμης[Επεξεργασία | επεξεργασία κώδικα]
Η ασπαρτάμη είναι πολύ σταθερή σε ξηρές συνθήκες αλλά αποικοδομείται με παρατεταμένη θέρμανση σε υδατικά διαλύματα.
Τα κύρια προϊόντα στα οποία αποικοδομείται είναι τα συστατικά από τα οποία αποτελείται ή ενδιάμεσες μορφές τους (L-ασπαρτικό οξύ, L-φαινυλαλανίνη, L-μεθυλεστέρας φαινυλαλανίνης, L- ασπαρτυλφαινυλαλανίνη κ.λπ) και το κυκλικό διπεπτίδιο δικετοπιπεραζίνη (DKP). Κανένα από αυτά τα προϊόντα δεν έχουν γλυκιά γεύση. Με την αποικοδόμηση της ασπαρτάμης χάνεται μέρος της γλυκύτητάς της, γεγονός που περιορίζει τη χρήση της σε τρόφιμα που ψήνονται ή τηγανίζονται καθώς και το χρόνο αποθήκευσης και διατήρησης των τελικών προϊόντων[14].
Ο ρυθμός αλλά και τα τελικά προϊόντα της αποικοδόμησης της ασπαρτάμης εξαρτώνται από το pH και τη θερμοκρασία[18], ενώ στα τρόφιμα εξαρτάται ακόμη από την ενεργότητα του νερού[19]. Οι Pattanaarson et al αξιολόγησαν την επίδραση του pH στην αποικοδόμηση της ασπαρτάμης σε διαλύματα με pH 2 ως pH12 και κατέληξαν ότι, σε pH 2 με 5 το κύριο προϊόν αποικοδόμησης είναι μεθυλεστέρας φαινυλαλανίνης, σε pH 7 έως 10 DKP και σε pH 12 το κύριο προϊόν αποικοδόμησης είναι α-ασπαρτυλφαινυλαλανίνη[20]. Τα αποτελέσματα αυτά ήταν σε συμφωνία με προηγούμενες μελέτες[21].
Η ποσότητα των προϊόντων της αποικοδόμησης της ασπαρτάμης που περιέχεται σε διάφορα τρόφιμα και ροφήματα που κυκλοφορούν έχει μελετηθεί και έχει βρεθεί ότι είναι εντός των αποδεκτών ορίων[22].
Μεταβολισμός της ασπαρτάμης[Επεξεργασία | επεξεργασία κώδικα]
Μετά την κατάποση, η ασπαρτάμη διασπάται στο λεπτό έντερο προς ασπαρτικό οξύ και φαινυλαλανίνη, καθώς και μικρή ποσότητα μεθανόλης, τα οποία αποτελούν κοινά συστατικά της διατροφής (Scientific Committee on Food, 2002).
Ο μεταβολισμός της ασπαρτάμης και των συστατικών στα οποία διασπάται μετά την κατάποσή της, έχει διερευνηθεί με μελέτες σε πειραματόζωα διαφορετικών ειδών και ανθρώπους, μεταξύ των οποίων υγιή άτομα, άτομα με PKU, έγκυες και θηλάζουσες γυναίκες , παιδιά κ.λπ., και με τη χορήγηση ασπαρτάμης σε διάφορες δοσολογίες, και με διάφορους τρόπους (π.χ. μεμονωμένη χορήγηση ή επαναλαμβανόμενες χορηγήσεις). Συνολικά, οι μελέτες έχουν δείξει ότι, η ασπαρτάμη διασπάται πλήρως προς φαινυλαλανίνη, ασπαρτικό οξύ και μεθανόλη, τα οποία μεταβολίζονται ταχύτατα και δεν συσωρεύονται στο αίμα. Στους ανθρώπους, ειδικότερα, η ασπαρτάμη μεταβολίζεται με τον ίδιο ακριβώς τρόπο με τον οποίο μεταβολίζεται οποιοδήποτε διπεπτίδιο της διατροφής και τα επίπεδά του ασπαρτικού οξέος και φαινυλαλανίνης που μετρώνται στο αίμα μετά την κατανάλωσή ασπαρτάμης παραμένουν εντός των φυσιολογικών μεταγευματικών επιπέδων για τα συγκεκριμένα αμινοξέα. Μία πλήρη ανασκόπηση και λεπτομερή περιγραφή των μελετών σε ανθρώπους και ζώα που διερεύνησαν τη μεταβολική τύχη των συστατικών της ασπαρτάμης έκαναν οι Magnuson et al σε μελέτη που δημοσιεύθηκε στο Critical Reviews in Toxicology το 2007[22].
Φαινυλκετονουρία[Επεξεργασία | επεξεργασία κώδικα]
Τα άτομα με φαινυλκετονουρία δεν πρέπει να καταναλώνουν ασπαρτάμη. Η φαινυλκετονουρία (PKU) είναι μια σπάνια κληρονομική κατάσταση που εμφανίζεται σε 1 στους 10.000 ανθρώπους και η οποία εντοπίζεται στη γέννηση. Ο οργανισμός των ατόμων με PKU δεν διαθέτει το ένζυμο που είναι απαραίτητο για να μετατραπεί η φαινυλαλανίνη στο αμινοξύ τυροσίνη (δομικά στοιχεία των πρωτεϊνών), με αποτέλεσμα η κατανάλωση τροφών που περιέχουν φαινυλαλανίνη να οδηγεί σε παθολογικά υψηλή συγκέντρωσή της το σώμα. Η διαχείριση της PKU απαιτεί δίαιτα με χαμηλή περιεκτικότητα σε φαινυλαλανίνη.
Για την προστασία των ατόμων με PKU, η νομοθεσία επιβάλλει σε τρόφιμα, ποτά και φαρμακευτικά προϊόντα που περιέχουν ασπαρτάμη, να φέρουν ειδική σήμανση, στην οποία θα αναγράφεται ότι το συγκεκριμένο προϊόν περιέχει πηγή φαινυλαλανίνης.
Ασπαρτάμη και σωματικό βάρος[Επεξεργασία | επεξεργασία κώδικα]
Αν και η ασπαρτάμη αποδίδει 4 θερμίδες ανά γραμμάριο, έχει εξαιρετικά έντονη γλυκύτητα οπότε χρησιμοποιείται σε πολύ μικρές ποσότητες, με αποτέλεσμα να προσθέτει σχεδόν μηδενικές θερμίδες στα τρόφιμα και ροφήματα. Σύμφωνα με μελέτες όταν τα τρόφιμα και ροφήματα με ασπαρτάμη αντικαθιστούν εκείνα που περιέχουν σάκχαρα μειώνονται οι θερμίδες που προσλαμβάνονται με τη διατροφή και αυτό μπορεί να οδηγήσει στη μείωση ή τη διατήρηση του σωματικού βάρους, με την προϋπόθεση ότι δεν αυξάνεται η κατανάλωση θερμίδων από άλλες πηγές (Blackburn et al, 1997[23], De la Hunty et al 2006[24], Bellisle και Drewnowski, 2007[25], Mattes and Popkins 2009[26]). Σύμφωνα με την Ακαδημία Διατροφής και Διαιτολογίας υπάρχουν επαρκή δεδομένα η χρήση ασπαρτάμης και των προϊόντων που την περιέχουν όταν χρησιμοποιούνται ως μέρος ενός προγράμματος για την απώλεια ή τη διατήρηση του βάρους μπορεί να σχετίζεται με μεγαλύτερη απώλεια βάρους και μπορεί να βοηθήσει τους ανθρώπους να διατηρήσουν το βάρος τους μακροπρόθεσμα[27].
Ασπαρτάμη και σακχαρώδης διαβήτης[Επεξεργασία | επεξεργασία κώδικα]
Η ασπαρτάμη δεν επηρεάζει τα επίπεδα της γλυκόζης και της ινσουλίνης στο αίμα και μπορεί να καταναλώνεται από άτομα με σακχαρώδη διαβήτη[28].
Τα τρόφιμα και ροφήματα που περιέχουν ασπαρτάμη αντί για σάκχαρα (όπως η ζάχαρη) δίνουν τη δυνατότητα στα άτομα με σακχαρώδη διαβήτη να απολαύσουν τη γλυκιά γεύση και να διατηρήσουν ευελιξία και ευχαρίστηση στο καθημερινό τους διαιτολόγιο, χωρίς το φόβο ότι θα απορρυθμιστεί η γλυκόζη στο αίμα ή ότι θα αυξηθεί το βάρος τους[29]. Τα τρόφιμα και ροφήματα που περιέχουν ασπαρτάμη μπορεί να περιέχουν άλλα συστατικά που επηρεάζουν τα επίπεδα γλυκόζης ή αποδίδουν ενέργεια και για αυτό συστείνεται να διαβάζουν οι διαβητικοί τις ετικέτες τροφίμων.
Ασπαρτάμη και τερηδόνα[Επεξεργασία | επεξεργασία κώδικα]
Η ασπαρτάμη δεν συμβάλλει στη δημιουργία οδοντικής τερηδόνας επειδή δεν αποικοδομείται από τα βακτήρια της στοματικής κοιλότητας[30].
Πρόσφατες δηλώσεις για την ασπαρτάμη[Επεξεργασία | επεξεργασία κώδικα]
Το 2012 ο American Diabetes Association και ο American Heart Association δήλωσαν ότι «τα μη θερμιδογόνα γλυκαντικά μπορούν να συμβάλλουν στη μείωση της πρόσληψης των πρόσθετων σακχάρων και να οδηγήσουν σε μειωμένη ενεργειακή πρόσληψη και κατ’ επέκταση μείωση ή διατήρηση του σωματικού βάρους - αρκεί αυτή η μείωση στην ενεργειακή πρόσληψη να μην εξισορροπηθεί με την αύξηση της πρόσληψη ενέργειας από άλλες διαιτητικές πηγές»[28]. Το ίδιο συμπέρανε η Ακαδημία Διατροφής και Διαιτολογίας (Academy of Nutrition and Dietetics)[27].
Ασπαρτάμη και παιδιά[Επεξεργασία | επεξεργασία κώδικα]
Συμφωνα με την Scientific Committee on Food της Ευρωπαϊκής Ένωσης τα παιδιά μπορούν να καταναλώνουν ασπαρτάμη εντός της τιμής Αποδεκτής Ημερήσιας Πρόσληψης (ADI). Το ADI είναι πολύ υψηλότερo από τα πραγματικά επίπεδα πρόσληψης ακόμα και στα παιδιά που καταναλώνουν μεγάλες ποσότητες ασπαρτάμης, όπως εκείνα με διαβήτη τύπου 1[9]. Η ασπαρτάμη δεν επηρεάζει τη συμπεριφορά των παιδιών, τη διάθεση, την ικανότητα μάθησης και το Σύνδρομο Ελλειματικής Προσοχής (ADD) (Επιστημονική Επιτροπή για τα Τρόφιμα, 2002) [31].
Ασπαρτάμη και εγκυμοσύνη και θηλασμός[Επεξεργασία | επεξεργασία κώδικα]
Οι γυναίκες μπορούν να καταναλώνουν ασπαρτάμη κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού, εντός της τιμής Αποδεκτής Ημερήσιας Πρόσληψης (ADI)[27].
Η ασπαρτάμη διασπάται από ένζυμα του πεπτικού σωλήνα προς τα αμινοξέα ασπαρτικό οξύ και φαινυλαλανίνη και μικρή ποσότητα μεθανόλης. Και τα τρία συστατικά απαντώνται σε πολλά τρόφιμα της καθημερινής διατροφής και μεταβολίζονται όπως ακριβώς θα συνέβαινε και στην περίπτωση που θα είχαν προέλθει από άλλες διατροφικες πηγές.
Όμως, το 2010 μια μελέτη Δανών ερευνητών πρότεινε ότι τα ολιγοθερμιδικά γλυκαντικά αυξάνουν τον κίνδυνο για πρόωρο τοκετό[32] λόγω της μεθανόλης που σχηματίζεται κατά την αποικοδόμηση της ασπαρτάμης. Η EFSA αξιολόγησε και απέρριψε τα αποτελέσματα της μελέτης και συμπέρανε ότι «δεν υπάρχουν δεδομένα που να υποστηρίζουν την αιτιολογική σχέση ανάμεσα στην κατανάλωση ολιγοθερμιδικών γλυκαντικών και τον πρόωρο τοκετό»[33].
Η Βρετανική Επιτροπή για την Τοξικότητα των Χημικών στα Τρόφιμα, τα Καταναλωτικά Προϊόντα και το Περιβάλλον (UK COT) μελέτησε την επίδραση από τη χρόνια έκθεση στη μεθανόλη. Η μεθανόλη βρίσκεται σε πολλά τρόφιμα όπως φρούτα, λαχανικά και τους χυμούς τους και παράγεται και στον πεπτικό σωλήνα από την πέψη της πηκτίνης. Έχει εκτιμηθεί ότι οι άνθρωποι παίρνουν περίπου 1000 mg μεθανόλης από φρούτα και λαχανικά. Η UK-COT δήλωσε ότι « η έκθεση στη μεθανόλη, στα επίπεδα που λαμβάνεται μέσω της διατροφής, συμπεριλαμβανομένης της ποσότητας που λαμβάνεται από τα επιτρεπόμενα επίπεδα ασπαρτάμης, δεν αναμένεται να οδηγήσει σε καμία ανεπιθύμητη ενέργεια[34].
Ασφάλεια της ασπαρτάμης[Επεξεργασία | επεξεργασία κώδικα]
Ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ FDA έχει περιγράψει την ασπαρτάμη ως ένα από τα από τα εκτενέστερα μελετημένα πρόσθετα τροφίμων που έχει εγκρίνει[35] και η Ευρωπαϊκή Αρχή Ασφάλειας Τροφίμων έχει πολλές φορές επιβεβαιώσει ότι είναι ασφαλής. Επίσης η ασπαρτάμη έχει ελεγχθεί από την Κοινή Επιτροπή για τα Πρόσθετα Τροφίμων του Παγκόσμιου Οργανισμού Υγείας και του Οργανισμού Τροφίμων και Γεωργίας. Τα άτομα με το σπάνιο γενετικό νόσημα φαινυλκετονουρία (PKU) δεν πρέπει να καταναλώνουν ασπαρτάμη.
Από το 2005 μέχρι το 2010, μια ομάδα Ιταλών ερευνητών δημοσίευσε 3 μελέτες που συνέδεσαν την ασπαρτάμη με καρκίνο σε ποντίκια[36][37][38]. Κατόπιν αιτήματος της Ευρωπαϊκής Επιτροπής η Ευρωπαϊκή Αρχή Ασφάλειας Τροφίμων αξιολόγησε τις μελέτες αυτές και κατέληξε ότι «δεν υπάρχει καμία επιστημονική τεκμηρίωση βάσει της οποίας θα πρέπει να αναθεωρηθούν οι προηγούμενες αξιολογήσεις της που κατέληξαν στο ότι η ασπαρτάμη δεν είναι καρκινογόνος ή γενοτοξική» (EFSA 2006, 2009, 2011)[39]. Ένα hoax e-mail που κυκλοφορεί εδώ και μια δεκαετία συνδέει την ασπαρτάμη με προβλήματα υγείας όπως η σκλήρυνση κατά πλάκας, ο ερυθηματώδης λύκος, η επιληψία κ.λπ.[40] αλλά οι αρχές και κυβερνητικοί οργανισμοί που σχετίζονται με αυτά τα προβλήματα υγείας κατέρριψαν τις κατηγορίες που εμφανίζονται στα Μέσα Μαζικής Ενημέρωσης και το διαδίκτυο (American Council on Science and Health[41], the UK Food Standards Agency[42] Health Canada[43]).
Αποδεκτή Ημερήσια Πρόσληψη[Επεξεργασία | επεξεργασία κώδικα]
Κατά την αξιολόγηση της ασφάλειας της ασπαρτάμης οι αρχές καθόρισαν μια τιμή Αποδεκτής Ημερήσιας Πρόσληψης (Acceptable Daily Intake) δηλαδή τη μέγιστη ποσότητα ασπαρτάμης που μπορεί να καταναλώνει ένας άνθρωπος καθημερινά και για όλη τη διάρκεια της ζωής του χωρίς κανένα κίνδυνο για την υγεία του. Η τιμή ADI για την ασπαρτάμη έχει οριστεί στα 40 mg ανά κιλό σωματικού βάρους ανά ημέρα από την SCF και την JEFCA και στα 50 mg/kg/day από τον FDA. Μελέτες πρόσληψης στην Ευρώπη και τις Η.Π.Α. έχουν δείξει ότι τα επίπεδα πρόσληψης της ασπαρτάμης είναι πολύ χαμηλότερα από τις τιμές ADI ακόμα και στις ομάδες υψηλής κατανάλωσης.
Αξιολόγηση της ασφάλειας της ασπαρτάμης μετά την έγκρισή της[Επεξεργασία | επεξεργασία κώδικα]
Μετά την έγκριση της ασπαρτάμης αρχές ασφάλειας τροφίμων, οργανισμοί υγείας και επιστημονικοί φορείς αξιολόγησαν πολλές κλινικές και εργαστηριακές μελέτες, μελέτες πρόσληψης από τον πληθυσμό και μη δημοσιευμένες αναφορές ανεπιθυμήτων ενεργειών και συμπέραναν ότι τα υπάρχοντα επιστημονικά δεδομένα δεν αποδεικνύουν ότι η ασπαρτάμη και τα μεταβολικά προϊόντα της συνδέονται με προβλήματα υγείας στον άνθρωπο [44][45][46][47].
Στις 8 Ιανουαρίου του 2013 η EFSA δημοσίευσε το προσχέδιο γνωμοδότησης για την αξιολόγηση της ασπαρτάμης, σύμφωνα με το οποίο «δεν προκύπτει ανησυχία από τοξικολογικής άποψης για τους καταναλωτές στα επίπεδα έκθεσης της ασπαρτάμης, όπως αυτά ισχύουν σήμερα»[48].
Σύμφωνα με το Δελτίο Τύπου [49] η επιστημονική ομάδα της Ευρωπαϊκής Αρχής Ασφάλειας Τροφίμων (EFSA) βασίστηκε σε όλες τις διαθέσιμες πληροφορίες σχετικά με την ασπαρτάμη και τα προϊόντα διάσπασής της, και μετά από λεπτομερή και μεθοδική ανάλυση, κατέληξε σε σχέδιο γνωμοδότησης, σύμφωνα με το οποίο δεν συντρέχει κίνδυνος τοξικότητας για τους καταναλωτές με βάση τα τρέχοντα επίπεδα έκθεσης. Η σημερινή Αποδεκτή Ημερήσια Πρόσληψη (ADI) θεωρείται ασφαλής για το γενικό πληθυσμό και η έκθεση των καταναλωτών στην ασπαρτάμη είναι κάτω από την τιμή ADI (40 mg/ kg/ day). Εξαίρεση αποτελούν όσοι υποφέρουν από το κληρονομικό νόσημα φαινυλκετονουρία, καθώς τα άτομα αυτά χρειάζονται αυστηρό περιορισμό και διατήρηση δίαιτας χαμηλής σε φαινυλαλανίνη. Παράλληλα η EFSA ανακοίνωσε την έναρξη ηλεκτρονικής δημόσιας διαβούλευσης όπου όλοι οι ενδιαφερόμενοι καλούνται να υποβάλουν τα σχόλιά τους επί του σχεδίου της επιστημονικής γνωμοδότησης έως τις 15 Φεβρουαρίου 2013.
Οι φόβοι για την ασπαρτάμη[Επεξεργασία | επεξεργασία κώδικα]
Ασπαρτάμη και καρκίνος[Επεξεργασία | επεξεργασία κώδικα]
Εργαστηριακές μελέτες σε πειραματικά μοντέλα και επιδημιολογικές και κλινικές μελέτες σε ανθρώπους έχουν διερευνήσει τη σχέση ανάμεσα στην κατανάλωση ασπαρτάμης και την εμφάνιση καρκίνου και έχουν καταλήξει ότι η ασπαρτάμη δεν προκαλεί καρκίνο στον άνθρωπο [50][51]. Το Εθνικό Ινστιτούτο για τον Καρκίνο των Η.Π.Α (US National Cancer Institute)[46], ο Οργανισμός Τροφίμων και Φαρμάκων των Η.Π.Α. (U.S. FDA) και η Eυρωπαϊκή Αρχή Ασφάλειας Τροφίμων (European Food Safety Authority, EFSA) και έχουν καταλήξει ότι η ασπαρτάμη δεν είναι καρκινογόνος για τον άνθρωπο.
Τρεις μελέτες των Soffritti et al. συνέδεσαν την κατανάλωση πολύ μεγάλων ποσοτήτων ασπαρτάμης με καρκίνο σε αρουραίους και ποντίκια[36][37][38]. Η Ευρωπαϊκή Αρχή Ασφάλειας Τροφίμων αξιολόγησε τις μελέτες αυτές, αμφισβήτησε την αξιοπιστία και την εγκυρότητά τους και κατέληξε ότι «δεν υπάρχει καμία επιστημονική τεκμηρίωση βάσει της οποίας θα πρέπει να αναθεωρηθούν οι προηγούμενες αξιολογήσεις της που κατέληξαν στο ότι η ασπαρτάμη δεν είναι καρκινογόνος ή γενοτοξική» (EFSA 2006, 2009, 2011).
Προϊόντα μεταβολισμού και αποικοδόμησης της ασπαρτάμης[Επεξεργασία | επεξεργασία κώδικα]
Οι υποθέσεις για τις ανεπιθύμητες ενέργειες της ασπαρτάμης σχετίζονται με τα προϊόντα από τη διάσπαση (φαινυλαλανίνη, ασπαρτικό οξύ, μεθανόλη) ή την αποικοδόμησή της (δικετοπιπεραζίνη DKP). Όμως τα προϊόντα από τη διάσπασή της είναι συστατικά που περιέχονται σε πολλά συνηθισμένα τρόφιμα και ότι τα προϊόντα από την αποικοδόμησή της, στις ποσότητες στις οποίες προσλαμβάνονται μέσω της κατανάλωσης ασπαρτάμης , δεν είναι επικίνδυνα για τον άνθρωπο.
Φαινυλαλανίνη[Επεξεργασία | επεξεργασία κώδικα]
Η φαινυλαλανίνη ανήκει στα απαραίτητα αμινοξέα (δομικά συστατικά των πρωτεϊνών), τα οποία δεν μπορεί να συνθέσει το ανθρώπινο σώμα και τα οποία είναι αναγκαία για τη φυσιολογική ανάπτυξη και τη διατήρηση στη ζωή. Περιέχεται σε πολλά τρόφιμα, όπως είναι το κρέας, το γάλα κ.λπ.[52]
Έχει διατυπωθεί η ανησυχία ότι η κατανάλωση ασπαρτάμης μπορεί να οδηγήσει σε αύξηση των επιπέδων φαινυλαλανίνης στο αίμα με επακόλουθη τη διατάραξη των επιπέδων των νευροδιαβιβαστών στον εγκέφαλο και την εμφάνιση νευρολογικών διαταραχών. Δεδομένα από μελέτες σε πειραματόζωα και στον άνθρωπο (τόσο σε υγιή άτομα όσο και σε άτομα με φαινυλκετονουρία) έχουν δείξει ότι μετά την κατάποση ασπαρτάμης τα επίπεδα της φαινυλαλανίνης στο αίμα αυξάνονται εντός των φυσιολογικών ορίων (SCF, 2002)[53].
Τα άτομα με το κληρονομικό μεταβολικό νόσημα φαινυλκετονουρία (PKU) έχουν μειωμένη ικανότητα να μεταβολισμού της φαινυλαλανίνης και, ειδικά οι ομοζυγώτες (άτομα που έχουν κληρονομίσει το γονίδιο και από τους δύο γονείς) συνίσταται να ακολουθούν δίαιτα ελεύθερη φαινυλαλανίνης. Με βάση την ευρωπαϊκή νομοθεσία τροφίμων όλα τα τρόφιμα και ροφήματα που περιέχουν ασπαρτάμη πρέπει να αναγράφουν «περιέχει πηγή φαινυλαλανίνης».
Ασπαρτικό οξύ[Επεξεργασία | επεξεργασία κώδικα]
Το ασπαρτικό οξύ είναι ένα από τα συνήθη αμινοξέα της τυπικής διατροφής. Μελέτες πρόσληψης έχουν δείξει ότι, τα άτομα που καταναλώνουν υψηλές ποσότητες ασπαρτάμης προσλαμβάνουν μόλις το 1 με 2% του ασπαρτικού οξέος μέσω της ασπαρτάμης και το υπόλοιπο από άλλες διαιτητικές πηγές.
Έχει διατυπωθεί η ανησυχία ότι το ασπαρτικό οξύ που προέρχεται από τη διάσπαση της ασπαρτάμης μπορεί να είναι τοξικό για τα εγκεφαλικά κύτταρα, ειδικά εάν συνδυαστεί με άλλα αμινοξέα όπως το γλουταμικό. Όμως μελέτες σε πειραματόζωα και ανθρώπους κατά τις οποίες χορηγήθηκε ασπαρτάμη σε διάφορες δοσολογίες και με διάφορους συνδυασμούς, έχουν δείξει ότι τα επίπεδα του ασπαρτικού οξέος στο αίμα μετά την κατάποση ασπαρτάμης είτε δεν επηρεάζονται, είτε επηρεάζονται αλλά παραμένοντας εντός των φυσιολογικών ορίων. Ακόμα και μεμονωμένες, καταχρηστικά υψηλές δόσολογίες ασπαρτάμης, δεν θα μπορούσαν να αυξήσουν τα επίπεδα ασπαρτικού οξέος στο αίμα στο βαθμό που να είναι τοξικά[54].
Μεθανόλη[Επεξεργασία | επεξεργασία κώδικα]
Κατά τη διάσπαση της ασπαρτάμης παράγεται μικρή ποσότητα μεθανόλης που απορροφάται ταχύτατα και μετατρέπεται σε φορμαλδεΰδη, που με τη σειρά της μετατρέπεται σε φορμικό οξύ και τελικά σε διοξείδιο του άνθρακα και νερό. Αν και έχουν εκφραστεί ανησυχίες για την επίδραση στον οργανισμό της μεθανόλης, της φορμαλδεΰδης και του φορμικού οξέος, που προέρχονται από την κατανάλωση ασπαρτάμης, μελέτες έχουν δείξει ότι το ανθρώπινο σώμα καθημερινά προσλαμβάνει και διαχειρίζεται μικρές ποσότητες από αυτά τα συστατικά. Έχει υπολογιστεί ότι ένας υγιής ενήλικας μπορεί να καταναλώσει μέχρι 2000 mg μεθανόλης την ημέρα, όταν 120ml χυμού ντομάτας περιέχουν 35 mg μεθανόλης, μία μέτρια μπανάνα 21 mg και 240ml αναψυκτικού διαίτης περιέχουν 12 mg μεθανόλης. Η φορμαλδεΰδη είναι συστατικό πολλών τροφίμων και παράγεται στο σώμα κατά την ενδογενή απομεθυλίωση πολλών συστατικών. Το ήπαρ μεταβολίζει 22 mg φορμαλδεΰδης το λεπτό προς φορμικό οξύ, διοξείδιο του άνθρακα και νερό. Σύμφωνα με υπολογισμούς, το ανθρώπινο σώμα ενός ενήλικα παράγει και μεταβολίζει περισσότερα από 50.000 mg φορμαλδεΰδης την ημέρα. Άρα είναι ξεκάθαρο ότι, η φορμαλδεΰδη που προέρχεται από τη διάσπαση της ασπαρτάμης είναι μηδαμινή σε σύγκριση με εκείνη την οποία λαμβάνει ή παράγει το ανθρώπινο σώμα καθημερινά[55].
Δικετοπιπεραζίνη (DKP)[Επεξεργασία | επεξεργασία κώδικα]
Η δικετοπιπεραζίνη (DKP) δεν είναι συστατικό της ασπαρτάμης, αλλά μία ένωση που μπορεί να προκύψει κατά την παραμονή της ασπαρτάμης, ανάλογα με το είδος του τροφίμου ή ροφήματος στο οποίο περιέχεται, το pH, τη θερμοκρασία και τη διάρκεια αποθήκευσης. Η δικετοπιπεραζίνη παράγεται κυρίως σε συνθήκες ουδέτερου και αλκαλικού pH ή σε υψηλές θερμοκρασίες. Είναι ένα σύνηθες κυκλικό διπεπτίδιο που σχηματίζεται σε πολλά πρωτεϊνούχα τρόφιμα, όπως δημητριακά, τυριά, επεξεργασμένα κρέατα, ψάρια, και ροφήματα όπως ο καφές, το κακάο, η μπύρα και το γάλα[56]. Η ασφάλεια της δικετοπιπεραζίνης (DKP) έχει αξιολογηθεί από τις επιστημονικές αρχές ασφάλειας τροφίμων όπως η Επιστημονική Επιτροπή για τα Τρόφιμα της Ε.Ε. και η Κοινή Επιτροπή για τα Πρόσθετα του Παγκόσμιου Οργανισμού Υγείας και Παγκόσμιου Οργανισμού Γεωργίας, που έχουν θέσει Αποδεκτή Ημερήσια Πρόσληψη τα 7,5 mg/kg ανά ημέρα. Σύμφωνα με μελέτες, η μέση ημερήσια πρόσληψη της DKP δεν ξεπερνά τα 0,56 mg/kg ανά ημέρα.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «ΕΦΕΤ. Νομοθεσία για τα Πρόσθετα Τροφίμων». Αρχειοθετήθηκε από το πρωτότυπο στις 27 Μαΐου 2011. Ανακτήθηκε στις 21 Νοεμβρίου 2012.
- ↑ «Academy of Nutrition and Dietetics (2012)». Αρχειοθετήθηκε από το πρωτότυπο στις 9 Σεπτεμβρίου 2012. Ανακτήθηκε στις 21 Νοεμβρίου 2012.
- ↑ Ελληνική Διαβητολογική Εταιρεία. Ολιγοθερμιδικά Γλυκαντικά: Σύμμαχος στη διατροφή ατόμων με σακχαρώδη διαβήτη. [1] Αρχειοθετήθηκε 2012-11-09 στο Wayback Machine. (pdf)
- ↑ Aspartame on Snopes.com
- ↑ «ACSH Debunks Internet Health Hoax». Αρχειοθετήθηκε από το πρωτότυπο στις 9 Μαΐου 2013. Ανακτήθηκε στις 21 Νοεμβρίου 2012.
- ↑ Mazur, R.H. (1984). Discovery of aspartame. In Aspartame: Physiology and Biochemistry (L. D. Stegink and L. J. Filer Jr., Eds.). Marcel Dekker, New York, pp. 3–9.
- ↑ Cloninger, M.R., and Baldwin, R.E. (1970). Aspartylphenylalanine methyl ester: A low-calorie sweetener. Science 170:81–82.
- ↑ European Food Safety Authority (EFSA). Topic: Aspartame
- ↑ 9,0 9,1 SCF (2002). Update on the Safety of Aspartame. [2](pdf)
- ↑ EFSA. Topic: Aspartame
- ↑ Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης. ΚΑΝΟΝΙΣΜΟΣ (ΕΚ) αριθ. 1333/2008 [3]
- ↑ O'Donnell, Kay (2006). «6 Aspartame and Neotame». Στο: Mitchell, Helen Lucy. Sweeteners and sugar alternatives in food technology. Blackwell. σελίδες 86–95. ISBN 1-4051-3434-8. Ανακτήθηκε στις 26 Ιουλίου 2011.
- ↑ Fry, J. (1999). The world market for intense sweeteners. World Review of Nutrition and Dietetics 85:211.
- ↑ 14,0 14,1 14,2 Magnuson, B. A., Burdock, G. A., Doull, J., Kroes, R. M., Marsh, G. M., Pariza, M. W., Spencer, P. S., Waddell, W. J., Walker, R. and Williams, G. M. (2007) 'Aspartame: A Safety Evaluation Based on Current Use Levels, Regulations, and Toxicological and Epidemiological Studies', Critical Reviews in Toxicology, 37:8, 629 – 727)
- ↑ [4]
- ↑ Burdock, G.A. (2005). Aspartame. In Fenaroli’s Handbook of Flavor Ingredients. 5th Edition. CRC Press, Boca Raton, FL, pp. 118–119.
- ↑ Rowe et al., 2003 Bell and Labuza, 1991; Prodolliet and Bruelhart, 1993
- ↑ Rowe, R.C., Sheskey, P.J. ,andWeller, P.J. (2003). Aspartame. In Handbook of Pharmaceutical Excipients. 4th Edition. American Pharmaceutical Association, Washington, DC, pp. 37–39.
- ↑ Bell and Labuza, 1991
- ↑ Pattanaargson, S., Chuapradit, C., and Srisukphonraruk, S. (2001). Aspartame degradation in solutions at various pH conditions. Food Chemistry and Toxicology 66:808–809. Pattanaargson, S., and Sanchavanakit, C. (2000). Aspartame degradation study using electrospray ionization mass spectrometry. Rapid Communications in Mass Spectrometry RCM 14:987–993.
- ↑ Sabah, S., and Scriba, G.K.E. (1998). Determination of aspartame and its degradation and epimerization products by capillary electrophoresis. Journal of Pharmaceutical and Biomedical Analysis 1998:1089– 1096.
- ↑ 22,0 22,1 Magnuson, B. A., Burdock, G. A., Doull, J., Kroes, R. M., Marsh, G. M., Pariza, M. W., Spencer, P. S., Waddell, W. J., Walker, R. and Williams, G. M. (2007) 'Aspartame: A Safety Evaluation Based on Current Use Levels, Regulations, and Toxicological and Epidemiological Studies', Critical Reviews in Toxicology, 37:8, 629 - 727
- ↑ Blackburn GL, Kanders BS, Lavin PT, Keller SD, Whatley J: The effect of aspartame as part of a multidisciplinary weight control program on short- and long-term control of body weight. Am J Clin Nutr 1997;65:409±418
- ↑ De La Hunty A, Gibson S, Ashwell M, (2006) A review of the effectiveness of aspartame in helping with weight control. Br Nutrition Foundation, Nutrition Bulletin 31, 115-128
- ↑ Bellisle, F & Drewnowski, A. Low-calorie sweeteners, energy intake and the control of body weight. Eur J Clin Nutr 2007;61:691–700
- ↑ Richard D. Mattes and Barry M. Popkin (2009) Nonnutritive sweetener consumption in humans: effects on appétite and food intake and their putative mechanisms. AmJ Clin Nutr 89: 1-14
- ↑ 27,0 27,1 27,2 Position of the Academy of Nutrition and Dietetics: Use of Nutritive and Nonnutritive Sweeteners. J Acad Nutr Diet. 2012;112:739-758
- ↑ 28,0 28,1 Nonnutritive Sweeteners: Current Use and Health Perspectives. A Scientific Statement From the American Heart Association and the American Diabetes Association. Circulation. 2012;126:509-519.
- ↑ Ελληνική Διαβητολογική Εταιρεία (2011) Ολιγοθερμιδικές Γλυκαντικές Ύλες. Ένας ασφαλής σύμμαχος στη διατροφή των ατόμων με σακχαρώδη διαβήτη. [5] Αρχειοθετήθηκε 2012-11-09 στο Wayback Machine.(pdf)
- ↑ [6]
- ↑ SCF (2002). Update on the Safety of Aspartame. [7] (pdf)
- ↑ Halldorsson TI et al. Intake of artificially sweetened soft drinks and risk of preterm delivery. Am J Clin Nutr doi: 10.3945/ajcn.2009.28968
- ↑ Statement of EFSA 2011
- ↑ Committee On Toxicity Of Chemicals In Food, Consumer Products And The Environment: COT STATEMENT ON EFFECTS OF CHRONIC DIETARY EXPOSURE TO METHANOL. March 2011 http://www.food.gov.uk/news-updates/news/2011/mar/methanol
- ↑ Henkel, John (November–December 1999). "Sugar Substitutes: Americans Opt for Sweetness and Lite". FDA Consumer. [8]
- ↑ 36,0 36,1 Soffritti M, Belpoggi F, Degli Esposti D, Lambertini L, Tibaldi E, Rigano A, 2006. First experimental demonstration of the multipotential carcinogenic effects of aspartame administered in the feed to Sprague-Dawley rats. Environmental Health Perspectives 114, 379-385.
- ↑ 37,0 37,1 Soffritti M, Belpoggi F, Tibaldi E, Eposti DD and Lauriola M, 2007. Life-span exposure to low doses of aspartame beginning during prenatal life increases cancer effects in rats. Env. Health Perspect. 115, 1293-1297.
- ↑ 38,0 38,1 Soffritti M, Belpoggi F, Manservigi M, Tibaldi E, Lauriola M, Falcioni L, Bua L, 2010. Aspartame administered in feed, beginning prenatally through life span, induces cancers of the liver and lung in male Swiss mice. American Journal of Industrial Medicine 53, 1197-1206.
- ↑ http://www.efsa.europa.eu/en/topics/topic/aspartame.htm?wtrl=01
- ↑ Urban Legends
- ↑ «American Council on Science and Health (1999)». Αρχειοθετήθηκε από το πρωτότυπο στις 9 Μαΐου 2013. Ανακτήθηκε στις 21 Νοεμβρίου 2012.
- ↑ the UK Food Standards Agency (2000) [9][νεκρός σύνδεσμος] (pdf)
- ↑ , Health Canada (2005)
- ↑ SCF (2002). Update on the Safety of Aspartame [10] (pdf)
- ↑ National Toxicology Program (NTP). The NTP long-term toxicology and carcinogenesis studies (bioassays) in rodents. [11]
- ↑ 46,0 46,1 National Cancer Institute. Artificial Sweeteners and Cancer
- ↑ European Food Safety Authority. Topic: Aspartame
- ↑ Σχέδιο Γνωμοδότησης διαθέσιμο [12] (pdf)
- ↑ http://www.efsa.europa.eu/en/press/news/130108.htm
- ↑ Gallus S, Scotti L, Negri E, Talamini R, Franceschi S, Montella M, Giacosa A, Dal Maso L, La Vecchia C. (2007) Artificial sweeteners and cancer risk in a network of case-control studies Annals of Oncology Volume 18, Issue 1, Pages 40-44
- ↑ Lim U, Subar AF, Mouw T, et al. Consumption of aspartame-containing beverages and incidence of hematopoietic and brain malignancies. Cancer Epidemiology, Biomarkers and Prevention 2006; 15(9):1654–1659.
- ↑ Butchko, H; Stargel, WW; Comer, CP; Mayhew, DA; Benninger, C; Blackburn, GL; De Sonneville, LM; Geha, RS et al. (2002). "Aspartame: Review of Safety". Regulatory Toxicology and Pharmacology 35 (2 Pt 2): S1–93. doi:10.1006/rtph.2002.1542. PMID 12180494.
- ↑ [13]
- ↑ Magnuson, B. A.; Burdock, G. A.; Doull, J.; Kroes, R. M.; Marsh, G. M.; Pariza, M. W.; Spencer, P. S.; Waddell, W. J. et al. (2007). "Aspartame: A Safety Evaluation Based on Current Use Levels, Regulations, and Toxicological and Epidemiological Studies". Critical Reviews in Toxicology 37 (8): 629–727. doi:10.1080/10408440701516184. PMID 17828671.
- ↑ Magnuson, B. A.; Burdock, G. A.; Doull, J.; Kroes, R. M.; Marsh, G. M.; Pariza, M. W.; Spencer, P. S.; Waddell, W. J. et al. (2007). "Aspartame: A Safety Evaluation Based on Current Use Levels, Regulations, and Toxicological and Epidemiological Studies". Critical Reviews in Toxicology 37 (8): 629–727. doi:10.1080/10408440701516184. PMID 17828671.
- ↑ Hilton et al., 1992; Gautschi and Schmid, 1997; Ginz and Engelhardt, 2000
