Νόμος του Μπόιλ
| Το λήμμα παραθέτει τις πηγές του αόριστα, χωρίς παραπομπές. |
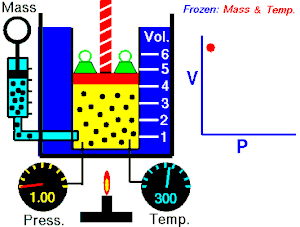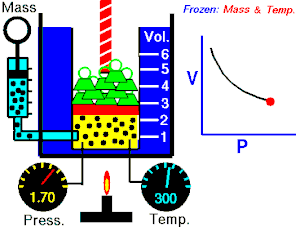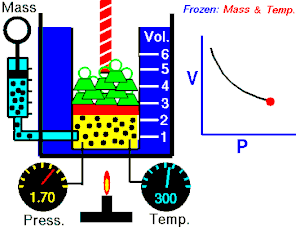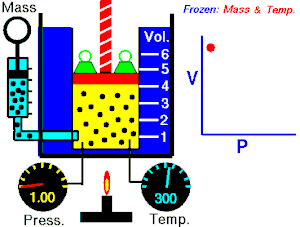
Στη θερμοδυναμική ο Νόμος του Μπόιλ είναι ένας από τους τρεις νόμους των αερίων.
Ιστορικό
[Επεξεργασία | επεξεργασία κώδικα]Ο Νόμος του Μπόιλ, γνωστός και σαν νόμος Μπόιλ-Μαριότ, πήρε το όνομά του αρχικά από τον Ιρλανδό φυσικό φιλόσοφο Ρόμπερτ Μπόιλ (Robert Boyle), (1627-1691), που πρώτος τον διατύπωσε και δημοσίευσε το 1662. Τον ίδιο νόμο διατύπωσε 14 χρόνια αργότερα και ο Γάλλος φυσικός Εντμέ Μαριότ (Edme Mariotte) (1620–1684), εξ ου και η διπλή ονομασία.
Ορισμός
[Επεξεργασία | επεξεργασία κώδικα]Σύμφωνα με αυτό το νόμο:
Για τις μεταβολές πίεσης και θερμοκρασίας αν P1 η αρχική πίεση του αερίου, V1 ο αρχικός ειδικός όγκος του και T η σταθερή θερμοκρασία του και προκληθεί μεταβολή της πίεσης και του όγκου του σε P2 και V2 κατά τρόπο που η θερμοκρασία μείνει αμετάβλητη, τότε μεταξύ των παραπάνω στοιχείων του αερίου θα ισχύει η μαθηματική σχέση:
Το γινόμενο επομένως είναι σταθερό και ισούται με
όπου ο αριθμός των γραμμομορίων τού αερίου και η παγκόσμια σταθερά των ιδανικών αερίων που στο διεθνές σύστημα μονάδων (S.I) έχει τιμή
Αυτό σημαίνει πως αν διπλασιαστεί η πίεση ενός αερίου ο όγκος του θα υποδιπλασιαστεί και αντίστροφα, φθάνει μόνο η θερμοκρασία του να παραμένει σταθερή. Σύμφωνα με τον νόμο αυτό όταν σπρώχνεται η λαβή της αεραντλίας ποδηλάτου προς τα μέσα, μειώνεται ο όγκος του αέρα με αποτέλεσμα ν΄ αυξάνεται η πίεσή του και να διοχετεύεται πλέον με πίεση στο λάστιχο του ποδηλάτου ώστε να το αναγκάζει τούτο να φουσκώνει.
Επομένως όταν η θερμοκρασία αερίου παραμένει σταθερά το γινόμενο μιας πίεσης του αερίου επί του αντίστοιχου ειδικού όγκου του είναι πάντοτε σταθερός αριθμός. Η δε μαθηματική διατύπωση αυτού είναι:
Οι παραπάνω σχέσεις ισχύουν προφανώς για 1 kg αερίου, δεδομένου ότι σ΄ αυτές υπεισέρχεται ο ειδικός όγκος του V, που παριστά τον όγκο στη μονάδα μέτρησης 1 kg αερίου. Εφαρμόζονται όμως και για περισσότερα του ενός χιλιόγραμμα με την διαφορά μόνο ότι αντί ειδικού όγκου v τοποθετείται τότε ο ολικός όγκος V του αερίου.
Αν τώρα ληφθεί υπόψη ότι ειδικός όγκος και ειδικό βάρος είναι μεγέθη αντίστροφα μεταξύ τους τότε εύκολα συνάγεται ότι η σχέση μεταξύ πιέσεων και ειδικών βαρών του αερίου θα παρίσταται από τον μαθηματικό τύπο:
Ο τελευταίος παραπάνω τύπος αποτελεί μια άλλη έκφραση του Νόμου Boyle - Mariotte κατά την οποία: υπό σταθερή θερμοκρασία τα ειδικά βάρη του αερίου είναι κατ΄ ευθεία ανάλογα προς τις αντίστοιχες πιέσεις αυτού.
Ο νόμος των Boyle και Mariotte όπως και οι άλλοι νόμοι των αερίων, ισχύει επακριβώς για ιδανικά αέρια. Οι νόμοι όμως μπορούν να εφαρμοστούν σαν καλή προσέγγιση και σε πραγματικά αέρια.









