Υδροξείδιο του βαρίου

| |

| |
| Αναγνωριστικά | |
|---|---|
| 17194-00-2 22326-55-2 Μονοένυδρο 12230-71-6 Οκταένυδρο | |
| ChEBI | CHEBI:32592 |
| ChemSpider | 26408 |
| 846955 | |
InChI=1S/Ba.2H2O/h;2*1H2/q+2;;/p-2 Key: RQPZNWPYLFFXCP-UHFFFAOYSA-L InChI=1/Ba.2H2O/h;2*1H2/q+2;;/p-2 Key: RQPZNWPYLFFXCP-NUQVWONBAR | |
| Jmol 3Δ Πρότυπο | Image |
| PubChem | 28387 |
| Αριθμός RTECS | CQ9200000 |
[Ba+2].[OH-].[OH-] | |
| Ιδιότητες | |
| Ba(OH)2 | |
| Μοριακή μάζα | 171,34 g/mol (άνυδρο) 189,355 g/mol (μονοένυδρο) 315,46 g/mol (οκταένυδρο) |
| Εμφάνιση | Λευκό στερεό |
| Πυκνότητα | 3,743 g/cm3 (μονοένυδρο) 2,18 g/cm3 (οκταένυδρο, 16 °C) |
| Σημείο τήξης | 78 °C (172 °F; 351 K) (οκταένυδρο) 300 °C (μονοένυδρο) 407 °C (άνυδρο) |
| Σημείο βρασμού | 780 °C (1,440 °F; 1,050 K) |
| Διαλυτότητα στο νερό | μάζα του BaO (όχι του Ba(OH)2): 1,67 g/100 mL (0 °C) 3,89 g/100 mL (20 °C) 4,68 g/100 mL (25 °C) 5,59 g/100 mL (30 °C) 8,22 g/100 mL (40 °C) 11,7 g/100 mL (50 °C) 20,94 g/100 mL (60 °C) 101,4 g/100 mL (100 °C) |
| Βασικότητα (pKb) | -2,02 |
Δείκτης διάθλασης (nD)
|
1,50 (οκταένυδρο) |
| Δομή | |
| Οκταεδρική | |
| Θερμοχημεία | |
Πρότυπη ενθαλπία
σχηματισμού (ΔfH |
−944,7 kJ/mol |
| Κίνδυνοι | |
Ταξινόμηση EΕ (DSD)
|
Επιβλαβές (Xn) |
| Φράσεις-R | R20/22 |
| Φράσεις-S | S2, S28 |
| NFPA 704 | |
| Σημείο ανάφλεξης | Μη αναφλέξιμο |
| Σχετικές ενώσεις | |
Άλλα Ανιόντα
|
Οξείδιο του βαρίου Υπεροξείδιο του βαρίου |
Άλλα Κατιόντα
|
Υδροξείδιο του ασβεστίου Υδροξείδιο του στροντίου |
Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες (25°C, 100 kPa). | |
| | |
| Infobox references | |
Το υδροξείδιο του βαρίου είναι μια χημική ένωση με τον χημικό τύπο Ba(OH)2 και σε ένυδρες μορφές Ba(OH)2(H2O)x.
Παρασκευή και δομή[Επεξεργασία | επεξεργασία κώδικα]
Το υδροξείδιο του βαρίου μπορεί να παρασκευαστεί διαλύοντας το οξείδιο του βαρίου (BaO) στο νερό:
- BaO + 9 H2O → Ba(OH)2·8H2O
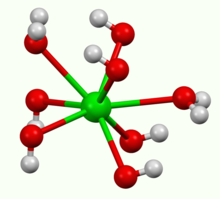
Κρυσταλλώνεται ως οκταένυδρο, που μετατρέπεται σε μονοένυδρο με θέρμανση στον αέρα. Στους 100 °C στο κενό, το μονοένυδρο δίνει υδροξείδιο του βαρίου δίνει BaO.[1] Το μονοένυδρο ακολουθεί μια στρωματική δομή (δείτε την παραπάνω εικόνα). Τα κέντρα του Ba2+ ακολουθούν μια τετραγωνική αντιπρισματική γεωμετρία. Κάθε κέντρο Ba2+ συνδέεται με δύο προσδέτες νερού και έξι προσδέτες υδροξειδίου, που γεφυρώνονται αντίστοιχα με διπλό και τριπλό δεσμό με τις γειτονικές θέσεις κέντρων του Ba2+.[2] Στο οκταένυδρο, τα μεμονωμένα κέντρα του Ba2+ έχουν πάλι οκτώ υποκαταστάτες, αλλά δεν μοιράζονται τους προσδέτες.[3]
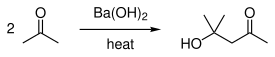
Χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Βιομηχανικά, το υδροξείδιο του βαρίου χρησιμοποιείται ως πρόδρομη ένωση για άλλες ενώσεις του βαρίου. Η μονοένυδρη ένωση χρησιμοποιείται για να αφυδατώσει και να αφαιρέσει θειικά από διάφορα προϊόντα.[4] Αυτή η εφαρμογή εκμεταλλεύεται την πολύ χαμηλή διαλυτότητα του θειικού βαρίου. Αυτή η βιομηχανική εφαρμογή έχει επίσης και εργαστηριακές χρήσεις.
Εργαστηριακές χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Το υδροξείδιο του βαρίου χρησιμοποιείται στην αναλυτική χημεία για την τιτλοδότηση των ασθενών οξέων, ιδιαίτερα των οργανικών οξέων. Το καθαρό υδατικό του διάλυμα εγγυάται ότι είναι ελεύθερο από ανθρακικά, αντίθετα με τα διαλύματα του υδροξειδίου του νατρίου και του υδροξειδίου του καλίου, επειδή το ανθρακικό βάριο είναι αδιάλυτο στο νερό. Αυτό επιτρέπει τη χρήση δεικτών όπως η φαινολοφθαλεΐνη ή η θυμολοφθαλεΐνη (με αλλαγές αλκαλικού χρώματος) χωρίς τον κίνδυνο σφαλμάτων τιτλοδότησης λόγω της παρουσίας ανθρακικών ιόντων, που είναι πολύ λιγότερο βασικά.[5]
Το υδροξείδιο του βαρίου χρησιμοποιείται κάποιες φορές στην οργανική σύνθεση ως ισχυρή βάση, π.χ. στην υδρόλυση των εστέρων[6] και των νιτριλίων.[7][8][9]
Το υδροξείδιο του βαρίου έχει χρησιμοποιηθεί για να υδρολύσει μία από τις δύο ισοδύναμες εστερομάδες στη ενδεκανοϊκό διμεθύλιο.[10]
Το υδροξείδιο του βαρίου χρησιμοποιείται, επίσης, στην αποκαρβοξυλίωση των αμινοξέων ελευθερώνοντας ανθρακικό βάριο στη διεργασία.[11]
Χρησιμοποιείται, επίσης, στην παρασκευή της κυκλοπεντανόνης,[12] της διακετονικής αλκοόλης[13] και της D-γκουλονικής γ-λακτόνης.[14]
Αντιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Το υδροξείδιο του βαρίου αποσυντίθεται σε οξείδιο του βαρίου όταν θερμανθεί στους 800 °C. Η αντίδραση με διοξείδιο του άνθρακα δίνει ανθρακικό βάριο. Το υδατικό του διάλυμα, όντας πολύ αλκαλικό, υφίσταται αντιδράσεις εξουδετέρωσης από οξέα. Συνεπώς, σχηματίζει θειικό βάριο και φωσφορικό βάριο με το θειικό και το φωσφορικό οξύ, αντίστοιχα. Η αντίδραση με υδρόθειο παράγει θειούχο βάριο. Η καθίζηση πολλών αδιάλυτων, ή λιγότερο διαλυτών αλάτων του βαρίου, μπορεί να δώσει αντίδραση διπλής αντικατάστασης, όταν το υδατικό διάλυμα του υδροξειδίου του βαρίου αναμειγνύεται με πολλά διαλύματα αλάτων άλλων μετάλλων. [15]
Οι αντιδράσεις του υδροξειδίου του βαρίου με άλατα αμμωνίου είναι ισχυρά ενδόθερμες. Η αντίδραση του οκταένυδρου υδροξειδίου του βαρίου με χλωριούχο αμμώνιο[16][17] ή[18] θειοκυανικό αμμώνιο[18][19] χρησιμοποιείται συχνά ως μια χημική επίδειξη στην τάξη, που παράγει θερμοκρασίες αρκετά χαμηλές για να παγώσει το νερό και αρκετό νερό για να διαλύσει το τελικό μείγμα.
Ασφάλεια[Επεξεργασία | επεξεργασία κώδικα]
Το υδροξείδιο του βαρίου παρουσιάζει τους ίδιους κινδύνους όπως οι άλλες ισχυρές βάσεις και όπως οι άλλες υδατοδιαλυτές ενώσεις του βαρίου: είναι διαβρωτικό και τοξικό.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ (1960). Gmelins Handbuch der anorganischen Chemie (8. Aufl.), Weinheim: Verlag Chemie, p. 289.
- ↑ Kuske, P.; Engelen, B.; Henning, J.; Lutz, H.D.; Fuess, H.; Gregson, D. "Neutron diffraction study of Sr(OH)2(H2O) and beta-Ba(OH)2*(H2O)" Zeitschrift für Kristallographie (1979-2010) 1988, vol. 183, p319-p325.
- ↑ Manohar, H.; Ramaseshan, S. "The crystal structure of barium hydroxide octahydrate Ba (OH)2(H2O)8" Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie 1964. vol. 119, p357-p374
- ↑ Robert Kresse, Ulrich Baudis, Paul Jäger, H. Hermann Riechers, Heinz Wagner, Jochen Winkler, Hans Uwe Wolf, "Barium and Barium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2007 Wiley-VCH, Weinheim. doi:10.1002/14356007.a03_325.pub2
- ↑ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000), Vogel's Quantitative Chemical Analysis (6th έκδοση), New York: Prentice Hall, ISBN 0-582-22628-7
- ↑ Meyer, K.; Bloch, H. S. (1945). "Naphthoresorcinol". Org. Synth. 25: 73; Coll. Vol. 3: 637.
- ↑ Brown, G. B. (1946). "Methylsuccinic acid". Org. Synth. 26: 54; Coll. Vol. 3: 615.
- ↑ Ford, Jared H. (1947). "β-Alanine". Org. Synth. 27: 1; Coll. Vol. 3: 34.
- ↑ Anslow, W. K.; King, H.; Orten, J. M.; Hill, R. M. (1925). "Glycine". Org. Synth. 4: 31; Coll. Vol. 1: 298.
- ↑ Durham, L. J.; McLeod, D. J.; Cason, J. (1958). "Methyl hydrogen hendecanedioate". Org. Synth. 38:55; Coll. Vol. 4:635.
- ↑ [1]
- ↑ Thorpe, J. F.; Kon, G. A. R. (1925). "Cyclopentanone". Org. Synth. 5: 37; Coll. Vol. 1: 192.
- ↑ Conant, J. B.; Tuttle, Niel. (1921). "Diacetone alcohol". Org. Synth. 1: 45; Coll. Vol. 1: 199.
- ↑ Karabinos, J. V. (1956). "γ-lactone". Org. Synth. 36: 38; Coll. Vol. 4: 506.
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ «Endothermic Reactions of Hydrated Barium Hydroxide and Ammonium Chloride». UC San Diego. Ανακτήθηκε στις 2 Απριλίου 2014.
- ↑ Endothermic Solid-Solid Reactions
- ↑ 18,0 18,1 Camp, Eric. «Endothermic Reaction». Univertist of Washington. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Ιανουαρίου 2020. Ανακτήθηκε στις 2 Απριλίου 2014.
- ↑ «Endothermic solid-solid reactions» (PDF). Classic Chemistry Demonstrations. The Royal Society of Chemistry. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 7 Απριλίου 2014. Ανακτήθηκε στις 2 Απριλίου 2014.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
| |||||
| ||||||||