Οξυκωδόνη
 | |
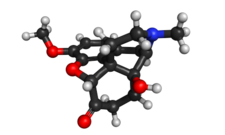 | |
| Ονομασία IUPAC | |
|---|---|
(5R,9R,13S,14S)-4,5α-Epoxy-14-hydroxy-3-methoxy-17-methylmorphinan-6-one | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | OxyContin, άλλες |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a682132 |
| Δεδομένα άδειας | |
| Κατηγορία ασφαλείας κύησης | |
| Πιθανότητα εξάρτησης | Υψηλός[1] |
| Οδοί χορήγησης | Από το στόμα, υπογλώσσια, ενδομυικά, ενδοφλέβια, ενδορρινικά, υποδόρια, διαδερμικά, διορθικά, επισκληρίδια[3] |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | Από το στόμα: 60–87%[4][5] |
| Πρωτεϊνική σύνδεση | 45%[4] |
| Μεταβολισμός | Ήπαρ: κυρίως CYP3A, και σε μικρότερο βαθμό CYP2D6 (~5%);[4] 95% μεταβολίζεται (δλδ. 5% εκκρίνεται αμετάβλητη)[6] |
| Μεταβολίτες | • Νοροξυκωδόνη (25%)[7][6] • Νοροξυμορφόνη (15%, ελεύθερη και συζευγμένη)[7][6] • Οξυμορφόνη (11%, συζευγμένη)[7][6] • Άλλοι[6] |
| Έναρξη δράση | Άμεση απελευθέρωση (ΑΑ): 10–30 λεπτά[5][6] Ελεγχόμενη απελευθέρωση (ΕΑ): 1 ώρα[8] |
| Βιολογικός χρόνος ημιζωής | Από το στόμα (ΑΑ): 2-3 ώρες[6][5] Από το στόμα (ΕΑ): 4,5 ώρες[9] |
| Διάρκεια δράσης | Από το στόμα (ΑΑ): 3-6 ώρες[6] Από το στόμα (ΕΑ): 10-12 ώρες[10] |
| Απέκκριση | Ούρα (83%)[4] |
| Κωδικοί | |
| Αριθμός CAS | 76-42-6 |
| Κωδικός ATC | N02AA05 N02AA55 N02AJ18 N02AJ19 N02AA56 N02AJ17 |
| PubChem | CID 5284603 |
| IUPHAR/BPS | 7093 |
| DrugBank | DB00497 |
| ChemSpider | 4447649 |
| UNII | CD35PMG570 |
| KEGG | D05312 |
| ChEBI | CHEBI:7852 |
| ChEMBL | CHEMBL656 |
| Συνώνυμα | Eukodal, eucodal; dihydrohydroxycodeinone, 7,8-dihydro-14-hydroxycodeinone, 6-deoxy-7,8-dihydro-14-hydroxy-3-O-methyl-6-oxomorphine[11][12][13] |
| Χημικά στοιχεία | |
| Χημικός τύπος | C18H21NO4 |
| Μοριακή μάζα | 315,37 g·mol−1 |
O=C4[C@@H]5Oc1c2c(ccc1OC)C[C@H]3N(CC[C@]25[C@@]3(O)CC4)C | |
InChI=1S/C18H21NO4/c1-19-8-7-17-14-10-3-4-12(22-2)15(14)23-16(17)11(20)5-6-18(17,21)13(19)9-10/h3-4,13,16,21H,5-9H2,1-2H3/t13-,16+,17+,18-/m1/s1 Key:BRUQQQPBMZOVGD-XFKAJCMBSA-N | |
| Φυσικά στοιχεία | |
| Σημείο τήξης | 219 °C (426 °F) |
| Υδροδιαλυτότητα | 166 mg/mL (20 °C) |
| (verify) | |
Η οξυκωδόνη, που πωλείται με την επωνυμία OxyContin (η οποία είναι η μορφή παρατεταμένης απελευθέρωσης) μεταξύ άλλων, είναι οπιοειδές φάρμακο που χρησιμοποιείται για τη θεραπεία μέτριου έως σοβαρού πόνου και κοινό φάρμακο κατάχρησης.[14][15] Συνήθως λαμβάνεται από το στόμα και διατίθεται σε σκευάσματα άμεσης απελευθέρωσης και ελεγχόμενης απελευθέρωσης.[14] Η έναρξη της ανακούφισης του πόνου αρχίζει συνήθως μέσα σε δεκαπέντε λεπτά και διαρκεί έως και έξι ώρες με τη σύνθεση άμεσης απελευθέρωσης.[14] Στο Ηνωμένο Βασίλειο, διατίθεται με ένεση.[16] Τα προϊόντα συνδυασμού διατίθενται επίσης με παρακεταμόλη (ακεταμινοφαίνη), ιβουπροφαίνη, ναλοξόνη και ασπιρίνη.[14]
Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν ευφορία, δυσκοιλιότητα, ναυτία, έμετο, απώλεια όρεξης, υπνηλία, ζάλη, κνησμό, ξηροστομία και εφίδρωση.[14] Σοβαρές ανεπιθύμητες ενέργειες μπορεί να περιλαμβάνουν εθισμό, εξάρτηση, ψευδαισθήσεις, αναπνευστική καταστολή (μείωση της αναπνοής), βραδυκαρδία και χαμηλή αρτηριακή πίεση.[14] Εκείνοι που είναι αλλεργικοί στην κωδεΐνη μπορεί επίσης να είναι αλλεργικοί στην οξυκωδόνη.[14] Η χρήση οξυκωδόνης στην αρχή της εγκυμοσύνης φαίνεται σχετικά ασφαλής.[14] Το στερητικό σύνδρομο των οπιοειδών μπορεί να συμβεί μετά από απότομη διακοπή.[14] Η οξυκωδόνη δρα ενεργοποιώντας τον μ-υποδοχέα οπιοειδών.[17] Όταν λαμβάνεται από το στόμα, έχει περίπου 1,5 φορές την επίδραση της ισοδύναμης ποσότητας μορφίνης.[18]
Η οξυκωδόνη κατασκευάστηκε για πρώτη φορά στη Γερμανία το 1916 από την θηβαΐνη.[19] Διατίθεται ως γενόσημο φάρμακο.[14] Το 2017, ήταν το 52ο πιο συχνά συνταγογραφούμενο φάρμακο στις Ηνωμένες Πολιτείες, με περισσότερες από δεκαπέντε εκατομμύρια συνταγές.[20][21] Διατίθενται διάφορα σκευάσματα αποτροπής κατάχρησης, όπως σε συνδυασμό με ναλοξόνη.[15][22]
Ιατρικές χρήσεις[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη χρησιμοποιείται για τη διαχείριση μετρίου έως σοβαρού οξέως ή χρόνιου πόνου, όταν άλλες θεραπείες δεν είναι επαρκείς.[14] Αυτό μπορεί να βελτιώσει την ποιότητα ζωής σε ορισμένους τύπους πόνου.[23] Δεν είναι σαφές αν η χρήση σε χρόνιο πόνο επιφέρει βελτίωση της ποιότητας ζωής ή συνεχή ανακούφιση από τον πόνο.
Η οξυκωδόνη διατίθεται ως δισκίο ελεγχόμενης απελευθέρωσης, το οποίο προορίζεται να λαμβάνεται κάθε 12 ώρες.[24] Μια μελέτη του Ιουλίου του 1996 ανεξάρτητη από Purdue Pharma, που παρήγαγε το φάρμακο, βρήκε ότι το σκεύασμα ελεγχόμενης απελευθέρωσης είχε μεταβλητή διάρκεια δράσης που κυμαινόταν μεταξύ 10 και 12 ωρών.[10] Μια ανασκόπηση του 2006 διαπίστωσε ότι η οξυκωδόνη ελεγχόμενης απελευθέρωσης είναι συγκρίσιμη με την οξυκωδόνη άμεσης απελευθέρωσης, τη μορφίνη και την υδρομορφόνη στη διαχείριση μέτριου έως σοβαρού πόνου του καρκίνου, με λιγότερες παρενέργειες από τη μορφίνη. Ο συγγραφέας κατέληξε στο συμπέρασμα ότι η μορφή ελεγχόμενης απελευθέρωσης είναι έγκυρη εναλλακτική λύση στη μορφίνη και θεραπεία πρώτης γραμμής για τον πόνο του καρκίνου.[24] Το 2014, η Ευρωπαϊκή Ένωση Παρηγορητικής Φροντίδας συνέστησε την από το στόμα οξυκωδόνη ως εναλλακτική λύση δεύτερης γραμμής της μορφίνης από το στόμα για τον πόνο από καρκίνο.[25]
Στις ΗΠΑ, η οξυκωδόνη παρατεταμένης αποδέσμευσης έχει εγκριθεί για χρήση σε παιδιά ηλικίας έως 11 ετών. Οι εγκεκριμένες χρήσεις είναι για την ανακούφιση από καρκίνο, πόνο τραύματος ή πόνο που οφείλεται σε σοβαρή χειρουργική επέμβαση, σε παιδιά που έχουν ήδη υποβληθεί σε θεραπεία με οπιοειδή, τα οποία μπορούν να ανεχθούν τουλάχιστον 20 mg ημερησίως οξυκωδόνης. Αυτό παρέχει μια εναλλακτική λύση στη φαιντανύλη, το μόνο άλλο αναλγητικό οπιοειδές παρατεταμένης αποδέσμευσης που έχει εγκριθεί για παιδιά.[26]
Διαθέσιμες φόρμες[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη διατίθεται σε μια ποικιλία σκευασμάτων από το στόμα ή υπογλώσσια :[5][27][28][29]
- Οξυκωδόνη άμεσης απελευθέρωσης (OxyFast, OxyIR, OxyNorm, Roxicodone)
- Οξυκωδόνη ελεγχόμενης απελευθέρωσης (OxyContin, Xtampza ER) - Διάρκεια 10-12 ωρών[10]
- Ανθεκτική στην παραβίαση της οξυκωδόνης (OxyContin OTR)[30]
- Οξυκωδόνη άμεσης αποδέσμευσης με παρακεταμόλη (ακεταμινοφαίνη) (Percocet, Endocet, Roxicet, Tylox)
- Οξυκωδόνη άμεσης απελευθέρωσης με ασπιρίνη (Endodan, Oxycodan, Percodan, Roxiprin)
- Οξυκωδόνη άμεσης απελευθέρωσης με ιβουπροφαίνη (Combunox)[31]
- Οξυκωδόνη ελεγχόμενης απελευθέρωσης με ναλοξόνη (Targin, Targiniq, Targinact)[32] - Διάρκεια 10-12 ωρών
- Οξυκωδόνη ελεγχόμενης απελευθέρωσης με ναλτρεξόνη (Troxyca) - Διάρκεια 10-12 ωρών[33]
Στις ΗΠΑ, η οξυκωδόνη εγκρίνεται μόνο για χρήση από το στόμα, διατίθεται ως δισκία και από του στόματος διαλύματα. Οι παρεντερικές συνθέσεις της οξυκωδόνης (εμπορική ονομασία OxyNorm) διατίθενται επίσης σε άλλα μέρη του κόσμου, και χρησιμοποιούνται ευρέως στην Ευρωπαϊκή Ένωση.[34][35][36] Στην Ισπανία, τις Κάτω Χώρες και το Ηνωμένο Βασίλειο, η οξυκωδόνη έχει εγκριθεί για ενδοφλέβια (IV) και ενδομυϊκή (IM) χρήση. Όταν πρωτοεμφανίστηκαν στη Γερμανία κατά τη διάρκεια του Α΄ Παγκοσμίου Πολέμου, τόσο οι χορηγήσεις οξυκοδόνης ενδοφλεβίως όσο και ενδομυικά χρησιμοποιήθηκαν συνήθως για τη μετεγχειρητική διαχείριση πόνου στους στρατιώτες των Κεντρικών Δυνάμεων.[3]
Παρενέργειες[Επεξεργασία | επεξεργασία κώδικα]

Σοβαρές παρενέργειες της οξυκωδόνης περιλαμβάνουν μειωμένη ευαισθησία στον πόνο (πέρα από τον πόνο που λαμβάνεται για να μειώσει το φάρμακο), ευφορία, αγχόλυση, αισθήματα χαλάρωσης και αναπνευστική καταστολή.[38] Συχνές ανεπιθύμητες ενέργειες της οξυκωδόνης περιλαμβάνουν δυσκοιλιότητα (23%), ναυτία (23%), έμετο (12%), υπνηλία (23%), ζάλη (13%), φαγούρα (13%), ξηροστομία (6%) και εφίδρωση (5%).[39] Οι λιγότερο συχνές ανεπιθύμητες ενέργειες (που εμφανίζονται σε λιγότερο από 5% των ασθενών) περιλαμβάνουν απώλεια όρεξης, νευρικότητα, κοιλιακό άλγος, διάρροια, κατακράτηση ούρων, δύσπνοια και λόξυγκας.[40] Οι περισσότερες ανεπιθύμητες ενέργειες γενικά γίνονται λιγότερο έντονες με την πάροδο του χρόνου, αν και ζητήματα που σχετίζονται με τη δυσκοιλιότητα είναι πιθανό να συνεχιστούν κατά τη διάρκεια της χρήσης.[41] Η οξυκωδόνη σε συνδυασμό με ναλοξόνη σε δισκία ελεγχόμενης απελευθέρωσης, έχει διαμορφωθεί τόσο για την αποτροπή της κατάχρησης όσο και για τη μείωση της δυσκοιλιότητας που προκαλείται από οπιοειδή.[42]
Εξάρτηση και στέρηση[Επεξεργασία | επεξεργασία κώδικα]
Ο κίνδυνος εμφάνισης σοβαρού στερητικού συνδρόμου είναι υψηλός, εάν ο ασθενής έχει γίνει φυσικά εξαρτημένος και διακόψει την οξυκωδόνη απότομα. Ιατρικά, όταν το φάρμακο λαμβάνεται τακτικά για μεγάλο χρονικό διάστημα, αποσύρεται σταδιακά και όχι απότομα. Τα άτομα που χρησιμοποιούν τακτικά οξυκωδόνη ψυχαγωγικά ή σε υψηλότερες από τις συνταγογραφούμενες δόσεις διατρέχουν ακόμη μεγαλύτερο κίνδυνο σοβαρών συμπτωμάτων στέρησης. Τα συμπτώματα στέρησης της οξυκωδόνης, όπως και με άλλα οπιοειδή, μπορεί να περιλαμβάνουν «άγχος, κρίση πανικού, ναυτία, αϋπνία, μυϊκό πόνο, μυϊκή αδυναμία, πυρετούς και άλλα συμπτώματα που μοιάζουν με γρίπη».[43][44]
Στερητικά συμπτώματα έχουν επίσης αναφερθεί σε νεογέννητα των οποίων οι μητέρες έλαβαν οξυκωδόνη με ένεση ή από το στόμα κατά τη διάρκεια της εγκυμοσύνης.[45]
Επίπεδα ορμονών[Επεξεργασία | επεξεργασία κώδικα]
Όπως και με άλλα οπιοειδή, η χρόνια χρήση οξυκωδόνης (ιδιαίτερα με υψηλότερες δόσεις) προκαλεί συχνά ταυτόχρονο υπογοναδισμό (χαμηλά επίπεδα ορμονών φύλου ).[46]
Υπερδοσολογία[Επεξεργασία | επεξεργασία κώδικα]
Σε υψηλές δόσεις, υπερδοσολογία ή σε ορισμένα άτομα που δεν είναι ανθεκτικά στα οπιοειδή, η οξυκωδόνη μπορεί να προκαλέσει ρηχή αναπνοή, βραδύ καρδιακό ρυθμό, κρύο / μαλακό δέρμα, παύσεις στην αναπνοή, χαμηλή αρτηριακή πίεση, μικρές οφθαλμικές κόρες, κυκλοφορική κατάρρευση, αναπνευστική ανακοπή και θάνατο.[40]
Το 2011, ήταν η κύρια αιτία θανάτων που σχετίζονται με φάρμακα στις ΗΠΑ[47] Ωστόσο, από το 2012 και μετά, η ηρωίνη και η φαιντανύλη έχουν γίνει πιο συχνές αιτίες θανάτων που σχετίζονται με τα ναρκωτικά.
Η υπερβολική δόση οξυκωδόνης έχει επίσης περιγραφεί ότι προκαλεί έμφραγμα του νωτιαίου μυελού σε υψηλές δόσεις και ισχαιμική βλάβη στον εγκέφαλο, λόγω παρατεταμένης υποξίας από την κατασταλτική αναπνοή.[48]
Αλληλεπιδράσεις[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη μεταβολίζεται από τα ένζυμα CYP3A4 και CYP2D6, και ως εκ τούτου η κάθαρσή της μπορεί να μεταβληθεί από αναστολείς και επαγωγείς αυτών των ενζύμων, αυξάνοντας και μειώνοντας τον χρόνο ημιζωής, αντίστοιχα.[35] Η φυσική γενετική διακύμανση σε αυτά τα ένζυμα μπορεί επίσης να επηρεάσει την κάθαρση της οξυκωδόνης, η οποία μπορεί να σχετίζεται με την ευρεία μεταβλητότητα μεταξύ ατόμων στην ημιζωή και την ισχύ της.
Η ριτοναβίρη ή η λοπιναβίρη / ριτοναβίρη αυξάνουν σημαντικά τις συγκεντρώσεις οξυκωδόνης στο πλάσμα σε υγιείς ανθρώπους εθελοντές λόγω της αναστολής των CYP3A4 και CYP2D6.[49] Ηριφαμπικίνη μειώνει σημαντικά τις συγκεντρώσεις της οξυκωδόνης στο πλάσμα λόγω της ισχυρής επαγωγής του CYP3A4.[50] Υπάρχει επίσης μια αναφορά περίπτωσης της φωσφαινυτοΐνης, ενός επαγωγέα του CYP3A4, να μειώνει δραματικά τις αναλγητικές επιδράσεις της οξυκωδόνης σε έναν ασθενή με χρόνιο πόνο.[51] Ενδέχεται να απαιτούνται προσαρμογές δοσολογίας ή φαρμάκων σε κάθε περίπτωση.
Φαρμακολογία[Επεξεργασία | επεξεργασία κώδικα]
Φαρμακοδυναμική[Επεξεργασία | επεξεργασία κώδικα]
| Χημική ένωση | Διαδρομή | Δόση |
|---|---|---|
| Κωδεΐνη | PO | 200 mg |
| Υδροκωδόνη | PO | 20–30 mg |
| Υδρομορφόνη | PO | 7.5 mg |
| Υδρομορφόνη | IV | 1.5 mg |
| Μορφίνη | PO | 30 mg |
| Μορφίνη | IV | 10 mg |
| Οξυκωδόνη | PO | 20 mg |
| Οξυκωδόνη | IV | 10 mg |
| Οξυμορφόνη | PO | 10 mg |
| Οξυμορφόνη | IV | 1 mg |
Η οξυκωδόνη, ένα ημι-συνθετικό οπιοειδές, είναι εξαιρετικά επιλεκτικός αγωνιστής του μ-υποδοχέα οπιοειδών (MOR).[34][35] Αυτός είναι ο κύριος βιολογικός στόχος του ενδογενούς οπιοειδούς νευροπεπτιδίου β-ενδορφίνη.[17] Η οξυκωδόνη έχει χαμηλή συγγένεια για τον δ-υποδοχέα οπιοειδών (DOR) και τον κ-υποδοχέα οπιοειδών (KOR), όπου είναι παρόμοια αγωνιστής. Αφού η οξυκωδόνη συνδέεται με το MOR, απελευθερώνεται ένα σύμπλοκο πρωτεΐνης G, το οποίο αναστέλλει την απελευθέρωση νευροδιαβιβαστών από το κύτταρο μειώνοντας την ποσότητα της cAMP που παράγεται, κλείνοντας τα κανάλια ασβεστίου και ανοίγοντας κανάλια καλίου.[55] Τα οπιοειδή όπως η οξυκωδόνη πιστεύεται ότι παράγουν τα αναλγητικά τους αποτελέσματα μέσω της ενεργοποίησης του MOR στη μεσοεγκεφαλική περιυδραγωγό φαιά ουσία (PAG) και στον ραχιαίο μεσοκοιλιακό μυελό (RVM).[56] Αντιστρόφως, πιστεύεται ότι παράγουν ανταμοιβή και εθισμό μέσω της ενεργοποίησης του MOR στην οδό μεσολιμπικής ανταμοιβής, συμπεριλαμβανομένης της κοιλιακής περιοχής του επικλινή πυρήνα και στα βασικά γάγγλια.[57][58] Η ανοχή στις αναλγητικές και ανταμείβουσες επιδράσεις των οπιοειδών είναι πολύπλοκη και συμβαίνει λόγω ανοχής σε επίπεδο υποδοχέα (π.χ. ρύθμιση προς τα κάτω των MOR), ανοχής σε επίπεδο κυττάρου (π.χ. ρύθμιση προς τα πάνω του cAMP) και ανοχής σε επίπεδο συστήματος (π.χ. νευρική προσαρμογή λόγω επαγωγής έκφρασης ΔFosB ).[59]
Λήφθηκε προφορικά, 20 mg mg οξυκωδόνης άμεσης αποδέσμευσης θεωρείται ισοδύναμο σε αναλγητικό αποτέλεσμα με 30 mg μορφίνης,[60][61] ενώ η οξυκωδόνη παρατεταμένης απελευθέρωσης θεωρείται ότι είναι δύο φορές πιο ισχυρή από τη στοματική μορφίνη.[62]
Ομοίως με τα περισσότερα άλλα οπιοειδή, η οξυκωδόνη αυξάνει την έκκριση προλακτίνης, αλλά η επίδρασή της στα επίπεδα τεστοστερόνης είναι άγνωστη.[34] Σε αντίθεση με τη μορφίνη, η οξυκωδόνη στερείται ανοσοκατασταλτικής δραστικότητας (μετριέται από τη δραστικότητα των κυττάρων φυσικών φονέων και την παραγωγή ιντερλευκίνης 2 in vitro). Η κλινική σημασία αυτού δεν έχει διευκρινιστεί.
Ενεργοί μεταβολίτες[Επεξεργασία | επεξεργασία κώδικα]
Μερικοί από τους μεταβολίτες της οξυκωδόνης έχουν επίσης βρεθεί ότι είναι δραστικοί ως αγωνιστές του MOR, μερικοί από τους οποίους έχουν συγκριτικά πολύ μεγαλύτερη συγγένεια για (καθώς και υψηλότερη αποτελεσματικότητα σε) τον MOR.[63][64][65] Η οξυμορφόνη διαθέτει 3 έως 5 φορές υψηλότερη συγγένεια για το MOR από ό, τι η οξυκωδόνη,[6] ενώ η νοροξυκωδόνη και η νοροξυμορφόνη έχουν το ένα τρίτο και 3 φορές υψηλότερη συγγένεια για το MOR, αντίστοιχα, και ενεργοποίηση MOR είναι 5 έως 10 φορές λιγότερη με νοροξυκοδόνη αλλά 2 φορές υψηλότερη με νοροξυμορφόνη σε σχέση με την οξυκωδόνη.[66] Η νοροξυκωδόνη, η νοροξυμορφόνη και η οξυμορφόνη έχουν επίσης μεγαλύτερο βιολογικό χρόνο ημιζωής από την οξυκωδόνη.[67]
Ωστόσο, παρά την μεγαλύτερη in vitro δράση ορισμένων από τους μεταβολίτες της, έχει προσδιοριστεί ότι η ίδια η οξυκωδόνη ευθύνεται για το 83,0% και το 94,8% της αναλγητικής της δράσης μετά από από του στόματος και ενδοφλέβια χορήγηση, αντίστοιχα.[64] Η οξυμορφόνη διαδραματίζει μόνο δευτερεύοντα ρόλο, που ευθύνεται για το 15,8% και 4,5% της αναλγητικής δράσης της οξυκωδόνης μετά από από του στόματος και ενδοφλέβια χορήγηση, αντίστοιχα. Αν και ο γονότυπος CYP2D6 και η οδός χορήγησης οδηγούν σε διαφορετικούς ρυθμούς σχηματισμού οξυμορφόνης, η αμετάβλητη μητρική ένωση παραμένει ο κύριος συντελεστής στη συνολική αναλγητική επίδραση της οξυκωδόνης. Σε αντίθεση με την οξυκωδόνη και την οξυμορφόνη, η νοροξυκοδόνη και η νοροξυμορφόνη, ενώ επίσης ισχυροί αγωνιστές MOR, διασχίζουν ελάχιστα το φράγμα αίματος-εγκεφάλου στο κεντρικό νευρικό σύστημα και για αυτόν τον λόγο είναι ελάχιστα αναλγητικά σε σύγκριση.[63][66][65]
Κ-υποδοχέας οπιοειδών[Επεξεργασία | επεξεργασία κώδικα]
Το 1997, μια ομάδα Αυστραλών ερευνητών πρότεινε (με βάση μια μελέτη σε αρουραίους) ότι η οξυκωδόνη δρα στους KOR, σε αντίθεση με τη μορφίνη, η οποία δρα στους MOR.[68] Περαιτέρω έρευνα από την ομάδα αυτή έδειξε το φάρμακο φαίνεται να είναι ένας υψηλής συγγένειας αγωνιστής των κ 2b υποδοχέων οπιοειδών αγωνιστή.[69] Ωστόσο, το συμπέρασμα αυτό αμφισβητήθηκε, κυρίως με βάση το ότι η οξυκωδόνη παράγει αποτελέσματα που είναι τυπικά των αγωνιστών MOR.[70] Το 2006, έρευνα από ιαπωνική ομάδα έδειξε ότι η επίδραση της οξυκωδόνης προκαλείται από διαφορετικούς υποδοχείς σε διαφορετικές καταστάσεις.[71] Συγκεκριμένα σε διαβητικούς ποντικούς, το KOR φαίνεται να εμπλέκεται στα αντι-αντιληπτικά αποτελέσματα της οξυκωδόνης, ενώ σε μη διαβητικούς ποντικούς, ο υποδοχέας μ1 - οπιοειδούς φαίνεται να είναι πρωταρχικά υπεύθυνος για αυτές τις επιδράσεις.[72]
Φαρμακοκινητική[Επεξεργασία | επεξεργασία κώδικα]
Προφίλ απορρόφησης άμεσης απελευθέρωσης[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη μπορεί να χορηγηθεί από το στόμα, ενδορινικά, μέσω ενδοφλέβιας, ενδομυϊκής ή υποδόριας ένεσης ή από το ορθό. Η βιοδιαθεσιμότητα της από του στόματος χορήγησης οξυκωδόνης κατά μέσο όρο κυμαίνεται μεταξύ 60 και 87%, με την ορθική χορήγηση να αποδίδει τα ίδια αποτελέσματα. Η ενδορινική διαφέρει μεταξύ ατόμων με μέσο όρο 46%.[73]
Μετά από μια δόση συμβατικής (άμεσης απελευθέρωσης) στοματικής οξυκωδόνης, η έναρξη της δράσης είναι σε 10 έως 30 λεπτά,[6][5] και τα μέγιστα επίπεδα πλάσματος του φαρμάκου επιτυγχάνονται εντός περίπου 30 έως 60 λεπτών.[63] σε αντίθεση, μετά από μια δόση OxyContin (μια στοματική σύνθεση ελεγχόμενης απελευθέρωσης), τα μέγιστα επίπεδα οξυκωδόνης στο πλάσμα εμφανίζονται σε περίπου τρεις ώρες.[40] Η διάρκεια της οξυκωδόνης άμεσης απελευθέρωσης είναι 3 έως 6 ώρες, αν και αυτό μπορεί να ποικίλλει ανάλογα με το άτομο.
Κατανομή[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη έχει όγκο κατανομής 2,6L / kg,[74] στο αίμα κατανέμεται σε σκελετικούς μυς, ήπαρ, εντερική οδό, πνεύμονες, σπλήνα και εγκέφαλο.[40] Τα συμβατικά στοματικά παρασκευάσματα αρχίζουν να μειώνουν τον πόνο μέσα σε 10 έως 15 λεπτά με άδειο στομάχι. Αντίθετα, το OxyContin αρχίζει να μειώνει τον πόνο μέσα σε μία ώρα.[14]
Μεταβολισμός[Επεξεργασία | επεξεργασία κώδικα]
Ο μεταβολισμός της οξυκωδόνης στους ανθρώπους λαμβάνει χώρα στο ήπαρ κυρίως μέσω του συστήματος κυτοχρώματος P450 και είναι εκτεταμένος (περίπου 95%) και πολύπλοκος, με πολλές μικρές οδούς και προκύπτοντες μεταβολίτες.[6][75] Περίπου το 10% (εύρος 8-14%) μιας δόσης οξυκωδόνης απεκκρίνεται ουσιαστικά αμετάβλητο (μη συζευγμένο ή συζευγμένο ) στα ούρα. Οι κύριοι μεταβολίτες της οξυκωδόνης είναι η νοροξυκοδόνη (70%), η νοροξυμορφόνη ("σχετικά υψηλές συγκεντρώσεις"),[38] και η οξυμορφόνη (5%).[63][66] Ο άμεσος μεταβολισμός της οξυκωδόνης στον άνθρωπο έχει ως εξής:[9][76]
- Ν- απομεθυλίωση σε νοροξυκωδόνη κυρίως μέσω του CYP3A4
- Ο-απομεθυλίωση σε οξυμορφόνη κυρίως μέσω του CYP2D6
- 6- Ketoreduction σε 6α- και 6β-οξυκωδόλη
- Ν- Οξείδωση σε οξυκωδόνη-Ν-οξείδιο
Στους ανθρώπους, η Ν-απομεθυλίωση της οξυκωδόνης προς τη νοροξυκοδόνη από το CYP3A4 είναι η κύρια μεταβολική οδός, που αντιπροσωπεύει το 45% ± 21% μιας δόσης οξυκωδόνης, ενώ η Ο-απομεθυλίωση της οξυκωδόνης σε οξυμορφόνη από το CYP2D6 και η 6-κετοαναγωγή της οξυκωδόνης σε 6-οξυκωδόλες αντιπροσωπεύουν σχετικά ελάσσονες μεταβολικές οδούς, που αντιπροσωπεύουν 11% ± 6% και 8% ± 6% μιας δόσης οξυκωδόνης, αντίστοιχα.[6][34]
Αρκετοί από τους άμεσους μεταβολίτες της οξυκωδόνης στη συνέχεια συζεύονται με γλυκουρονικό οξύ και απεκκρίνονται στα ούρα.[6] Η 6α-οξυκωδόλη και η 6β-οξυκωδόλη μεταβολίζονται περαιτέρω με Ν-απομεθυλίωση σε νορ-6α-οξυκωδόλη και νορ-6β-οξυκωδόλη, αντίστοιχα, και με Ν-οξείδωση σε 6α-οξυκωδόλη-Ν-οξείδιο και 6β-οξυκωδόλη- Ν-οξείδιο (το οποίο μπορεί στη συνέχεια να γλυκουρονιωστεί επίσης).[9] Η οξυμορφόνη μεταβολίζεται περαιτέρω, ως εξής:[76]
- 3-Γλουκουρονιδίωση σε οξυμορφόνη-3-γλυκουρονίδιο κυρίως μέσω UGT2B7
- 6-κετοαναγωγή σε 6α-οξυμορφόλη και 6β-οξυμορφόλη
- Ν- Απομεθυλίωση σε νοροξυμορφόνη
Η πρώτη πορεία των τριών παραπάνω αντιστοιχεί στο 40% του μεταβολισμού της οξυμορφόνης, καθιστώντας την οξυμορφόνη-3-γλυκουρονίδιο τον κύριο μεταβολίτη της οξυμορφόνης, ενώ οι δύο τελευταίες οδοί αντιπροσωπεύουν λιγότερο από το 10% του μεταβολισμού της οξυμορφόνης.[76] Μετά την Ν-απομεθυλίωση της οξυμορφόνης, η νοροξυμορφόνη περαιτέρω γλυκουρονιδώνεται σε νοροξυμορφόνη-3-γλυκουρονίδη.
Επειδή η οξυκωδόνη μεταβολίζεται από το σύστημα κυτοχρώματος P450 στο ήπαρ, η φαρμακοκινητική της μπορεί να επηρεαστεί από γενετικούς πολυμορφισμούς και αλληλεπιδράσεις φαρμάκων που αφορούν αυτό το σύστημα, καθώς και από τη λειτουργία του ήπατος.[40] Μερικοί άνθρωποι είναι γρήγοροι μεταβολιστές της οξυκωδόνης, με αποτέλεσμα μειωμένες επιδράσεις, ενώ άλλοι είναι αργοί μεταβολιστές, με αποτέλεσμα αυξημένες επιδράσεις και τοξικότητα.[77][78] Ενώ η υψηλότερη δραστικότητα του CYP2D6 αυξάνει τις επιδράσεις της οξυκωδόνης (λόγω της αυξημένης μετατροπής σε οξυμορφόνη), η υψηλότερη δραστικότητα του CYP3A4 έχει το αντίθετο αποτέλεσμα και μειώνει τις επιδράσεις της οξυκωδόνης (λόγω του αυξημένου μεταβολισμού σε νοροξυκοδόνη και νοροξυμορφόνη).[79] Η δόση της οξυκωδόνης πρέπει να μειωθεί σε ασθενείς με μειωμένη ηπατική λειτουργία.[80]
Κάθαρση[Επεξεργασία | επεξεργασία κώδικα]
Η κάθαρση της οξυκωδόνης είναι 0,8 λίτρα/λεπτό.[81] Η οξυκωδόνη και οι μεταβολίτες της απεκκρίνονται κυρίως στα ούρα.[82] Επομένως, η οξυκωδόνη συσσωρεύεται σε ασθενείς με νεφρική δυσλειτουργία.[80] Η οξυκωδόνη αποβάλλεται στα ούρα 10% ως αμετάβλητη οξυκωδόνη, 45% ± 21% ως Ν -απομεθυλιωμένοι μεταβολίτες (νοροξυκοδόνη, νοροξυμορφόνη, νοροξυκοδόλες), 11 ± 6% ως Ο -απομεθυλιωμένοι μεταβολίτες (οξυμορφόνη, οξυμορφόλες) και 8% ± 6 % ως 6-κετο-μειωμένοι μεταβολίτες (οξυκωδόλες).[63]
Διάρκεια δράσης[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη έχει χρόνο ημιζωής 4,5 ώρες.[74] Διατίθεται ως γενόσημο φάρμακο.[14] Ο κατασκευαστής της Purdue Pharma ισχυρίστηκε στην αίτηση ευρεσιτεχνίας του 1992 ότι η διάρκεια δράσης του OxyContin, του παρασκευάσματος ελεγχόμενης αποδέσμευσης της οξυκωδόνης, είναι 12 ώρες στο "90% των ασθενών". Δεν έχει πραγματοποιήσει ποτέ κλινικές μελέτες στις οποίες χορηγήθηκε OxyContin σε συχνότερα διαστήματα. Σε ξεχωριστή αρχειοθέτηση, ο Purdue ισχυρίζεται ότι η οξυκωδόνη ελεγχόμενης απελευθέρωσης "παρέχει ανακούφιση από τον πόνο στον εν λόγω ασθενή για τουλάχιστον 12 ώρες μετά τη χορήγηση."[83] Ωστόσο, το 2016 μια έρευνα από τους Los Angeles Times διαπίστωσε ότι «το φάρμακο εξαντλείται ώρες νωρίς σε πολλούς ανθρώπους», προκαλώντας συμπτώματα απόσυρσης οπιούχων και έντονης επιθυμίας για το OxyContin. Ένας γιατρός, ο Λόρενς Ρόμπινς είπε στους δημοσιογράφους ότι πάνω από το 70% των ασθενών του θα ανέφεραν ότι το OxyContin θα παρείχε μόνο 4-7 ώρες ανακούφισης. Οι γιατροί τη δεκαετία του 1990 συχνά άλλαζαν τους ασθενείς τους σε ένα δοσολογικό σχήμα μία φορά κάθε οκτώ ώρες, όταν διαμαρτύρονταν ότι η διάρκεια δράσης για το OxyContin ήταν πολύ μικρή για να ληφθεί μόνο δύο φορές την ημέρα.[84]
Ο Purdue αποθάρρυνε έντονα την πρακτική: Ο ιατρικός διευθυντής της Purdue Ρόμπερτ Ρέντερ έγραψε σε έναν γιατρό το 1995 ότι "Το OxyContin έχει αναπτυχθεί για δόση [12 ωρών]... Ζητώ να μην χρησιμοποιήσετε ένα [8-ωρο] δοσολογικό σχήμα. " Η Purdue δημοσίευσε επανειλημμένα σημειώματα στους αντιπροσώπους πωλήσεών της, ζητώντας τους να υπενθυμίσουν στους γιατρούς να μην παρεκκλίνουν από το πρόγραμμα δόσεων 12 ωρών. Ένα τέτοιο σημείωμα έγραφε, "Δεν υπάρχει δοσολογία Q8 με το OxyContin... [8-ωρη δόση] πρέπει να αφαιρεθεί. ΤΩΡΑ!!"[83] Οι δημοσιογράφοι που κάλυψαν την έρευνα υποστηρίζουν ότι η Purdue Pharma επέμεινε σε 12 ώρες διάρκειας δράσης για όλους σχεδόν τους ασθενείς, παρά τα αποδεικτικά στοιχεία για το αντίθετο, προκειμένου να προστατευθεί η φήμη του OxyContin ως φάρμακο 12 ωρών και η προθυμία των εταιρειών ιατρικών ασφαλίσεων και διαχειριζόμενης φροντίδας για την κάλυψη του OxyContin παρά το υψηλό κόστος σε σχέση με τα γενόσημα οπιοειδή όπως η μορφίνη.
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Ο Μάρτιν Φρόιντ και ο Έντμουντ Σπέγιερ του Πανεπιστημίου της Φραγκφούρτης στη Γερμανία συνέθεσαν για πρώτη φορά την οξυκωδόνη από τη θηβαΐνη το 1916.[85][19] Όταν ο Φρόιντ πέθανε το 1920, ο Σπέγερ έγραψε τον επικήδειό του.[86] Ο Σπέγερ, γόνος Εβραϊκής οικογένειας της Φραγκφούρτης το 1878, ήταν θύμα του Ολοκαυτώματος. Πέθανε τις 5 Μαΐου 1942, την δεύτερη ημέρα της εκκένωσης του Γκέτο του Λοτζ και ο θάνατός του σημειώθηκε στο χρονικό του γκέτο.[87]
Η πρώτη κλινική χρήση του φαρμάκου τεκμηριώθηκε το 1917, ένα χρόνο μετά την ανάπτυξή του.[19][10] Εισήχθη για πρώτη φορά στην αγορά των ΗΠΑ τον Μάιο του 1939. Στις αρχές του 1928, η Merck εισήγαγε ένα προϊόν συνδυασμού που περιείχε σκοπολαμίνη, οξυκωδόνη και εφεδρίνη με τα γερμανικά αρχικά για τα συστατικά SEE, το οποίο αργότερα μετονομάστηκε Scophedal (SCOpolamine, ePHEDrine και eukodAL) το 1942. Κατασκευάστηκε τελευταία φορά το 1987, αλλά μπορεί να φτιαχτεί σε φαρμακείο. Αυτός ο συνδυασμός είναι ουσιαστικά το ανάλογο οξυκωδόνης του " ύπνου λυκόφατος " με βάση τη μορφίνη, με προσθήκη εφεδρίνης για τη μείωση των κυκλοφοριακών και αναπνευστικών επιδράσεων.[88] Το φάρμακο έγινε γνωστό ως "Θαυματουργό φάρμακο της δεκαετίας του 1930" στην ηπειρωτική Ευρώπη και αλλού και ήταν η επιλογή της Βέρμαχτ για αναλγητικό πεδίου μάχης για κάποιο χρονικό διάστημα. Το φάρμακο σχεδιάστηκε ρητά για να παρέχει αυτό που η αίτηση διπλώματος ευρεσιτεχνίας και το ένθετο πακέτου αναφέρονται ως «πολύ βαθιά αναλγησία και βαθιά και έντονη ευφορία» καθώς και ηρεμιστική και πρόδρομη αμνησία χρήσιμη για περιπτώσεις χειρουργικών επεμβάσεων και τραυματισμών στο πεδίο της μάχης. Η οξυκωδόνη φέρεται να επιλέχθηκε έναντι της μορφίνης, της υδρομορφόνης και της υδροκοδόνης για αυτό το προϊόν επειδή η οξυκωδόνη έχει υποκειμενικά στοιχεία στο προφίλ παρενεργειών παρόμοια με την κοκαΐνη.[89]
Κατά τη διάρκεια της Επιχείρησης Χίμλερ, το Σκόφενταλ φέρεται να εγχύθηκε επίσης σε μαζική υπερβολική δόση στους κρατούμενους ντυμένους με στολές Πολωνικού Στρατού στο σκηνικό περιστατικό την 1η Σεπτεμβρίου 1939 που άνοιξε τον Δεύτερο Παγκόσμιο Πόλεμο.[88][90]
Οι προσωπικές σημειώσεις του ιατρού του Αδόλφου Χίτλερ, Τέοντορ Μορέλ, δείχνουν ότι ο Χίτλερ έλαβε επανειλημμένες ενέσεις οξυκωδόνης και Scophedal, καθώς και πεθιδίνη και μορφίνη λιγότερο συχνά. Η οξυκωδόνη δεν μπορούσε να ληφθεί μετά τα τέλη Ιανουαρίου 1945.[91][92]
Η Purdue Pharma - μια ιδιωτική εταιρεία που εδρεύει στο Στάμφορντ του Κοννέκτικατ, ανέπτυξε το συνταγογραφούμενο παυσίπονο OxyContin. Με την κυκλοφορία του το 1995, το OxyContin χαιρετίστηκε ως ιατρική αποκάλυψη, ένα ναρκωτικό μακράς διάρκειας που θα μπορούσε να βοηθήσει ασθενείς που υποφέρουν από μέτριο έως σοβαρό πόνο. Το φάρμακο έγινε μεγάλη επιτυχία, και σύμφωνα με πληροφορίες έχει αποφέρει περίπου 35 δισεκατομμύρια δολάρια σε έσοδα για τον Purdue.[93]
Νομικό καθεστώς[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη υπόκειται σε διεθνείς συμβάσεις για τα ναρκωτικά. Επιπλέον, η οξυκωδόνη υπόκειται σε εθνικούς νόμους που διαφέρουν ανά χώρα. Η σύμβαση του 1931 για τον περιορισμό της παρασκευής και τη ρύθμιση της διανομής ναρκωτικών φαρμάκων της Κοινωνίας των Εθνών περιελάμβανε την οξυκωδόνη.[94] Η Ενιαία Σύμβαση του 1961 για τα ναρκωτικά των Ηνωμένων Εθνών, η οποία αντικατέστησε τη σύμβαση του 1931, ταξινόμησε την οξυκωδόνη στο Παράρτημα Ι.[95] Παγκόσμιοι περιορισμοί στα φάρμακα του Προγράμματος Ι περιλαμβάνουν «περιορισμό αποκλειστικά σε ιατρικούς και επιστημονικούς σκοπούς την παραγωγή, κατασκευή, εξαγωγή, εισαγωγή, διανομή, εμπορία, χρήση και κατοχή» αυτών των ναρκωτικών · «απαιτούν ιατρικές συνταγές για την προμήθεια ή διανομή [αυτών των] φαρμάκων σε άτομα» και «αποτροπή της συσσώρευσης» ποσοτήτων αυτών των φαρμάκων «που υπερβαίνουν εκείνες που απαιτούνται για τη συνήθη συμπεριφορά των επιχειρήσεων».

Η οξυκωδόνη είναι φάρμακο κατηγορίας Α βάσει του νόμου περί κατάχρησης ναρκωτικών στο Ηνωμένο Βασίλειο.[96] Για φάρμακα κατηγορίας Α, τα οποία «θεωρούνται τα πιο πιθανά να προκαλέσουν βλάβη» και η κατοχή χωρίς ιατρική συνταγή τιμωρείται με φυλάκιση έως επτά ετών, απεριόριστο πρόστιμο ή και τα δύο.[97] Η παράνομη εμπορεία του φαρμάκου τιμωρείται με ισόβια κάθειρξη, απεριόριστο πρόστιμο ή και τα δύο. Επιπλέον, η οξυκωδόνη είναι φάρμακο του Προγράμματος 2 σύμφωνα με τους κανονισμούς κατάχρησης ναρκωτικών 2001 που «προβλέπουν ορισμένες εξαιρέσεις από τις διατάξεις του νόμου 1971 περί κατάχρησης ναρκωτικών».[98]
Σύμφωνα με το νόμο περί ελεγχόμενων ουσιών των Ηνωμένων Πολιτειών, η οξυκωδόνη είναι ελεγχόμενη ουσία του παραρτήματος ΙΙ είτε από μόνη της είτε μέρος ενός φαρμάκου πολλαπλών συστατικών.[99] Η DEA καταχωρεί την οξυκωδόνη τόσο προς πώληση όσο και για χρήση στην κατασκευή άλλων οπιοειδών ως ACSCN 9143 και το 2013 ενέκρινε τις ακόλουθες ετήσιες συνολικές ποσοστώσεις παραγωγής: 131,5 μετρικοί τόνοι προς πώληση, από 153,75 το 2012 και 10,25 μετρικούς τόνους για μετατροπή, αμετάβλητοι από το προηγούμενο έτος.[100] Το 2020, η κατοχή οξυκωδόνης αποποινικοποιήθηκε στην πολιτεία του Όρεγκον των ΗΠΑ.[101]
Ψυχαγωγική χρήση[Επεξεργασία | επεξεργασία κώδικα]
Η οξυκωδόνη, όπως και άλλα οπιοειδή αναλγητικά, τείνει να προκαλεί συναισθήματα ευφορίας, χαλάρωσης και μειωμένου άγχους σε όσους είναι περιστασιακοί χρήστες.[102] Αυτές οι επιδράσεις το καθιστούν ένα από τα πιο συχνά καταχρησιμοποιούμενα φάρμακα στις Ηνωμένες Πολιτείες.[103]
Η μη ιατρική χρήση της οξυκωδόνης υπήρχε από τις αρχές της δεκαετίας του 1970, αλλά έως το 2015, το 91% ενός εθνικού δείγματος χρηστών ενέσιμων ναρκωτικών στην Αυστραλία είχαν αναφέρει χρήση οξυκωδόνης και το 27% την ένεση τους τελευταίους έξι μήνες.[104]
Η κατάχρηση και η εκτροπή της οξυκωδόνης στο Ηνωμένο Βασίλειο ξεκίνησαν στις αρχές έως τα μέσα της δεκαετίας του 2000.[105] Ο πρώτος γνωστός θάνατος λόγω υπερδοσολογίας στο Ηνωμένο Βασίλειο σημειώθηκε το 2002[106] Ωστόσο, η ψυχαγωγική χρήση παραμένει σχετικά σπάνια.
Στις Ηνωμένες Πολιτείες, περισσότερα από 12 εκατομμύρια άνθρωποι χρησιμοποιούν οπιοειδή ναρκωτικά.[107] Τα οπιοειδή ήταν υπεύθυνα για 49.000 από τους 72.000 θανάτους από υπερδοσολογία φαρμάκων στις ΗΠΑ το 2017.[108] Τον Σεπτέμβριο του 2013, η FDA κυκλοφόρησε νέες κατευθυντήριες γραμμές για τις ετικέτες των μακράς δράσης και εκτεταμένης απελευθέρωσης οπιοειδών που απαιτούσαν από τους κατασκευαστές να αφαιρέσουν το μέτριο πόνο ως ένδειξη για τη χρήση, και να αναφέρουν ότι το φάρμακο είναι για «πόνο αρκετά σοβαρό ώστε να απαιτεί καθημερινά, όλο το εικοσιτετράωρο, μακροχρόνια θεραπεία με οπιοειδή.»[109] Η επικαιροποιημένη ετικέτα δεν περιόρισε τους γιατρούς από τη συνταγογράφηση οπιοειδών για μέτρια, όπως απαιτείται για τη χρήση.
Η οξυκωδόνη είναι το πιο ευρέως χρησιμοποιούμενο ψυχαγωγικό οπιοειδές στην Αμερική. Το Υπουργείο Υγείας και Ανθρωπίνων Υπηρεσιών των ΗΠΑ εκτιμά ότι περίπου 11 εκατομμύρια άνθρωποι στις ΗΠΑ καταναλώνουν οξυκωδόνη με μη ιατρικό τρόπο ετησίως.[110] Το 2007, πραγματοποιήθηκαν περίπου 42.800 επισκέψεις στα επείγοντα λόγω «επεισοδίων» που αφορούσαν οξυκωδόνη.[111] Η οξυκωδόνη μπορεί να ληφθεί από το στόμα ή να καταποθεί μέσω εισπνοής. Επίσης, χρησιμοποιείται ενδοφλεβίως ή μέσω εισπνοής θερμών ατμών. Το 2008, η ψυχαγωγική χρήση οξυκωδόνης και υδροκοδόνης εμπλεκόταν σε 14.800 θανάτους. Μερικές από τις περιπτώσεις οφείλονταν σε υπερδοσολογία της παρακεταμόλης στο σκεύασμα, με αποτέλεσμα θανατηφόρα ηπατική βλάβη.[112] Τον Αύγουστο του 2010, η Purdue Pharma αναδιαμόρφωσε τη σειρά οξυκωδόνης μακράς δράσης, που κυκλοφόρησε ως OxyContin, χρησιμοποιώντας ένα πολυμερές, το Intac,[113] για να κάνει τα χάπια εξαιρετικά δύσκολο να διαλυθούν[114] σε νερό και να συνθλιβούν για να μειώσουν την κατάχρηση του OxyContin.[115] Η FDA ενέκρινε την επισήμανση της αναδιατυπωμένης έκδοσης ως ανθεκτική στην κατάχρηση τον Απρίλιο του 2013.[116]
Η Pfizer κατασκευάζει ένα παρασκεύασμα οξυκωδόνης βραχείας δράσης, που διατίθεται στο εμπόριο ως Oxecta, το οποίο περιέχει ανενεργά συστατικά, που αναφέρονται ως αποτρεπτικά συστατικά ανθεκτικά σε παραβιάσεις.[117] Δεν αποτρέπει την κατάχρηση από του στόματος. Εγκριμένο από τη FDA στις ΗΠΑ τον Ιούνιο του 2011, το νέο σκεύασμα καθιστά τη σύνθλιψη, το μάσημα, το ρουθούνισμα ή την ένεση του οπιοειδούς λόγω της αλλαγής στις χημικές του ιδιότητες μη πρακτική.[118]
Οικονομικά[Επεξεργασία | επεξεργασία κώδικα]
Η Διεθνής Επιτροπή Ελέγχου Ναρκωτικών υπολόγισε 10,4 τόνοι οξυκωδόνης κατασκευάστηκαν παγκοσμίως το 1998 · έως το 2007, ο αριθμός αυτός είχε αυξηθεί σε 68 τόνους.[119] Οι Ηνωμένες Πολιτείες αντιπροσώπευαν το 82% της κατανάλωσης το 2007, με 47 τόνους. Ο Καναδάς, η Γερμανία, η Αυστραλία και η Γαλλία αντιστοιχούσαν στο 13% της κατανάλωσης το 2007.[120] Το 2010, 1,2 τόνοι οξυκωδόνης κατασκευάστηκαν παράνομα χρησιμοποιώντας ψεύτικο αποτύπωμα χαπιού. Αυτό αντιπροσώπευε το 0,8% της κατανάλωσης. Αυτά τα παράνομα δισκία κατασχέθηκαν αργότερα από την αμερικανική αρχή επιβολής ναρκωτικών, σύμφωνα με το Διεθνές Συμβούλιο Ελέγχου Ναρκωτικών.[121] Το διοικητικό συμβούλιο ανέφερε επίσης ότι 111 τόνοι κατασκευάστηκαν το 2010. Ο αριθμός αυτός είχε μειωθεί από το ρεκόρ των 123 τόνων το 2009.[122]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Bonewit-West K, Hunt SA, Applegate E (2012). Today's Medical Assistant: Clinical and Administrative Procedures (στα Αγγλικά). Elsevier Health Sciences. σελ. 571. ISBN 9781455701506.
- ↑ 2,0 2,1 «Oxycodone Use During Pregnancy». Drugs.com. 14 Οκτωβρίου 2019. Ανακτήθηκε στις 12 Απριλίου 2020.
- ↑ 3,0 3,1 «Oxycodone». Journal of Pain and Symptom Management 29 (5 Suppl): S47-56. May 2005. doi:. PMID 15907646.
- ↑ 4,0 4,1 4,2 4,3 «Roxicodone, OxyContin (oxycodone) dosing, indications, interactions, adverse effects, and more». Medscape Reference. WebMD. Ανακτήθηκε στις 8 Απριλίου 2014.
- ↑ 5,0 5,1 5,2 5,3 5,4 Elliott, Jennifer A.· Smith, Howard S. (19 Απριλίου 2016). Handbook of Acute Pain Management. CRC Press. σελίδες 82–. ISBN 978-1-4665-9635-1.
- ↑ 6,00 6,01 6,02 6,03 6,04 6,05 6,06 6,07 6,08 6,09 6,10 6,11 6,12 Smith, Howard· Passik, Steven (25 Απριλίου 2008). Pain and Chemical Dependency. Oxford University Press USA. σελίδες 195–. ISBN 978-0-19-530055-0.
- ↑ 7,0 7,1 7,2 «Roxicodone, OxyContin (oxycodone) dosing, indications, interactions, adverse effects, and more». Medscape Reference. WebMD. Ανακτήθηκε στις 4 Ιανουαρίου 2019.
- ↑ Yarbro, Connie Henke· Wujcik, Debra· Gobel, Barbara Holmes (15 Νοεμβρίου 2010). Cancer Nursing: Principles and Practice. Jones & Bartlett Publishers. σελίδες 695–. ISBN 978-1-4496-1829-2.
- ↑ 9,0 9,1 9,2 McPherson, Richard A.· Pincus, Matthew R. (31 Μαρτίου 2016). Henry's Clinical Diagnosis and Management by Laboratory Methods. Elsevier Health Sciences. σελίδες 336–. ISBN 978-0-323-41315-2.
- ↑ 10,0 10,1 10,2 10,3 «Analgesic efficacy of controlled-release oxycodone in postoperative pain». Journal of Clinical Pharmacology 36 (7): 595–603. July 1996. doi:. PMID 8844441. https://archive.org/details/sim_journal-of-clinical-pharmacology_1996-07_36_7/page/595. «Treatment with CR oxycodone was safe and effective in this study, and its characteristics will be beneficial in the treatment of pain.».
- ↑ O'Neil MJ, επιμ. (2006). The Merck index (14th έκδοση). Whitehouse Station, NJ: Merck & Co. ISBN 978-0-911910-00-1.
- ↑ Eddy NB (1973). The National Research Council involvement in the opiate problem, 1928–1971. Washington: National Academy of Sciences.
- ↑ «The Committee on Problems of Drug Dependence: a legacy of the National Academy of Sciences. A historical account». Drug and Alcohol Dependence 23 (3): 183–218. June 1989. doi:. PMID 2666074. https://archive.org/details/sim_drug-and-alcohol-dependence_1989-06_23_3/page/183.
- ↑ 14,00 14,01 14,02 14,03 14,04 14,05 14,06 14,07 14,08 14,09 14,10 14,11 14,12 «Oxycodone Monograph for Professionals». Drugs.com. AHFS. Ανακτήθηκε στις 28 Δεκεμβρίου 2018.
- ↑ 15,0 15,1 «Managing severe pain and abuse potential: the potential impact of a new abuse-deterrent formulation oxycodone/naltrexone extended-release product». Journal of Pain Research 11: 301–311. 2018. doi:. PMID 29445297.
- ↑ British national formulary : BNF 74 (74 έκδοση). British Medical Association. 2017. σελ. 442. ISBN 978-0857112989.
- ↑ 17,0 17,1 Talley, Nicholas J· Frankum, Brad (10 Φεβρουαρίου 2015). Essentials of Internal Medicine 3e. Elsevier Health Sciences. σελίδες 491–. ISBN 978-0-7295-8081-6.
- ↑ Stanford School of Medicine, Palliative Care, Opioid Conversion / Equivalency Table. 2013-04-20. Αρχειοθετήθηκε από το πρωτότυπο στις 2020-09-09. https://web.archive.org/web/20200909012800/https://palliative.stanford.edu/opioid-conversion/equivalency-table/. Ανακτήθηκε στις 2020-12-08.
- ↑ 19,0 19,1 19,2 Sneader, W. (2005). Drug discovery: a history. Hoboken, NJ: Wiley. σελ. 119. ISBN 978-0-471-89980-8.
- ↑ «The Top 300 of 2020». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Oxycodone - Drug Usage Statistics». ClinCalc. Ανακτήθηκε στις 11 Απριλίου 2020.
- ↑ «Do abuse deterrent opioid formulations work?». Journal of Opioid Management 13 (6): 365–378. 2017. doi:. PMID 29308584.
- ↑ «Oxycodone: a review of its use in the management of pain». Current Medical Research and Opinion 24 (1): 175–92. January 2008. doi:. PMID 18039433.
- ↑ 24,0 24,1 «Oxycodone controlled release in cancer pain management» (PDF). Therapeutics and Clinical Risk Management 2 (3): 229–34. September 2006. doi:. PMID 18360598. PMC 1936259. https://europepmc.org/backend/ptpmcrender.fcgi?accid=PMC1936259&blobtype=pdf. Ανακτήθηκε στις January 30, 2019.
- ↑ «Morphine and alternative opioids in cancer pain: the EAPC recommendations». British Journal of Cancer 84 (5): 587–93. March 2001. doi:. PMID 11237376.
- ↑ «FDA approves OxyContin for kids 11 to 16». www.msn.com. Αρχειοθετήθηκε από το πρωτότυπο στις 30 Ιουνίου 2017. Ανακτήθηκε στις 11 Φεβρουαρίου 2018.
- ↑ Gould III, Harry J (11 Δεκεμβρίου 2006). Understanding Pain: What It Is, Why It Happens, and How It's Managed. Demos Medical Publishing. σελίδες 71–. ISBN 978-1-934559-82-6.
- ↑ Graves, Keith (29 Σεπτεμβρίου 2015). Drug I.D. & Symptom Guide 6th Edition QWIK-CODE. LawTech Publishing Group. σελίδες 99–. ISBN 978-1-56325-225-9.
- ↑ Linda Skidmore-Roth (16 Ιουλίου 2015). Mosby's Drug Guide for Nursing Students, with 2016 Update. Elsevier Health Sciences. σελίδες 789–. ISBN 978-0-323-17297-4.
- ↑ «accessdata.fda.gov» (PDF). Ανακτήθηκε στις 11 Φεβρουαρίου 2018.
- ↑ Sinatra, Raymond S.· de Leon-Cassasola, Oscar A. (27 Απριλίου 2009). Acute Pain Management. Cambridge University Press. σελίδες 198–. ISBN 978-0-521-87491-5.
- ↑ Staats, Peter S.· Silverman, Sanford M. (28 Μαΐου 2016). Controlled Substance Management in Chronic Pain: A Balanced Approach. Springer. σελίδες 172–. ISBN 978-3-319-30964-4.
- ↑ «FDA Approves Troxyca® ER (Oxycodone Hydrochloride and Naltrexone Hydrochloride) Extended-release Capsules CII with Abuse-deterrent Properties for the Management of Pain». 19 Αυγούστου 2016.
- ↑ 34,0 34,1 34,2 34,3 Mellar P. Davis (28 Μαΐου 2009). Opioids in Cancer Pain. OUP Oxford. σελίδες 155–158. ISBN 978-0-19-923664-0.
- ↑ 35,0 35,1 35,2 Karen Forbes (29 Νοεμβρίου 2007). Opioids in Cancer Pain. OUP Oxford. σελίδες 64–65. ISBN 978-0-19-921880-6.
- ↑ Bradbury, Helen· Hodge, Barry Strickland (8 Νοεμβρίου 2013). Practical Prescribing for Medical Students. SAGE Publications. σελίδες 93–. ISBN 978-1-4462-9753-7.
- ↑ American Society of Health-System Pharmacists (23 Μαρτίου 2009). «Oxycodone». U.S. National Library of Medicine, MedlinePlus. Ανακτήθηκε στις 27 Μαρτίου 2009.
- ↑ 38,0 38,1 Fitzgibbon, Dermot R.· Loeser, John D. (28 Μαρτίου 2012). Cancer Pain. Lippincott Williams & Wilkins. σελίδες 198–. ISBN 978-1-4511-5279-1.
- ↑ «Oxycodone Side Effects». Drugs.com. Ανακτήθηκε στις 22 Μαΐου 2013.
- ↑ 40,0 40,1 40,2 40,3 40,4 1. Package insert Oxycontin (PDF). Stamford, CT: Purdue Pharma L.P. 5 Νοεμβρίου 2007. Ανακτήθηκε στις 23 Μαρτίου 2009.
- ↑ «Oxycodone: a pharmacological and clinical review». Clinical & Translational Oncology 9 (5): 298–307. May 2007. doi:. PMID 17525040.
- ↑ «Fixed-ratio combination oxycodone/naloxone compared with oxycodone alone for the relief of opioid-induced constipation in moderate-to-severe noncancer pain». Current Medical Research and Opinion 24 (12): 3503–12. December 2008. doi:. PMID 19032132.
- ↑ «Oxycodone». Center for Substance Abuse Research. 2 Μαΐου 2005. Αρχειοθετήθηκε από το πρωτότυπο στις 6 Απριλίου 2009. Ανακτήθηκε στις 25 Μαρτίου 2009.
- ↑ «Tapering off opioids: When and how». Mayo Clinic. Ανακτήθηκε στις 10 Οκτωβρίου 2020.
- ↑ «OxyContin and neonatal abstinence syndrome». Journal of Perinatology 22 (4): 324–5. June 2002. doi:. PMID 12032797.
- ↑ «The effect of opioid therapy on endocrine function». The American Journal of Medicine 126 (3 Suppl 1): S12-8. March 2013. doi:. PMID 23414717.
- ↑ «Drugs Most Frequently Involved in Drug Overdose Deaths: United States, 2011–2016» (PDF). CDC. 12 Δεκεμβρίου 2018. Ανακτήθηκε στις 21 Δεκεμβρίου 2018.
- ↑ «Clinical Reasoning: A young woman with respiratory failure, hearing loss, and paraplegia». Neurology 88 (10): e78–e84. March 2017. doi:. PMID 28265044. https://www.researchgate.net/publication/314274959. Ανακτήθηκε στις 2017-03-09.
- ↑ «Oxycodone concentrations are greatly increased by the concomitant use of ritonavir or lopinavir/ritonavir». European Journal of Clinical Pharmacology 66 (10): 977–85. October 2010. doi:. PMID 20697700. https://hal.archives-ouvertes.fr/hal-00614173.
- ↑ «Rifampin greatly reduces the plasma concentrations of intravenous and oral oxycodone». Anesthesiology 110 (6): 1371–8. June 2009. doi:. PMID 19417618. https://archive.org/details/sim_anesthesiology_2009-06_110_6/page/1371.
- ↑ «Decreased responsiveness to oxycodone: A case of a pharmacokinetic drug interaction?». Journal of Opioid Management 11 (4): 357–61. 2015. doi:. PMID 26312962.
- ↑ King (25 Οκτωβρίου 2010). Pharmacology for Women's Health. Jones & Bartlett Publishers. σελίδες 332–. ISBN 978-1-4496-1073-9.
- ↑ Chestnut, David H.· Wong, Cynthia A (28 Φεβρουαρίου 2014). Chestnut's Obstetric Anesthesia: Principles and Practice E-Book. Elsevier Health Sciences. σελίδες 611–. ISBN 978-0-323-11374-8.
- ↑ Adriana P. Tiziani (1 Ιουνίου 2013). Havard's Nursing Guide to Drugs. Elsevier Health Sciences. σελίδες 933–. ISBN 978-0-7295-8162-2.
- ↑ Chahl L (1996). «Opioids- mechanism of action». Aust Prescr 19 (3): 63–65. doi:.
- ↑ Christoph Stein (1999). Opioids in Pain Control: Basic and Clinical Aspects. Cambridge University Press. σελίδες 46–. ISBN 978-0-521-62269-1.
- ↑ Squire, Larry· Berg, Darwin (17 Δεκεμβρίου 2012). Fundamental Neuroscience. Academic Press. σελίδες 884–. ISBN 978-0-12-385871-9.
- ↑ Kringelbach, Morten L.· Berridge, Kent C. (2010). Pleasures of the Brain. Oxford University Press. σελίδες 33–. ISBN 978-0-19-533102-8.
- ↑ Sinatra, Raymond S.· Jahr, Jonathan S. (14 Οκτωβρίου 2010). The Essence of Analgesia and Analgesics. Cambridge University Press. σελίδες 167–. ISBN 978-1-139-49198-3.
- ↑ «Treatment of Pain». Merck Manuals Professional Edition. Ανακτήθηκε στις 24 Απριλίου 2016.
- ↑ Ferrell, Betty Rolling· Pasero, Chris (2010). «Table 16-1 Equianalgesic Dose Chart». Pain Assessment and Pharmacologic Management (στα Αγγλικά). Elsevier Health Sciences. ISBN 978-0323082631.
- ↑ Levy, Enno Freye· Victor, Joseph (2007). Opioids in medicine a comprehensive review on the mode of action and the use of analgesics in different clinical pain states. New York: Springer Science+Business Media B.V. σελ. 371. ISBN 978-1402059476.
- ↑ 63,0 63,1 63,2 63,3 63,4 «Pharmacokinetics and pharmacodynamics of oral oxycodone in healthy human subjects: role of circulating active metabolites». Clinical Pharmacology and Therapeutics 79 (5): 461–79. May 2006. doi:. PMID 16678548. https://archive.org/details/sim_clinical-pharmacology-and-therapeutics_2006-05_79_5/page/461.
- ↑ 64,0 64,1 «Contribution of oxycodone and its metabolites to the overall analgesic effect after oxycodone administration». Expert Opinion on Drug Metabolism & Toxicology 9 (5): 517–28. May 2013. doi:. PMID 23488585.
- ↑ 65,0 65,1 «Pharmacological characterization of noroxymorphone as a new opioid for spinal analgesia». Anesthesia and Analgesia 106 (2): 463–70, table of contents. February 2008. doi:. PMID 18227301. https://semanticscholar.org/paper/0d0a802acff3976f86e165e7966c5a40ea3cc250.
- ↑ 66,0 66,1 66,2 Victor R. Preedy (25 Απριλίου 2016). Neuropathology of Drug Addictions and Substance Misuse Volume 3: General Processes and Mechanisms, Prescription Medications, Caffeine and Areca, Polydrug Misuse, Emerging Addictions and Non-Drug Addictions. Elsevier Science. σελίδες 462–464. ISBN 978-0-12-800677-1.
- ↑ Firestein, Gary S.· Budd, Ralph C. (21 Ιουνίου 2016). Kelley and Firestein's Textbook of Rheumatology. Elsevier Health Sciences. σελίδες 1080–. ISBN 978-0-323-31696-5.
- ↑ «The intrinsic antinociceptive effects of oxycodone appear to be kappa-opioid receptor mediated». Pain 73 (2): 151–7. November 1997. doi:. PMID 9415500. https://archive.org/details/sim_pain_1997-11_73_2/page/151.
- ↑ «Differences between and combinations of opioids re-visited». Current Opinion in Anesthesiology 21 (5): 596–601. October 2008. doi:. PMID 18784485.
- ↑ «How different is oxycodone from morphine?». Pain 132 (3): 227–8. December 2007. doi:. PMID 17961923.
- ↑ «Characterization of the antinociceptive effects of oxycodone in diabetic mice». European Journal of Pharmacology 535 (1–3): 145–51. March 2006. doi:. PMID 16533506.
- ↑ «Involvement of mu1-opioid receptor on oxycodone-induced antinociception in diabetic mice». European Journal of Pharmacology 560 (2–3): 160–2. April 2007. doi:. PMID 17292346.
- ↑ Analgesic Expert Group. Therapeutic Guidelines: Analgesic. Version 4. Melbourne: Therapeutic Guidelines Ltd, 2007.
- ↑ 74,0 74,1 «Oxycodone». www.drugbank.ca. Ανακτήθηκε στις 24 Ιανουαρίου 2019.
- ↑ «Tentative identification of novel oxycodone metabolites in human urine». Journal of Analytical Toxicology 27 (6): 346–52. September 2003. doi:. PMID 14516487.
- ↑ 76,0 76,1 76,2 Anzenbacher, Pavel· Zanger, Ulrich M. (29 Μαΐου 2012). Metabolism of Drugs and Other Xenobiotics. John Wiley & Sons. σελίδες 420–. ISBN 978-3-527-32903-8.
- ↑ «Codeine intoxication associated with ultrarapid CYP2D6 metabolism». The New England Journal of Medicine 351 (27): 2827–31. December 2004. doi:. PMID 15625333.
- ↑ «Inhibition by fluoxetine of cytochrome P450 2D6 activity». Clinical Pharmacology and Therapeutics 53 (4): 401–9. April 1993. doi:. PMID 8477556. https://archive.org/details/sim_clinical-pharmacology-and-therapeutics_1993-04_53_4/page/401.
- ↑ «Genetic polymorphisms and drug interactions modulating CYP2D6 and CYP3A activities have a major effect on oxycodone analgesic efficacy and safety». British Journal of Pharmacology 160 (4): 919–30. June 2010. doi:. PMID 20590588.
- ↑ 80,0 80,1 «Oxycodone». The American Society of Health-System Pharmacists. Ανακτήθηκε στις 3 Απριλίου 2011.
- ↑ «Oxycodone». www.drugbank.ca. Ανακτήθηκε στις 24 Ιανουαρίου 2019.
- ↑ Davis, Peter J.· Cladis, Franklyn P. (15 Οκτωβρίου 2016). Smith's Anesthesia for Infants and Children E-Book. Elsevier Health Sciences. σελίδες 234–. ISBN 978-0-323-38869-6.
- ↑ 83,0 83,1 Ryan, Harriet; Girion, Lisa; Glover, Scott (7 July 2016). «You want a description of hell?' OxyContin's 12-hour problem». Los Angeles Times. https://www.latimes.com/projects/oxycontin-part1/. Ανακτήθηκε στις 8 July 2018.
- ↑ «'Q12' Workshops, 2001». Los Angeles Times. http://documents.latimes.com/q12-workshops-2001/. Ανακτήθηκε στις 8 July 2018.
- ↑ Freund, Martin; Speyer, Edmund (24 November 1916). «Über die Umwandlung von Thebain in Oxycodeinon und dessen Derivate». Journal für Praktische Chemie 94 (1): 135–178. doi:. https://zenodo.org/record/1428060.
- ↑ «Martin Freund». Berichte der Deutschen Chemischen Gesellschaft (A and B Series) 54 (5): A53–A79. 7 May 1921. doi:.
- ↑ The Holocaust : a history of the Jews of Europe during the Second World War (1st American έκδοση). Holt, Rinehart, and Winston. 1986. σελίδες 346. ISBN 0-03-062416-9. Ανακτήθηκε στις 3 Ιουνίου 2020.
- ↑ 88,0 88,1 «Scophedal (SEE) was it a fad or a miracle drug?». Bulletin of Anesthesia History 21 (4): 12–4. October 2003. doi:. PMID 17494237.
- ↑ William S Burroughs 1952 letter to Allen Ginsburg concerning Eukodal, in Collected Correspondance, pp 141-2
- ↑ Merck 1930 package insert for Skophedal (German)
- ↑ Breitenbach, Dagmar (9 Σεπτεμβρίου 2015). «A fresh light on the Nazis' wartime drug addiction». Deutsche Welle. Ανακτήθηκε στις 24 Απριλίου 2016.
- ↑ Ohler, Norman· Whiteside, Shaun (2017). Blitzed: drugs in the Third Reich (First U.S. έκδοση). Boston: Houghton Mifflin Harcourt. σελ. 194. ISBN 978-1-328-66379-5.
- ↑ Keefe, Patrick Radden (23 Οκτωβρίου 2017). «The Family That Built an Empire of Pain». The New Yorker. ISSN 0028-792X. Ανακτήθηκε στις 2 Φεβρουαρίου 2019.
- ↑ League of Nations (1931). «Convention for limiting the manufacture and regulating the distribution of narcotic drugs» (PDF). Ανακτήθηκε στις 4 Απριλίου 2009.
- ↑ «United Nations conference for the adoption of a single convention on narcotic drugs. Final act» (PDF). 1961. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 17 Αυγούστου 2011. Ανακτήθηκε στις 4 Απριλίου 2009.
- ↑ «List of drugs currently controlled under the Misuse of Drugs legislation» (PDF). UK. Home Office. 2009. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 5 Φεβρουαρίου 2007. Ανακτήθηκε στις 8 Απριλίου 2009.
- ↑ «Class A, B and C drugs». UK. Home Office. Αρχειοθετήθηκε από το πρωτότυπο στις 4 Αυγούστου 2007. Ανακτήθηκε στις 8 Απριλίου 2009.
- ↑ «Statutory instrument 2001 No. 3998. The Misuse of Drugs regulations 2001». UK. Office of Public Sector Information. Ανακτήθηκε στις 8 Απριλίου 2009.
- ↑ DEA. «Controlled substance scheduling». Drug information and scheduling. Drug Enforcerment Administration. Αρχειοθετήθηκε από το πρωτότυπο στις 21 Νοεμβρίου 2015. Ανακτήθηκε στις 23 Νοεμβρίου 2015.
- ↑ «DEA Diversion Control CSA». US Dept of Justice – DEA. Αρχειοθετήθηκε από το πρωτότυπο στις 16 Μαΐου 2013. Ανακτήθηκε στις 23 Μαΐου 2013.
- ↑ Andrew Selsky (4 November 2020). «Oregon leads the way in decriminalizing hard drugs». The Associated Press. https://apnews.com/article/oregon-first-decriminalizing-hard-drugs-01edca37c776c9ea8bfd4afdd7a7a33e. Ανακτήθηκε στις 7 November 2020.
- ↑ «OxyContin: Pain Relief vs. Abuse». Ανακτήθηκε στις 11 Φεβρουαρίου 2018.
- ↑ «Top 10 Most Commonly Abused Prescription Medications». 28 Απριλίου 2014. Αρχειοθετήθηκε από το πρωτότυπο στις 2 Ιανουαρίου 2018. Ανακτήθηκε στις 11 Φεβρουαρίου 2018.
- ↑ Australian drug trends 2007. Findings from the Illicit Drug Reporting System (IDRS) (PDF). Sydney: National Drug and Alcohol Research Centre, University of New South Wales. 2008. ISBN 978-0-7334-2625-4.
- ↑ Gordon T (2008-03-30). «Scots' use of 'hillbilly heroin' rises by 430%». Sunday Times (London).
- ↑ Thompson T (2002-03-24). «Epidemic fear as 'hillbilly heroin' hits the streets». Society Guardian. https://www.theguardian.com/society/2002/mar/24/drugsandalcohol. Ανακτήθηκε στις 2009-04-16.
- ↑ Girioin, Lisa; Haely, Melissa (11 September 2013). «FDA to require stricter labeling for pain drugs». Los Angeles Times: σελ. A1 and A9.
- ↑ «Overdose Death Rates». www.drugabuse.gov (στα Αγγλικά). 29 Ιανουαρίου 2019. Ανακτήθηκε στις 11 Μαΐου 2019.
- ↑ «ER/LA Opioid Analgesic Class Labeling Changes and Postmarket Requirements» (PDF). FDA. Ανακτήθηκε στις 12 Σεπτεμβρίου 2013.
- ↑ Now a counselor, she went from stoned to straight, San Francisco Chronicle, November 2. 2015.
- ↑ «Oxycontin and Addiction». consumer.healthday.com. Αρχειοθετήθηκε από το πρωτότυπο στις 15 Απριλίου 2016. Ανακτήθηκε στις 24 Απριλίου 2016.
- ↑ Policy Impact: Prescription Pain Killer Overdoses Centers for Disease Control and Prevention. Retrieved 24 December 2013.
- ↑ «New Abuse Deterrent Formulation Technology for Immediate-Release Opiods» (PDF). Grünenthal Group. Grünenthal Group Worldwide. 2010. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 22 Δεκεμβρίου 2015. Ανακτήθηκε στις 15 Δεκεμβρίου 2015.
- ↑ Diep, Francie (13 Μαΐου 2013). «How Do You Make a Painkiller Addiction-Proof». Popular Science. Bonnier Corporation. Ανακτήθηκε στις 30 Ιανουαρίου 2019.
- ↑ «Findings from Purdue's Post-Marketing Epidemiology Studies of Reformulated OxyContin's Effects». Αρχειοθετήθηκε από το πρωτότυπο στις 2013-06-14. https://web.archive.org/web/20130614115419/http://www.nascsa.org/Conference2012/Presentations/Coplan.pdf. Ανακτήθηκε στις 2020-12-08.
- ↑ «Press Announcements; FDA approves abuse-deterrent labeling for reformulated OxyContin». US Government – FDA. Αρχειοθετήθηκε από το πρωτότυπο στις 20 Μαΐου 2013. Ανακτήθηκε στις 23 Μαΐου 2013.
- ↑ «Pfizer and Acura Announce FDA Approval of Oxectatm (Oxycodone HCL, USP) CII». Pfizer News and Media. Pfizer Inc. Αρχειοθετήθηκε από το πρωτότυπο στις 22 Δεκεμβρίου 2015. Ανακτήθηκε στις 15 Δεκεμβρίου 2015.
- ↑ Fiore, Kristina (20 Ιουνίου 2011). «FDA Okays New Abuse-Resistant Opioid». MedPage Today. MedPage Today. Αρχειοθετήθηκε από το πρωτότυπο στις 22 Δεκεμβρίου 2015. Ανακτήθηκε στις 15 Δεκεμβρίου 2015.
- ↑ International Narcotics Control Board (2009). Narcotic drugs: estimated world requirements for 2009; statistics for 2007. Report E/INCB/2008/2 (PDF). New York: United Nations. ISBN 978-92-1-048124-3.
- ↑ «Availability of Opioid Analgesics in the World and Asia, With a special focus on: Indonesia, Philippines, Thailand» (PDF). University of Wisconsin Pain & Policy Studies Group/World Health Organization (WHO) Collaborating Center for Policy and Communications in Cancer Care. United Nations. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 26 Απριλίου 2012. Ανακτήθηκε στις 27 Νοεμβρίου 2011.
- ↑ Narcotic Drugs: Estimated World Requirements for 2012 and Statistics for 2010[νεκρός σύνδεσμος]. International Narcotics Control Board (2011).
- ↑ Narcotic Drugs: Estimated World Requirements for 2012 and Statistics for 2010. International Narcotics Control Board (2011).
Περαιτέρω ανάγνωση[Επεξεργασία | επεξεργασία κώδικα]
- «Oxycodone. Pharmacological profile and clinical data in chronic pain management». Minerva Anestesiologica 71 (7–8): 451–60. July–August 2005. PMID 16012419. Αρχειοθετήθηκε από το πρωτότυπο στις March 9, 2006. https://web.archive.org/web/20060309000726/http://www.minervamedica.it/pdf/R02Y2005/R02Y2005N07A0451.pdf.
Εξωτερικοί σύνδεσμοι[Επεξεργασία | επεξεργασία κώδικα]
- «Oxycodone». Drug Information Portal. U.S. National Library of Medicine.
- «Oxycodone hydrochloride». Drug Information Portal. U.S. National Library of Medicine.
