Φυτικό οξύ

Το φυτικό οξύ (αγγλ. phytic acid) είναι εξα-διυδροφωσφορικός εστέρας της ινοσιτόλης (συγκεκριμένα του ισομερούς μυο), που ονομάζεται συνήθως ινοσιτολικό εξαφωσφατίδιο (συντομογραφικά, IP6) και αποτελεί τη βασική μορφή αποθήκευσης του φωσφόρου σε πολλά φυτικά μέρη, ιδίως σε ποικιλίες σιτηρών (π.χ. σιτάρι, ρύζι, σίκαλη, κριθάρι).[1] Σε φυσιολογικές τιμές οξύτητας (pH), τα φωσφορικά άλατα ιονίζονται μερικώς, με αποτέλεσμα να παράγεται το φυτικό ανιόν.
Το (μυο) φυτικό ανιόν είναι άχρωμο, ενώ διαδραματίζει σημαντικό διατροφικό ρόλο ως η κύρια μορφή αποθήκευσης του φωσφόρου σε πολλούς φυτικούς ιστούς και στους σπόρους. Υπάρχει επίσης σε πολλά όσπρια και δημητριακά. Το φυτικό οξύ και το φυτικό ανιόν (αγγλ. phytate anion) έχουν ισχυρή δεσμευτική συγγένεια με τα διαιτητικά μέταλλα, το ασβέστιο, το σίδηρο και τον ψευδάργυρο, αναστέλλοντας την απορρόφησή τους στο λεπτό έντερο.[2]
Τα κατώτερα ινοσιτολικά πολυφωσφορικά είναι εστέρες της ινοσιτόλης με λιγότερα από έξι φωσφορικές ομάδες, όπως λ.χ. πεντα- (IP5), τετρα- (IP4) και τριφωσφορική ινοσιτόλη (IP3). Αυτά τα πολυφωσφορικά εμφανίζονται ευρέως στη φύση ως καταβολίτες του φυτικού οξέος.
Σπουδαιότητα για τη γεωργία[Επεξεργασία | επεξεργασία κώδικα]
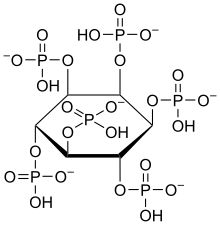
Το φυτικό οξύ ανακαλύφθηκε το 1903.[3]
Γενικά, ο φώσφορος και η ινοσιτόλη σε φυτική μορφή δεν είναι βιοδιαθέσιμα σε μη μηρυκαστικά ζώα επειδή αυτά τα ζώα δεν διαθέτουν το ένζυμο, φυτάση, που απαιτείται για την υδρόλυση των δεσμών ινοσιτόλης-φωσφορικού. Τα μηρυκαστικά είναι σε θέση να αφομοιώσουν το φυτικό άλας λόγω της φυτάσης που παράγεται από τους μικροοργανισμούς της μεγάλης κοιλίας.[4]
Στην πλειονότητα της βιομηχανοποιημένης γεωργίας, τα μη μηρυκαστικά ζώα, όπως λ.χ. οι χοίροι, τα πτηνά και τα ταψάρια,[5] τρέφονται κυρίως με δημητριακά, όπως καλαμπόκι, όσπρια και σόγια.[6] Επειδή το φυτικό οξύ -ή οι ενώσεις του- από αυτούς τους κόκκους και τα φασόλια δεν είναι διαθέσιμα για άμεση απορρόφηση, το μη απορροφημένο φυτικό οξύ διέρχεται μέσω του γαστρεντερικού σωλήνα, αυξάνοντας την ποσότητα του φωσφόρου στα κόπρανα.[4]
Η υπερβολική απέκκριση φωσφόρου μπορεί να οδηγήσει σε περιβαλλοντικά προβλήματα, όπως λ.χ. ο ευτροφισμός.[7] Η χρήση ήδη φυτρωμένων σπόρων μπορεί να μειώσει την ποσότητα των ανεπιθύμητων φυτικών οξέων στις ζωοτροφές, χωρίς να επιφέρει σημαντική μείωση της θρεπτικής αξίας τους. [8]
Πρόσθετα βιώσιμες μεταλλαγμένες σειρές χαμηλής περιεκτικότητας σε φυτικό οξύ έχουν αναπτυχθεί σε πολλά είδη καλλιεργειών.[9] Ωστόσο, προβλήματα βλάστησης φέρεται να έχουν εμποδίσει τη χρήση αυτών των ποικιλιών μέχρι στιγμής. Αυτό μπορεί να οφείλεται στον κρίσιμο ρόλο του φυτικού οξέος στην αποθήκευση τόσο του φωσφόρου όσο και των μεταλλικών ιόντων.[10] Οι φυτικές παραλλαγές έχουν επίσης τη δυνατότητα να αξιοποιηθούν για την αποκατάσταση του εδάφους, για την ακινητοποίηση του ουρανίου, του νικελίου και άλλων ανόργανων ρύπων.[11]
Βιολογικός ρόλος[Επεξεργασία | επεξεργασία κώδικα]
Αν και εξόχως δύσπεπτο για πολλά ζώα (αφού απαντάται συχνότατα σε σπόρους), το φυτικό οξύ και οι μεταβολίτες του έχουν αρκετούς σημαντικούς ρόλους για τα φυτά σε πρώιμη ηλικία.
Πιο συγκεκριμένα, το φυτικό οξύ λειτουργεί ως αποθήκη φωσφόρου, ως αποθήκη ενέργειας, ως πηγή κατιόντων και ως πηγή μυο-ινοσιτόλης (δηλ. μιας ουσίας που είναι πρόδρομος του κυτταρικού τοιχώματος). Το φυτικό οξύ είναι η κύρια μορφή αποθήκευσης του φωσφόρου στους σπόρους των φυτών.[12]
Στα ζωικά κύτταρα, τα (μυο) ινοσιτολικά πολυφωσφορικά είναι πανταχού παρόντα και το φυτικό οξύ (συν. ινοσιτολικό εξαφωσφατίδιο) είναι το πιο άφθονο, με τη συγκέντρωσή του να κυμαίνεται από 10 έως 100 μM στα κύτταρα των θηλαστικών, ανάλογα με τον τύπο του κυττάρου και το αναπτυξιακό στάδιο.[13] [14]
Αυτή η ένωση δεν λαμβάνεται από τη διατροφή των ζώων, αλλά πρέπει να συντίθεται στο εσωτερικό του κυττάρου από φωσφορικό άλας και ινοσιτόλη (η οποία με τη σειρά της παράγεται από τη γλυκόζη, συνήθως στα νεφρά). Η αλληλεπίδραση του ενδοκυτταρικού φυτικού οξέος με συγκεκριμένες ενδοκυτταρικές πρωτεΐνες έχει διερευνηθεί in vitro, και αυτές οι αλληλεπιδράσεις έχει βρεθεί ότι έχουν ως αποτέλεσμα την αναστολή ή την ενίσχυση των φυσιολογικών δραστηριοτήτων αυτών των πρωτεϊνών.[15][16]
Τα πιο ενδιαφέροντα στοιχεία από αυτές τις μελέτες υποδηλώνουν έναν ενδοκυτταρικό ρόλο για το φυτικό οξύ ως συμπαράγοντας στην επιδιόρθωση του DNA με μη ομόλογη τελική ένωση.[15] Άλλες μελέτες που χρησιμοποιούν μεταλλάξεις ζυμομύκητα έχουν επίσης προτείνει ότι το ενδοκυτταρικό φυτικό οξύ μπορεί να εμπλέκεται στην εξαγωγή mRNA από τον πυρήνα στο κυτταρόπλασμα.[17][18]
Το ινοσιτολικό εξαφωσφατίδιο διευκολύνει τον σχηματισμό της δέσμης των έξι ελίκων και τη συναρμολόγηση του ανώριμου πλέγματος HIV-1 Gag. Το IP6 αλληλεπιδρά με ιοντικές επαφές με δύο δακτυλίους υπολειμμάτων λυσίνης στο κέντρο του εξαμερούς Gag. Στη συνέχεια, η πρωτεολυτική διάσπαση αποκαλύπτει μια εναλλακτική θέση δέσμευσης, όπου η αλληλεπίδραση IP6 προάγει τη συναρμολόγηση του ώριμου πλέγματος καψιδίου. Αυτές οι μελέτες προσδιορίζουν το IP6 ως ένα φυσικό μικρό μόριο που προάγει τόσο τη συναρμολόγηση όσο και την ωρίμανση του HIV-1.[19]
Χρήσεις στην οδοντιατρική[Επεξεργασία | επεξεργασία κώδικα]
Το IP6 μπορεί να χρησιμοποιηθεί στην ενδοδοντική, συγκολλητική, προληπτική και αναγεννητική οδοντιατρική και στη βελτίωση των χαρακτηριστικών και της απόδοσης των οδοντιατρικών υλικών.[20][21] [22]
Χρήσεις στην επιστήμη τροφίμων[Επεξεργασία | επεξεργασία κώδικα]
Το φυτικό οξύ, κυρίως ως άλας με τη μορφή φυτίνης, βρίσκεται στο φλοιό και τους πυρήνες των σπόρων, [23] συμπεριλαμβανομένων των ξηρών καρπών, των δημητριακών και των οσπρίων.[2]
Οι τεχνικές παρασκευής του οικιακού φαγητού μπορούν να διασπάσουν το φυτικό οξύ σε όλα αυτά τα τρόφιμα. Το απλό μαγείρεμα του φαγητού θα μειώσει σε κάποιο βαθμό το φυτικό οξύ. Πιο αποτελεσματικές μέθοδοι είναι το μούλιασμα σε ένα όξινο μέσο, η βλάστηση και η ζύμωση γαλακτικού οξέος όπως λ.χ. σε προζύμι και τουρσί.[24]
Δεν παρατηρήθηκε ανιχνεύσιμο φυτικό οξύ ή ιόντα του (λιγότερο από 0,02% του υγρού βάρους) σε λαχανικά όπως π.χ. το κρεμμύδι ή τα φύλλα λάχανου, ή σε φρούτα όπως τα μήλα, τα πορτοκάλια, οι μπανάνες ή τα αχλάδια.[25]
Ως πρόσθετο τροφίμων, το φυτικό οξύ χρησιμοποιείται και ως συντηρητικό, με την ονομασία E391.[26][27]
Τρόφιμα με φυτικό οξύ[Επεξεργασία | επεξεργασία κώδικα]
Περιεκτικότητα τροφίμων σε φυτικό οξύ[28][25][29][30][31][32][33][34] Τρόφιμο Ποσοστό κατά βάρος (g/100 g) Min. Max. Σπόρος κάνναβης[23] 4.5 4.5 Κολοκυθόσπορος 4.3 4.3 Λιναρόσπορος 2.15 2.78 Σουσάμι 5.36 5.36 Αμύγδαλα 1.35 3.22 Καρύδα 0.36 0.36 Φουντούκι 0.65 0.65 Αράπικο φυστίκι 0.95 1.76 Καρύδι, κοινό 0.98 0.98 Βρώμη 0.42 1.16 Ρύζι, λευκό 0.14 0.60 Σιτάρι 0.39 1.35 Αλεύρι σιταριού 0.25 1.37 Ψωμί ολικής 0.43 1.05 Μπιζέλια 0.56 0.56 Ρεβύθια 0.44 0.50 Κύαμος σόγιας 1.00 2.22 Τόφου 1.46 2.90 Σπανάκι 0.22 NR Αβογκάντο 0.51 0.51 Κάστανο[35] 0.47
Aπορρόφηση μετάλλων[Επεξεργασία | επεξεργασία κώδικα]
Το φυτικό οξύ έχει ισχυρή συγγένεια με τα διαιτητικά μέταλλα, π.χ. το ασβέστιο, τον σίδηρο και τον ψευδάργυρο, αναστέλλοντας την απορρόφησή τους από το λεπτό έντερο.[2][36]
Τα φυτοχημικά όπως λ.χ. πολυφαινόλες και ταννίνες επηρεάζουν τη δέσμευση.[37] Όταν ο σίδηρος και ο ψευδάργυρος συνδέονται με το φυτικό οξύ, σχηματίζουν αδιάλυτα ιζήματα τα οποία είναι πολύ λιγότερο απορροφήσιμα στα έντερα.[38][39]
Επειδή το φυτικό οξύ μπορεί επίσης να επηρεάσει την απορρόφηση του σιδήρου, «η αποφυτινοποίηση θα πρέπει να θεωρείται ως μια σημαντική στρατηγική για τη βελτίωση της διατροφής με σίδηρο κατά την περίοδο του απογαλακτισμού».[40] Η αποφυτινοποίηση από εξωγενή φυτάση σε τρόφιμα που περιέχουν ανιόντα φυτικού οξέος είναι μια προσέγγιση που διερευνάται για τη βελτίωση της διατροφικής υγείας σε πληθυσμούς που είναι ευάλωτοι σε ανεπάρκεια μετάλλων λόγω της εξάρτησής τους από τα βασικά τρόφιμα με φυτικά.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ «Food-Info.net : Τι είναι το φυτικό οξύ;». Food-Info. 26 Ιουλίου 2001. Ανακτήθηκε στις 3 Μαΐου 2022.
- ↑ 2,0 2,1 2,2 Schlemmer, U.; Frølich, W.; Prieto, R. M.; Grases, F. (2009). «Phytate in foods and significance for humans: Food sources, intake, processing, bioavailability, protective role and analysis». Molecular Nutrition & Food Research 53 Suppl 2: S330–75. doi:. PMID 19774556. https://wiebaktmee.nl/cms/pdf/Schlemmer%20_Mol_Nutr_Food_res_2009_Phytate_in_foods_and_significance_for_humans.pdf.
- ↑ Mullaney, Edward J.· Ullah, Abul H.J. «Phytases: attributes, catalytic mechanisms, and applications» (PDF). United States Department of Agriculture–Agricultural Research Service. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 7 Νοεμβρίου 2012. Ανακτήθηκε στις 18 Μαΐου 2012.
- ↑ 4,0 4,1 Klopfenstein, Terry J.; Angel, Rosalina; Cromwell, Gary; Erickson, Galen E.; Fox, Danny G.; Parsons, Carl; Satter, Larry D.; Sutton, Alan L. και άλλοι. (July 2002). «Animal Diet Modification to Decrease the Potential for Nitrogen and Phosphorus Pollution». Council for Agricultural Science and Technology 21. http://digitalcommons.unl.edu/animalscifacpub/518/.
- ↑ «Growth and intestinal morphology in cobia (Rachycentron canadum) fed extruded diets with two types of soybean meal partly replacing fish meal». Aquaculture Nutrition 14 (2): 174–180. 2008. doi:.
- ↑ Jezierny, D.; Mosenthin, R.; Weiss, E. (2010-05-01). «The use of grain legumes as a protein source in pig nutrition: A review». Animal Feed Science and Technology 157 (3–4): 111–128. doi:. https://www.researchgate.net/publication/248333607.
- ↑ «Industrialized Animal Production—A Major Source of Nutrient and Microbial Pollution to Aquatic Ecosystems». Population and Environment 24 (5): 369–385. 2003. doi:.
- ↑ Malleshi, N. G.; Desikachar, H. S. R. (1986). «Nutritive value of malted millet flours». Plant Foods for Human Nutrition 36 (3): 191–6. doi:.
- ↑ «Milling and Baking Quality of Low Phytic Acid Wheat». Crop Science 46 (6): 2403–8. 2006. doi:. https://semanticscholar.org/paper/b3418b51c19d0fb6e81bb745781126194d604b25.
- ↑ Shitan, Nobukazu; Yazaki, Kazufumi (2013-01-01), Jeon, Kwang W., επιμ., «Chapter Nine - New Insights into the Transport Mechanisms in Plant Vacuoles», International Review of Cell and Molecular Biology (Academic Press) 305: 383–433, doi:, PMID 23890387, http://www.sciencedirect.com/science/article/pii/B9780124076952000093, ανακτήθηκε στις 2020-04-24
- ↑ «In situ treatment of metals in contaminated soils with phytate». Journal of Environmental Quality 32 (1): 153–61. 2003. doi:. PMID 12549554.
- ↑ «Phytates in legumes and cereals». Advances in Food Research Volume 28. 28. 1982. σελίδες 1–92. ISBN 9780120164288.
- ↑ «Observation of inositol pentakis- and hexakis-phosphates in mammalian tissues by 31P NMR». Biochemical and Biophysical Research Communications 149 (3): 874–81. December 1987. doi:. PMID 3426614.
- ↑ «Metabolism and biological activities of inositol pentakisphosphate and inositol hexakisphosphate». Biochemical Pharmacology 50 (2): 137–46. July 1995. doi:. PMID 7543266.
- ↑ 15,0 15,1 «Binding of inositol phosphate to DNA-PK and stimulation of double-strand break repair». Cell 102 (6): 721–9. September 2000. doi:. PMID 11030616.
- ↑ «Inositol hexakisphosphate binds to clathrin assembly protein 3 (AP-3/AP180) and inhibits clathrin cage assembly in vitro». The Journal of Biological Chemistry 270 (1): 214–7. January 1995. doi:. PMID 7814377.
- ↑ «A phospholipase C-dependent inositol polyphosphate kinase pathway required for efficient messenger RNA export». Science 285 (5424): 96–100. July 1999. doi:. PMID 10390371.
- ↑ «Assessing the omnipotence of inositol hexakisphosphate». Cellular Signalling 13 (3): 151–8. March 2001. doi:. PMID 11282453. https://zenodo.org/record/1260121.
- ↑ «Inositol phosphates are assembly co-factors for HIV-1». Nature 560 (7719): 509–512. August 2018. doi:. PMID 30069050. Bibcode: 2018Natur.560..509D.
- ↑ Nassar, Mohannad; Nassar, Rania; Maki, Husain; Al-Yagoob, Abdullah; Hachim, Mahmood; Senok, Abiola; Williams, David; Hiraishi, Noriko (2021). «Phytic Acid: Properties and Potential Applications in Dentistry». Frontiers in Materials 8: 29. doi:. Bibcode: 2021FrMat...8...29N.
- ↑ «Phytic Acid: Properties and Potential Applications in Dentistry». Frontiers in Materials 8: 29. March 2021. doi:. Bibcode: 2021FrMat...8...29N.
- ↑ Nassar, Rania; Nassar, Mohannad; Vianna, Morgana E.; Naidoo, Nerissa; Alqutami, Fatma; Kaklamanos, Eleftherios G.; Senok, Abiola; Williams, David (2021). «Antimicrobial Activity of Phytic Acid: An Emerging Agent in Endodontics». Frontiers in Cellular and Infection Microbiology 11: 753649. doi:. ISSN 2235-2988. PMID 34765567.
- ↑ 23,0 23,1 Ellison, Campbell; Moreno, Teresa; Catchpole, Owen; Fenton, Tina; Lagutin, Kirill; MacKenzie, Andrew; Mitchell, Kevin; Scott, Dawn (2021-07-01). «Extraction of hemp seed using near-critical CO2, propane and dimethyl ether» (στα αγγλικά). The Journal of Supercritical Fluids 173: 105218. doi:. ISSN 0896-8446. https://www.sciencedirect.com/science/article/pii/S0896844621000577.
- ↑ "Phytates in cereals and legumes" Αρχειοθετήθηκε 2018-09-15 στο Wayback Machine.. fao.org.
- ↑ 25,0 25,1 «Degradation of phytate in foods by phytases in fruit and vegetable extracts.». Journal of Food Science 66 (4): 535–539. May 2001. doi:. https://archive.org/details/sim_journal-of-food-science_2001-05_66_4/page/535.
- ↑ Functional Food - Improve Health through Adequate Food edited by María Chávarri Hueda, pg. 86
- ↑ «Wise Eating, Made Easy». Αρχειοθετήθηκε από το πρωτότυπο στις 30 Σεπτεμβρίου 2022. Ανακτήθηκε στις 3 Μαΐου 2022.
- ↑ Dephytinisation with Intrinsic Wheat Phytase and Iron Fortification Significantly Increase Iron Absorption from Fonio (Digitaria exilis) Meals in West African Women (2013)
- ↑ Reddy, N. R.· Sathe, Shridhar K. (2001). Food Phytates. Boca Raton: CRC. ISBN 978-1-56676-867-2. Unknown parameter
|name-list-style=ignored (βοήθεια)[Χρειάζεται σελίδα] - ↑ «Ion chromatography of phytate in roots and tubers». Journal of Agricultural and Food Chemistry 51 (2): 350–3. January 2003. doi:. PMID 12517094.
- ↑ «Inhibitory effect of nuts on iron absorption». The American Journal of Clinical Nutrition 47 (2): 270–4. February 1988. doi:. PMID 3341259. https://archive.org/details/sim_american-journal-of-clinical-nutrition_1988-02_47_2/page/270.
- ↑ «Relationship of components in wheat bran and spinach to iron bioavailability in the anemic rat». The Journal of Nutrition 114 (3): 526–35. March 1984. doi:. PMID 6321704. https://archive.org/details/sim_journal-of-nutrition_1984-03_114_3/page/526.
- ↑ Arendt, Elke K· Zannini, Emanuele (9 Απριλίου 2013). «Chapter 11: Buckwheat». Cereal grains for the food and beverage industries. Woodhead Publishing. σελ. 388. ISBN 978-0-85709-892-4. Unknown parameter
|name-list-style=ignored (βοήθεια) - ↑ Pereira Da Silva B. Concentration of nutrients and bioactive compounds in chia (Salvia Hispanica L.), protein quality and iron bioavailability in wistar rats (Διδακτορική διατριβή). Federal University of Viçosa.
- ↑ Scuhlz, Markus. «Paleo Diet Guide: With Recipes in 30 Minutes or Less: Diabetes Heart Disease: Paleo Diet Friendly: Dairy Gluten Nut Soy Free Cookbook». PWPH Publications – μέσω Google Books. Unknown parameter
|name-list-style=ignored (βοήθεια) - ↑ Gupta, R. K.; Gangoliya, S. S.; Singh, N. K. (2013). «Reduction of phytic acid and enhancement of bioavailable micronutrients in food grains». Journal of Food Science and Technology 52 (2): 676–684. doi:. PMID 25694676.
- ↑ «Iron (Fe) bioavailability and the distribution of anti-Fe nutrition biochemicals in the unpolished, polished grain and bran fraction of five rice genotypes». Journal of the Science of Food and Agriculture 86 (8): 1209–15. 2006. doi:. Αρχειοθετήθηκε από το πρωτότυπο στις 2020-02-23. https://web.archive.org/web/20200223165420/https://naldc-legacy.nal.usda.gov/naldc/download.xhtml?id=19315&content=PDF. Ανακτήθηκε στις 2022-05-03.
- ↑ «Influence of vegetable protein sources on trace element and mineral bioavailability». The Journal of Nutrition 133 (9): 2973S–7S. September 2003. doi:. PMID 12949395.
- ↑ Committee on Food Protection· Food and Nutrition Board (1973). «Phytates». Toxicants Occurring Naturally in Foods. National Academy of Sciences. σελίδες 363–371. ISBN 978-0-309-02117-3.
- ↑ «Degradation of phytic acid in cereal porridges improves iron absorption by human subjects». The American Journal of Clinical Nutrition 77 (5): 1213–9. May 2003. doi:. PMID 12716674. https://archive.org/details/sim_american-journal-of-clinical-nutrition_2003-05_77_5/page/1213.
