Λεβισίτης
| Λεβισίτης | |||
|---|---|---|---|

| |||
| |||

| |||
| Γενικά | |||
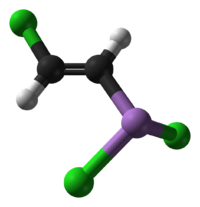
| Όνομα IUPAC | Διχλωρο[(Ε)-2-χλωροβινυλ]αρσάνη | ||
| Άλλες ονομασίες | L, λεβισίτης Α, λεβισίτης 1, β-χλωροβινυλοδιχλωροαρσίνη | ||
| Χημικά αναγνωριστικά | |||
| Μοριακή μάζα | 207.31788 g/mol | ||
| Αριθμός CAS | 541-25-3 | ||
| SMILES | C(=C[As](Cl)Cl)Cl | ||
| InChI | 1S/C2H2AsCl3/c4-2-1-3(5)6/h1-2H/b2-1+ | ||
| Αριθμός EINECS | 232-059-5 | ||
| Αριθμός RTECS | (Δεν έχει δημιουργηθεί) | ||
| Αριθμός UN | 1556 | ||
| PubChem CID | 5372798 | ||
| ChemSpider ID | 4522971 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -18 °C | ||
| Σημείο βρασμού | 203 °C (σε 760 mmHg) | ||
| Πυκνότητα | 1,89 g/cm3 (στους 20 °C) | ||
| Διαλυτότητα στο νερό |
0,5 g/L | ||
| Διαλυτότητα σε άλλους διαλύτες |
Ευδιάλυτο σε οργανικούς διαλύτες, έλαια και λίπη | ||
| Εμφάνιση | Άχρωμο ή ανοιχτό καστανοκίτρινο ελαιώδες υγρό με οσμή φρεσκοκομμένων γερανιών | ||
| Χημικές ιδιότητες | |||
| Ελάχιστη θερμοκρασία ανάφλεξης |
84,4 °C | ||
| Επικινδυνότητα | |||
  
| |||
| Τοξικό (Τ+) Ρυπογόνο (Ν) Ερεθιστικό (Χi) | |||
| Φράσεις κινδύνου | 23/25-50/53 | ||
| Φράσεις ασφαλείας | (1/2)-20/21-28-45-60-61 | ||
| Κίνδυνοι κατά NFPA 704 |
|||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Ο λεβισίτης (παλιότερα λεβιζίτις, η, αγγλ. "Lewisite"), είναι ένα χημικό όπλο, το οποίο λόγω της ιδιότητάς του να δημιουργεί εγκαύματα στο δέρμα και να προσβάλλει το αναπνευστικό σύστημα, ταξινομείται ως καυστική ουσία (αγγλ. blister agent). Η χρήση της ουσίας για στρατιωτικούς σκοπούς έχει σταματήσει εδώ και μισό αιώνα.
Συγγενείς ουσίες[Επεξεργασία | επεξεργασία κώδικα]
Με τον όρο "λεβισίτης" εννοείται η ουσία με χημικό τύπο C2H2AsCl3 (Λεβισίτης Α). Υπάρχουν δύο χημικές ουσίες που έχουν παρόμοια χημική δομή με αυτή του λεβισίτη Α:
-
Λεβισίτης Β (C4H4AsCl3)
(2,2’-διχλωροδιβινυλαρσινοχλωρίδιο) -
Λεβισίτης Γ (C6H6AsCl3)
(1,1’,1’-τριχλωροτριβυνιλαρσίνη)
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Ο λεβισίτης και οι συγγενείς με αυτόν αρσίνες (λεβισίτες Β και Γ) είχαν μελετηθεί λεπτομερώς από Γερμανούς επιστήμονες κατά τη διάρκεια του Α’ Παγκοσμίου Πολέμου πριν τους ανακαλύψουν στις ΗΠΑ. Μάλιστα, οι Γερμανοί επιστήμονες Τίλε (J. Thiele), Βίλαντ (H. Wieland) και Μπλέμερ (A. Blömer) δημοσίευσαν σχετικές εργασίες, παραδόξως όμως δεν εισηγήθηκαν τη χρήση του λεβισίτη ως χημικού όπλου.[1]
Το 1918, στο Καθολικό Πανεπιστήμιο της Ουάσινγκτον, ο Αμερικανός πλοίαρχος Ουίνφορντ Λι Λιούις (Winford Lee Lewis) ανακάλυψε και αυτός τον λεβισίτη, βασιζόμενος σε προγενέστερα πειράματα του χημικού Άρθουρ Νιούλαντ (Julius Arthur Nieuwland) αυτή τη φορά όμως η ουσία τράβηξε το ενδιαφέρον του Στρατού.[2] Οι Αμερικανοί άρχισαν να παρασκευάζουν, κάτω από συνθήκες άκρας μυστικότητας, μεγάλες ποσότητες λεβισίτη με τα κωδικά στοιχεία “νέο G-34”, για να τις χρησιμοποιήσουν κατά των Γερμανών στην Ευρώπη. Μάλιστα, το δόγμα χρήσης του λεβισίτη προέβλεπε τον ψεκασμό του αντιπάλου από ειδικά διαμορφωμένα αεροπλάνα. Αυτή την εποχή, ο στρατηγός Έιμος Άλφρεντ Φράιζ (Amos Alfred Fries) έδωσε στην ουσία το όνομα «Δρόσος του Θανάτου» (Dew of Death).[1] Τελικά το Νοέμβρη του 1918, οι Αμερικανοί αποφάσισαν να στείλουν με πλοία 150 τόνους λεβισίτη στην Ευρώπη. Ωστόσο, δεν πρόλαβαν να τον χρησιμοποιήσουν, διότι η Γερμανία συνήψε ανακωχή με τις δυνάμεις της Αντάντ ενώ το φορτίο με τον λεβισίτη ήταν ακόμα εν πλω.[3]
Ο Μπενίτο Μουσολίνι χρησιμοποίησε λεβισίτη και αέριο μουστάρδας κατά την «ηρωική» εκστρατεία του στην Αβησσυνία, το 1935, παρά το ότι η χώρα του δεσμευόταν από το Πρωτόκολλο της Γενεύης, το οποίο απαγόρευε τη χρήση χημικών όπλων. Οι Ιταλοί έκαναν χρήση λεβισίτη τόσο εναντίον στρατιωτών, οι οποίοι στερούνταν τα στοιχειώδη μέτρα προστασίας, όσο και εναντίον αμάχων. Όπως ήταν επόμενο, το έγκλημα αυτό προκάλεσε διεθνή κατακραυγή, ιδιαίτερα από τη Μεγάλη Βρετανία και φυσικά από τον Χαϊλέ Σελασιέ Α'.[4]
Κατά το Μεσοπόλεμο, πολλές χώρες ασχολήθηκαν με την παραγωγή του λεβισίτη, όπως οι ΗΠΑ, η Μεγάλη Βρετανία, η Γαλλία, η Σοβιετική Ένωση, η Ιταλία και η Ιαπωνία.[5]
Η Ιαπωνία ήταν η μόνη χώρα που χρησιμοποίησε λεβισίτη κατά τον Δεύτερο Παγκόσμιο Πόλεμο εναντίον των Κινέζων στη Μαντζουρία. Μάλιστα, οι Ιάπωνες, μετά την αποχώρησή τους από την Κίνα, το 1945, κατέστρεψαν τα εκεί αποθέματά τους σε χημικά όπλα, ωστόσο εγκαταλειμμένα όπλα με χημική γόμωση προκαλούν ατυχήματα ακόμη και σήμερα σε ανυποψίαστους Κινέζους.[6]
Μετά τον πόλεμο, οι Αμερικανοί άρχισαν να ενδιαφέρονται περισσότερο για τον λεβισίτη, λόγω του ότι δεν ήταν εύφλεκτος και επειδή, λόγω του χαμηλού σημείου τήξης και της αντοχής του σε χαμηλές και υψηλές θερμοκρασίες, κάτι που έκανε την ουσία κατάλληλη για χρήση σε περιοχές με ακραίες συνθήκες (Βόρειος Πόλος, τροπικές περιοχές), αλλά και την ικανότητά του να διαπερνά το ελαστικό. Εκείνη την εποχή, το κωδικό όνομα του λεβισίτη άλλαξε από Μ1 σε L. Μίγματα αερίου μουστάρδας και λεβισίτη (HL) παρασκευάστηκαν επίσης, προκειμένου να μειωθεί το σημείο τήξης του αερίου μουστάρδας, για χρήση σε περιοχές με ψυχρό κλίμα.[7] Ωστόσο, δοκιμές που πραγματοποιούνταν ήδη από το Μεσοπόλεμο [1] απέδειξαν ότι ο λεβισίτης σε συνθήκες μάχης έχει μάλλον μειωμένα αποτελέσματα επί του αντιπάλου, συν του ότι γίνεται εύκολα αντιληπτός (λειτουργεί ως δακρυγόνο και η έντονη μυρωδιά γερανιού είναι αναγνωρίσιμα χαρακτηριστικά), ενώ είναι χημικά ευπαθής στην υγρασία. Οι ΗΠΑ κατασκεύασαν 20.000 περίπου τόνους λεβισίτη. Τελικά όμως, η εμφάνιση στο προσκήνιο των άχρωμων και άοσμων παραγόντων νεύρων, των οποίων μία σταγόνα είναι υπεραρκετή για να προκαλέσει τον θάνατο, και ειδικά του VX, το 1952, κατέστησε τον λεβισίτη ξεπερασμένο σαν χημικό όπλο. Εν τέλει, τα αμερικανικά αποθέματα λεβισίτη εξουδετερώθηκαν με χλωρίνη και ρίχτηκαν στον Κόλπο του Μεξικού.[8]
Χημικά χαρακτηριστικά[Επεξεργασία | επεξεργασία κώδικα]
Ο λεβισίτης σε καθαρή κατάσταση είναι ένα άχρωμο, ελαιώδες υγρό με έντονη οσμή φρεσκοκομμένων γερανιών, το οποίο όταν εκτίθεται στον ατμοσφαιρικό αέρα παίρνει γρήγορα μία καστανοκίτρινη χροιά.
Παράγεται με την αντίδραση ασετυλίνης (C2H2) και τριχλωριούχου αρσενικού (AsCl3), παρουσία χλωριούχου αργιλίου (AlCl3) ή διαλύματος διχλωριούχου υδραργύρου (HgCl2) σε υδροχλωρικό οξύ (HCl), ουσίες οι οποίες λειτουργούν ως καταλύτες:
Πρακτικά ωστόσο, το προϊόν της αντίδρασης δεν είναι καθαρός λεβισίτης, αλλά μίγμα λεβισιτών Α, Β και Γ, οι οποίοι προκύπτουν ταυτόχρονα, σύμφωνα με τις αντιδράσεις:
(Λεβισίτης Β)
(Λεβισίτης Γ)
Το μίγμα που προκύπτει υποβάλλεται σε κλασματική απόσταξη, όπου ο λεβισίτης Α, ως λιγότερο πτητικός, εξατμίζεται τελευταίος (ο λεβισίτης Β έχει σημείο ζέσης 130 °C και ο λεβισίτης Γ 151 °C). Επιπλέον, οι λεβισίτες Β και Γ μπορούν και αυτοί με τη σειρά τους να μετατραπούν εύκολα σε λεβισίτη Α με την αντίδρασή τους με τριχλωριούχο αρσενικό σε θερμοκρασία 200 – 250 °C:
Ο λεβισίτης, όπως και οι περισσότερες χλωροαρσίνες, υδρολύεται ταχέως σε ακίνδυνο οξείδιο με την παρουσία νερού ή υγρασίας:
Ο λεβισίτης είναι επίσης δυνατό να εξουδετερωθεί με αλκαλικά διαλύματα όπως διάλυμα υδροξειδίου του νατρίου (NaOH), οπότε εκλύεται ασετυλίνη και παράγεται το δηλητηριώδες, αλλά μη πτητικό, αρσενικώδες νάτριο:[1]
Δράση, συμπτώματα και αντιμετώπιση[Επεξεργασία | επεξεργασία κώδικα]

Ο λεβισίτης, ως χημικό όπλο, έχει παρόμοια χαρακτηριστικά με το αέριο μουστάρδας. Επιπλέον όμως, έχει τη δυνατότητα να διαπερνά τα ρούχα και ορισμένα είδη ελαστικού.[5] Οι ατμοί του, επτά φορές βαρύτεροι απ’ τον αέρα, κυλούν από τα ψηλά στα χαμηλά μέρη και προσβάλλουν τους βλεννογόνους αδένες, (και γενικότερα τους ιστούς του σώματος) προκαλώντας τσούξιμο σε μάτια και μύτη.[1] Αν η ουσία έρθει σε επαφή με τα μάτια, μπορεί να προκαλέσει τύφλωση. Άμεσος θάνατος προέρχεται από πνευμονικό οίδημα ή ασφυξία, αν ο λεβισίτης προσβάλλει το αναπνευστικό σύστημα και τους πνεύμονες, οι οποίοι τότε γεμίζουν με αίμα, βλέννα και νεκρούς ιστούς.[9] Η κατάποση λεβισίτη προκαλέι έντονο πόνο, βήχα, ναυτία και εμετό.[10]
Επίσης, αν ο λεβισίτης έρθει σε επαφή με το δέρμα, προκαλεί αρχικά κνησμό και λίγο αργότερα (σε περίπου 12 ώρες από την επαφή) μεγάλες φλύκταινες, οι οποίες συνοδεύονται από φρικτούς πόνους, αλλά σε αντίθεση με το αέριο της μουστάρδας δεν προκαλεί μακροχρόνιες μολύνσεις.[1] Δύο κυβικά εκατοστά λεβισίτη είναι αρκετά για να προκαλέσουν το θάνατο σε έναν ενήλικα εντός δέκα λεπτών, αν απορροφηθούν.[9]
Μακροπρόθεσμα, ο λεβισίτης προκαλεί χρόνιο πνευμονικό οίδημα, υποθερμίες, χαμηλή πίεση, ζημιές στο ενδοκρινολογικό σύστημα και συστηματική καταστροφή του ήπατος, ενώ είναι δυνατό να προκληθούν διαταραχές στο νευρικό σύστημα του θύματος και να το οδηγήσουν στην αυτοκτονία.[11]
Η δηλητηρίαση από λεβισίτη αντιμετωπίζεται αποτελεσματικά με τον "Βρετανικό αντι-λεβισίτη" ή BAL (British Anti-Lewisite) (διμερκαπρόλη).[12]
Βιβλιογραφία[Επεξεργασία | επεξεργασία κώδικα]
- Γεώργιος Ε. Μανουσάκης, "Χημικός και Βιολογικός Πόλεμος. Από τις Πλαταιές στο Τόκιο και τη Βαγδάτη", εκδόσεις Πατάκη
- Παύλου Δρανδάκη, "Μεγάλη Ελληνική Εγκυκλοπαίδεια", λήμμα "Λεβιζίται"
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Δρανδάκης, ό.π, σ. 877
- ↑ Μανουσάκης, ό.π., σ. 72 – 73
- ↑ Μανουσάκης, ό.π., σ. 74 - 75
- ↑ Μανουσάκης, ό.π., σ. 86 - 88
- ↑ 5,0 5,1 Μανουσάκης, ό.π., σ. 74
- ↑ Μανουσάκης, ό.π., σ. 106 – 109
- ↑ Μανουσάκης, ό.π., σ. 302
- ↑ Code Red - Weapons of Mass Destruction [Online Resource] - Blister Agents
- ↑ 9,0 9,1 Μανουσάκης, ό.π., σ. 301
- ↑ Committee on Review and Evaluation of the Army Non-Stockpile Chemical Materiel Disposal Program, U.S. National Research Council. Disposal of Chemical Agent Identification Sets, (Google Books), p. 16, National Academies Press, 1999, (ISBN 0309068797).
- ↑ Μανουσάκης, ό.π., σ. 301 – 302 και 73
- ↑ Domingo Tabangcura, Jr., G. Patrick Daubert. «British anti-Lewisite».
| |||||||||||||||||||||||||




![{\displaystyle \mathrm {AsCl_{3}+HC\equiv CH{\xrightarrow[{HCl}]{HgCl_{2}}}ClHC=CH-AsCl_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ecf9f3f4374b8c34db049169313117ab0f51ff22)
![{\displaystyle \mathrm {AsCl_{3}+2HC\equiv CH{\xrightarrow[{HCl}]{HgCl_{2}}}(ClHC=CH)_{2}AsCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/077d65d0b1717475c46427e449c08d12c8658a21)
![{\displaystyle \mathrm {AsCl_{3}+3HC\equiv CH{\xrightarrow[{HCl}]{HgCl_{2}}}(ClHC=CH)_{3}As} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7704f3df8b6b7569f6dbd225b20cac75fd84b6bc)