Ιός Ρότα
| Ιός Ρότα | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
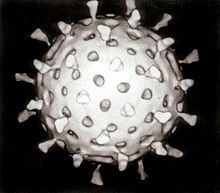
 Ηλεκτρονική μικρογραφία του ιού Ρότα. The bar = 100 nm
| ||||||||||
| Ταξινόμηση ιού | ||||||||||
| ||||||||||
| Τυπικό είδος | ||||||||||
| Rotavirus A | ||||||||||
| Species | ||||||||||
|
Rotavirus A | ||||||||||
Ο Ιός Ρότα είναι η πιο κοινή αιτία της σοβαρής διάρροιας μεταξύ βρεφών και μικρών παιδιών,[1] και είναι ένας από τους πολλούς ιούς που προκαλούν λοιμώξεις που συχνά ονομάζονται στομαχικές διαταραχές, παρά το γεγονός ότι δεν έχουν σχέση με τη γρίπη. Πρόκειται για ένα γένος δίκλωνου RNA ιού της οικογένειας Reoviridae. Στην ηλικία των πέντε ετών, σχεδόν κάθε παιδί στον κόσμο μολύνεται με τον Ιό Ρότα τουλάχιστον μια φορά.[2] Παρόλα αυτά, με κάθε μόλυνση, αναπτύσσεται ανοσία, και τα συμπτώματα από επακόλουθη λοίμωξη είναι λιγότερο σοβαρά.[3] Οι ενήλικες σπάνια μολύνονται.[4] Υπάρχουν πέντε είδη του ιού αυτού, που αναφέρονται ως A, B, C, D, και E είδος.[5] Ο ιός Ρότα τύπου A, που είναι ο πιο κοινός, είναι υπεύθυνος για περισσότερο από το 90% των λοιμώξεων στον άνθρωπο.
Ο ιός μεταδίδεται από κόπρανα της γαστρεντερικής οδού. Μολύνει και καταστρέφει τα κύτταρα τα οποία δομούν το λεπτό έντερο και προκαλεί γαστρεντερίτιδα. Παρά το γεγονός ότι ο ιός Ρότα ανακαλύφθηκε το 1973[6] και αναλογεί στο 50% των νοσηλειών σοβαρής διάρροιας σε βρέφη και παιδιά,[7] η σημασία του δεν είναι ακόμα ευρέως γνωστή στη κοινότητα της δημόσιας υγείας, ιδίως στις αναπτυσσόμενες χώρες.[8] Εκτός από τις επιπτώσεις του στον άνθρωπο, ο ιός Ρότα μολύνει και ζώα, και είναι ιδιαίτερα παθογόνο και επιβλαβές στην κτηνοτροφία.[9]
Η αντιμετώπιση των ασθενών με ιό Ρότα είναι συνήθως εύκολη, αλλά σε όλο τον κόσμο σχεδόν 500.000 παιδιά κάτω των πέντε ετών εξακολουθούν να πεθαίνουν από λοίμωξη από τον ιό Ρότα[10] και σχεδόν 2 εκατομμύρια είναι σε σοβαρή κατάσταση.[8] Στις Ηνωμένες Πολιτείες, πριν από την έναρξη του προγράμματος εμβολιασμού, ο ιός Ρότα προκαλούσε περίπου 2.7 εκατομμύρια περιπτώσεις σοβαρής γαστρεντερίτιδας σε παιδιά, σχεδόν 60,000 νοσηλείες, και περίπου 37 θανάτους κάθε χρόνο.[11] Εκστρατείες της δημόσιας υγείας εναντίον του ιού Ρότα εστίασαν στη θεραπεία ενυδάτωσης από το στόμα για μολυσμένα παιδιά και στον εμβολιασμό για την πρόληψη της νόσου.[12]
Ιστορία[Επεξεργασία | επεξεργασία κώδικα]
Το 1943, ο Jacob Light και ο Horace Hodes απέδειξαν ότι ένας παράγοντας φιλτραρίσματος στα κόπρανα των παιδιών με σοβαρή διάρροια προκαλεί επίσης διάρροια (σοβαρή διάρροια στα ζώα) στα βοοειδή.[13] Τρεις δεκαετίες αργότερα, σε διατηρημένα δείγματα αντιπροσώπου αποδείχτηκε ότι υπήρχε ο ιός Ρότα.[14] Στα χρόνια που μεσολάβησαν ένας ιός, που βρέθηκε στα ποντίκια.[15] έμοιαζε στον ιό Ρότα.[16] Το 1973,ο επίσκοπος Ruth και οι συνεργάτες του περιέγραψαν συγγενή είδη του ιού που βρέθηκαν σε παιδιά με γαστρεντερίτιδα.[6][17]
Το 1974, ο Thomas Henry Flewett πρότεινε το όνομα ιός Ρότα αφού παρατήρησε ότι, κατά τη μελέτη σε ηλεκτρονικό μικροσκόπιο, το σωματίδιο του ιού μοιάζει με ρόδα (rota στα λατινικά).[18][19] Το όνομα αναγνωρίστηκε επίσημα από τη Διεθνή Επιτροπή Ταξινόμησης των Ιών τέσσερα χρόνια αργότερα.[20] Το 1976, συγγενή είδη περιγράφηκαν σε πολλά άλλα είδη ζώων.[16] Αυτοί οι ιοί, όλοι προκαλούν οξεία γαστρεντερίτιδα, και αναγνωρίστηκαν ως ένας συλλογικός παθογόνος παράγοντας που προσβάλλει τους ανθρώπους και τα ζώα σε παγκόσμιο επίπεδο.[18] Οι ορότυποι του ιού περιγράφηκαν πρώτη φορά το 1980,[21] και την επόμενη χρονιά, ο ιός Ρότα που απομονώθηκε από τον άνθρωπο αναπτύχθηκε σε καλλιέργειες κυττάρων προερχόμενες από νεφρά πιθήκου, με την προσθήκη θρυψίνης (ενός ενζύμου που βρίσκεται στο δωδεκαδάκτυλο των θηλαστικών και τώρα είναι γνωστό ότι είναι απαραίτητο για την αναπαραγωγή του ιού Ρότα) στο μέσο της καλλιέργειας.[22] Η ικανότητα να αναπτύσσεται ο ιός Ρότα στην καλλιέργεια επιτάχυνε τον ρυθμό της έρευνας, και από τα μέσα της δεκαετίας του 1980 τα πρώτα υποψήφια εμβόλια ήταν στο στάδιο της αξιολόγησης.[23] Το 1998, ένα εμβόλιο για τον ιό Ρότα πήρε την άδεια να χρησιμοποιείται στις ΗΠΑ. κλινικές δοκιμές στις ΗΠΑ, στη Φινλανδία, και τη Βενεζουέλα απέδειξαν ότι είναι 80 έως 100% αποτελεσματικό στην πρόληψη της σοβαρής διάρροιας που προκαλείται από τον ιό Ρότα A, και ερευνητές δεν διαπίστωσαν με σημαντικές στατιστικές σοβαρές ανεπιθύμητες ενέργειες.[24][25] Ο κατασκευαστής, ωστόσο, το απέσυρε από την κυκλοφορία το 1999, αφού διαπίστωσε ότι το εμβόλιο μπορεί να προκαλέσει αυξημένο εγκολεασμό, ένα είδος εντερικής απόφραξης, σε ένα από τα 12,000 εμβολιασμένα βρέφη.[26] Η πρακτική προκάλεσε έντονη συζήτηση σχετικά με τους κινδύνους και τα οφέλη από το εμβόλιο για τον ιό Ρότα.[27] Το 2006, δύο νέα εμβόλια κατά της μόλυνσης από τον ιό Ρότα A αποδείχθηκαν ότι είναι ασφαλή και αποτελεσματικά σε παιδιά,[28] και τον Ιούνιο του 2009 ο Παγκόσμιος Οργανισμός Υγείας συνέστησε ότι ο εμβολιασμός κατά του ιού Ρότα θα πρέπει να περιλαμβάνεται σε όλα τα εθνικά προγράμματα εμβολιασμού έτσι ώστε να παρέχεται προστασία έναντι του ιού.[29]
Σημεία και Συμπτώματα[Επεξεργασία | επεξεργασία κώδικα]
Η γαστρεντερίτιδα από ιό Ρότα είναι μία ήπια εώς σοβαρή ασθένεια που χαρακτηρίζεται από εμετό, υδαρή διάρροια, χαμηλό πυρετό. Όταν ένα παιδί προσβληθεί από τον ιό, υπάρχει μια περίοδος επώασης περίπου 2 μέρες πριν εμφανιστούν τα συμπτώματα.[30] Τα συμπτώματα ξεκινούν με εμετό ακολουθούμενο από τεσσάρων εώς πέντε ημερών ακατάσχετη διάρροια. Η αφυδάτωση είναι πιο κοινή σε λοίμωξη από ιό Ρότα από ότι σε λοιμώξεις που προκαλούνται από παθογόνα βακτήρια, και είναι η πιο κοινή αιτία θανάτου που σχετίζεται με λοίμωξη από ιό Ρότα.[31] Οι λοιμώξεις του ιού Ρότα A μπορούν να εμφανιστούν καθ' όλη τη διάρκεια της ζωής: η πρώτη συνήθως είναι συμπτωματική, αλλά οι επόμενες λοιμώξεις είναι συνήθως ασυμπτωματικές,[4] as the immune system provides some protection.[2] Κατά συνέπεια, στη συμπτωματική λοίμωξη τα ποσοστά είναι υψηλότερα σε παιδιά ηλικίας κάτω των δύο ετών και μειώνονται σταδιακά έως την ηλικία των 45 ετών.[32][33] Η λοίμωξη στα νεογνά, αν και συχνή, συνδέεται συνήθως με ήπια ή ασυμπτωματική νόσο,[34][35] Τα πιο σοβαρά συμπτώματα τείνουν να εμφανίζονται σε παιδιά ηλικίας 6 μηνών έως δύο ετών, σε ηλικιωμένους, και σε άτομα με μειωμένη ή πλήρη καταστολή του ανοσοποιητικού συστήματος. Λόγω της ανοσίας που απέκτησαν κατά την παιδική ηλικία, οι περισσότεροι ενήλικες δεν είναι ευπαθείς στον ιό Ρότα. Η γαστρεντερίτιδα στους ενήλικες συνήθως έχει άλλη αιτία εκτός από τον ιό Ρότα, αλλά οι ασυμπτωματικές λοιμώξεις στους ενήλικες μπορούν να διατηρήσουν τη μετάδοση της λοίμωξης στον πληθυσμό.[36] Η συμπτωματική εκ νέου μόλυνση προκαλείται συχνά λόγω ενός νέου ορότυπου του ιού Ρότα A.[3][37]
Μετάδοση[Επεξεργασία | επεξεργασία κώδικα]

Ο ιός Ρότα μεταδίδεται μέσω των περιττωμάτων της γαστρεντερικής οδού, μέσω της επαφής με μολυσμένα χέρια, επιφάνειες, και αντικείμενα [38] και ενδεχομένως από τη γαστρεντερική οδό.[1] Τα κόπρανα ενός μολυσμένου ατόμου μπορούν να περιέχουν περισσότερα από 10 τρισεκατομμύρια μολυσματικά σωματίδια ανά γραμμάριο,[4] μόνο 10-100 από αυτά απαιτούνται για τη μετάδοση της λοίμωξης σε άλλο άτομο.[39]
Ο ιός Ρότα είναι σταθερός στο περιβάλλον και έχουν βρεθεί στις εκβολές ποταμών δείγματα σε επίπεδα μέχρι και 1–5 μολυσματικά σωματίδια ανά γαλόνι νερού στις ΗΠΑ.[40] Υγειονομικά μέτρα για την εξάλειψη βακτηρίων και παρασίτων φαίνεται να είναι αναποτελεσματικά στον έλεγχο του ιού Ρότα, καθώς η συχνότητα της λοίμωξης από τον ιό Ρότα σε χώρες με υψηλά και χαμηλά πρότυπα υγείας είναι παρόμοια.[1]
Μηχανισμός της λοίμωξης[Επεξεργασία | επεξεργασία κώδικα]

Η διάρροια προκαλείται από πολλαπλούς μηχανισμούς του ιού. Η Δυσαπορρόφηση παρουσιάζεται εξαιτίας της καταστροφής των κυττάρων του εντέρου που ονομάζονται επιθηλιακά κύτταρα του εντέρου. Η τοξική πρωτεΐνη του ιού Ρότα NSP4 επάγει την εξαρτώμενη από την ηλικία και από τα ιόντα ασβεστίου χλωριούχο έκκριση, διαταράσσει τον SGLT1 μεταφορέα-μεσολαβητή της επαναρρόφησης ύδατος, προφανώς μειώνει τη δραστηριότητα των δισακχαριτών της λαχνωτής μεμβράνης, και πιθανώς ενεργοποιεί τα ιόντα ασβεστίου που εξαρτώνται από εκκριτικά αντανακλαστικά του εντερικού νευρικού συστήματος.[41][42] Υγιή επιθηλιακά κύτταρα του εντέρου εκκρίνουν λακτάση στο λεπτό έντερο. Δυσανεξία στο γάλα λόγω της λακτάσης είναι ένα συγκεκριμένο σύμπτωμα της λοίμωξης από τον ιό Ρότα,[43][44] το οποίο μπορεί να διαρκέσει για εβδομάδες.[45] Ένα επαναλαμβανόμενο επεισόδιο ήπιας διάρροιας συχνά ακολουθείται από την επανεισαγωγή του γάλακτος στη διατροφή του παιδιού, που οφείλεται σε βακτηριδιακή ζύμωση της δισακχαριτικής λακτόζης στο έντερο.[46]
Διάγνωση και Εντοπισμός[Επεξεργασία | επεξεργασία κώδικα]
Η διάγνωση της λοίμωξης από τον ιό Ρότα συνήθως ακολουθεί τη διάγνωση της γαστρεντερίτιδας και είναι αιτία σοβαρής διάρροιας. Τα περισσότερα παιδιά στο νοσοκομείο με γαστρεντερίτιδα έχουν δοκιμαστεί για τον ιό Ρότα A.[47][48] Η ειδική διάγνωση της λοίμωξης από τον ιό Ρότα A γίνεται με την εύρεση του ιού στα κόπρανα του παιδιού μέσω ανοσοενζυμικής μεθόδου. Υπάρχουν πολλά τεστ που έχουν αδειοδοτηθεί στην αγορά τα οποία είναι ευαίσθητα, ειδικά και εντοπίζουν όλους τους ορότυπους του ιού Ρότα A.[49][50] Άλλες μέθοδοι, ηλεκτρονική μικροσκόπιση και ηλεκτροφόρηση σε πηκτή πολυακρυλαμιδίου, χρησιμοποιήθηκαν σε ερευνητικά εργαστήρια.[51] Η αντίστροφη μεταγραφή αλυσιδωτής αντίδρασης πολυμεράσης (RT-PCR) μπορεί να ανιχνεύσει και να εντοπίσει όλα τα είδη και τους ορότυπους του ανθρώπινου ιού Ρότα.[52]
Θεραπεία και Πρόγνωση[Επεξεργασία | επεξεργασία κώδικα]
Η θεραπεία της οξείας λοίμωξης από ιό Ρότα είναι μη ειδική και περιλαμβάνει το διαχωρισμό των συμπτωμάτων και, το πιο σημαντικό, την προστασία από την αφυδάτωση.[12] Εάν δεν αντιμετωπιστεί, τα παιδιά μπορεί να πεθάνουν από την προκύπτουσα σοβαρή αφυδάτωση.[53] Ανάλογα με τη σοβαρότητα της διάρροιας, η θεραπεία περιλαμβάνει ενυδάτωση από το στόμα, κατά την οποία δίνεται στο παιδί επιπλέον νερό το οποίο περιέχει μικρές ποσότητες αλατιού και ζάχαρης.[54] Ορισμένες λοιμώξεις είναι αρκετά σοβαρές ώστε να δικαιολογούν νοσηλεία όπου δίνονται υγρά ενδοφλεβίως ή με ρινογαστρικό σωλήνα. Οι ηλεκτρολύτες και η τιμή του σακχάρου στο αίμα ελέγχονται.[47]
Οι λοιμώξεις από ιους Ρότα σπάνια προκαλούν άλλες επιπλοκές και με μια καλή διαχείριση το παιδί έχει καλή πρόγνωση.[55][56] Υπάρχουν σπάνιες αναφορές των επιπλοκών που περιλαμβάνουν το κεντρικό νευρικό σύστημα (CNS) όπου ο ιός Ρότα εντοπίστηκε στο υγρό του ΚΝΣ σε περιπτώσεις εγκεφαλίτιδας και μηνιγγίτιδας,[57][58][59] Πρόσφατές μελέτες έχουν επιβεβαιώσει ότι η λοίμωξη από τον ιο Ρότα δεν περιορίζεται πάντα στο έντερο αλλά μπορεί να προκαλέσει ιαιμία.[60]
Επιδημιολογία[Επεξεργασία | επεξεργασία κώδικα]

Ο ιός Ρότα είναι υπεύθυνος για το περισσότερο από το 90% της γαστρεντερίτιδας στον άνθρωπο,[61] και είναι ενδημικός σε όλο τον κόσμο. Κάθε χρόνο ο ιός Ρότα προκαλεί εκατομμύρια κρούσματα διάρροιας σε αναπτυσσόμενες χώρες. Σχεδόν 2 εκατομμύρια νοσηλεύτηκαν [8] και αναφέρθηκαν 453.000 θάνατοι παιδιών κάτω των πέντε χρονών.[10] Στις Ηνωμένες Πολιτείες πριν από την έναρξη του εμβολιασμού για τον ιό Ρότα [62]—πάνω από 2.7 εκατομμύριες περιπτώσεις γαστρεντερίτιδας (απο ιό Ρότα) συνέβησαν σε ετήσια βάση, 60,000 παιδιά νοσηλεύτηκαν και περίπου 37 πέθαναν ως αποτέλεσμα της λοίμωξης.[11] Ο κύριος ρόλος του ιού Ρότα στη πρόκληση της διάρροιας δεν είναι ακόμη ευρέως αναγνωρισμένος στην κοινότητα της δημόσιας υγείας,[63] ειδικά στις αναπτυσσόμενες χώρες.[8] Σχεδόν κάθε παιδί έχει μολυνθεί με τον ιό Ρότα έως την ηλικία των πέντε ετών.[64] Είναι η κορυφαία αιτία σοβαρής διάρροιας σε βρέφη και παιδιά, καθώς είναι υπεύθυνη για το 20% των περιπτώσεων της, και αντιπροσωπεύει το 50% των περιπτώσεων που απαιτούν νοσηλεία.[8] Ο ιός Ρότα προκαλεί το 37% των θανάτων που οφείλονται σε διάρροια και το 5% όλων των θανάτων σε παιδιά κάτω των πέντε ετών.[10] Τα αγόρια έχουν διπλάσιες πιθανότητες από τα κορίτσια να νοσηλευτούν.[7][65] Στις εύκρατες περιοχές, οι λοιμώξεις από τον ιό Ρότα αρχίζουν πρώιμα κυρίως τον χειμώνα, αλλά στους τροπικές ζώνες συμβαίνουν όλο το χρόνο ;[66] Η διαφορά αυτή εξηγείται από τις αλλαγές στη θερμοκρασία και την υγρασία.[67][68] Ο αριθμός που αναλογεί στη μόλυνση των τροφίμων δεν είναι γνωστός.[69]
of all hospital admissions due to diarrhoea among children under five years of age worldwide—leading to some 100 million episodes of acute diarrhoea each year that result in 350,000 to
600,000 child deaths."Τα κρούσματα της διάρροιας από τον ιό Ρότα είναι κοινά μεταξύ των νοσηλευόντων βρεφών, μικρών παιδιών που νοσηλεύονται σε κέντρα ημερήσιας φροντίδας,και ηλικιωμένων σε οίκους ευγηρίας.[71] Ένα ξέσπασμα που προκαλείται από μολυσμένο νερό δημοτικών συνέβει στο Κολοράντο το 1981.[72] Κατά το 2005, το μεγαλύτερο ποσοστό σε επιδημία διάρροιας συνέβη στη Νικαράγουα. Αυτό το ασυνήθιστα μεγάλο και σοβαρό κρούσμα που σχετίζεται με μεταλλάξεις στο γονιδίωμα του ιού Ρότα A, πιθανόν να βοηθάει τον ιό να ξεφύγει από την επικράτουσα ανοσία στον πληθυσμό.[73] Μια παρόμοια μεγάλη έκρηξη έγινε στη Βραζιλία το 1977.[74]
Ο ιός Ρότα B, που αναφέρεται επίσης και ως ιός Ρότα ενηλίκων ή ADRV, έχει προκαλέσει μεγάλες επιδημίες σοβαρής διάρροιας που προσβάλλουν χιλιάδες ανθρώπους κάθε ηλικίας στην Κίνα. Αυτές οι επιδημίες εμφανίστηκαν ως αποτέλεσμα της μόλυνσης από λύματα του πόσιμου νερού.[75][76] Λοιμώξεις από ιό Ρότα B συνέβησαν και στην Ινδία το 1998.Το αιτιολογικό στέλεχος ονομάστηκε CAL. Σε αντίθεση με το ADRV, το στέλεχος CAL είναι ενδημικό.[77][78] Μέχρι σήμερα επιδημίες που προκαλούνταν από τον ιό Ρότα B έχουν περιοριστεί ηπειρωτική Κίνα,και οι έρευνες καταδεικνύουν έλλειψη ανοσίας στις Ηνωμένες Πολιτείες.[79]
Ο ιός Ρότα C έχει συνδεθεί με σπάνιες και σποραδικές περιπτώσεις διάρροιας σε παιδιά σε πολλές χώρες, και εστίες εμφανίστηκαν στην Ιαπωνία και στην Αγγλία.[80][81]
Πρόληψη[Επεξεργασία | επεξεργασία κώδικα]
Επειδή βελτιώθηκαν οι εγκαταστάσεις υγιεινής δεν σημαίνει ότι μειώθηκε ο επιπολασμός της νόσου από τον ιό Ρότα, και το ποσοστό των νοσηλειών παραμένει υψηλό, παρά την ενυδάτωση από το στόμα. Το κύριο μέτρο της δημόσιας υγείας παραμένει ο εμβολιασμός.[82]
Λοιμώξεις των ζώων[Επεξεργασία | επεξεργασία κώδικα]
Ο ιός Ρότα μολύνει και μπορεί να προκαλέσει διάρροια στους νέους από πολλά είδη ζώων.[83] Μολύνει τα θηλαστικά (για παράδειγμα, τους πιθήκους,[84] βοοειδη,[85] χοίρων,[86] σε πρόβατα,[9] αρουραίους,[87] γάτες και σκυλιά,[88] ποντίκια,[89] άλογα,[90] κουνέλια)[91] και πτηνά (κοτόπουλα και γαλοπούλες).[92] Αυτά τα είδη των ιών Ρότα μπορούν να εξαλλαχθούν γενετικά σε ανθρώπινους ιούς Ρότα.[93] Υπάρχουν αποδείξεις ότι οι ιοί Ρότα των ζώων μπορούν να μολύνουν ανθρώπους, είτε με άμεση μετάδοση του ιού είτε με τη συμβολή ενός ή περισσοτέρών τμημάτων RNA για να γίνει ο ετεροσυνδυασμός με τα ανθρώπινα στελέχη.[94][95] Οι ιοί Ρότα είναι παθογόνοι και μπορούν να προκαλέσουν οικονομικές απώλειες για τους γεωργούς λόγω του κόστους της θεραπείας που συνδέονται με υψηλά ποσοστά νοσηρότητας και θνητότητας.[9]
Ιολογία[Επεξεργασία | επεξεργασία κώδικα]
Τύποι του ιού Ρότα[Επεξεργασία | επεξεργασία κώδικα]
Υπάρχουν 5 τύποι του ιού Ρότα που αναφέρονται ως A, B, C, D και E.Οι άνθρωποι κυρίως μολύνονται από τα είδη A, B και C, πιο συχνά από το είδος A. Και τα πέντε είδη προκαλούν ασθένεια στα ζώα.[96] Στην κατηγορία του ιού Ρότα Α υπάρχουν διαφορετικά στελέχη που ονομάζονται ορότυποι.[97] Όπως και στον ιό της γρίπης, ένα σύστημα διπλής ταξινόμησης χρησιμοποιείται, που βασίζεται σε δύο δομικές πρωτεΐνες στην επιφάνεια του βιρίου. Η γλυκοπρωτεΐνη VP7 καθορίζει τους G τύπους και η πρωτεάση-ευαίσθητη πρωτεΐνη VP4 καθορίζει τους P τύπους. Τα στελέχη γενικά υποδεικνύονται από τον ειδικό G ορότυπό τους (ορότυποι G1 με G4 και G9 ),και τα P τύπου υποδηλώνονται από έναν αριθμό και ένα γράμμα και από έναν ακόμα αριθμό μέσα σε αγκύλες για τον αντίστοιχο Pγονότυπος.( Οι ορότυποι P είναι δύσκολο να χαρακτηριστούν, γι αυτό μοριακές μέθοδοι που βασίζονται στην ανάλυση ακολουθίας χρησιμοποιούνται συχνά για τον καθορισμό του αντίστοιχου P γονότυπου. Αυτοί οι γονότυποι συσχετίζονται καλά με γνωστούς P ορότυπους.[28] Επειδή τα δύο γονίδια που καθορίζουν τους G και P τύπους μπορούν να μεταβιβαστούν ξεχωριστά στους απογόνους, διάφοροι συνδυασμοί λαμβάνουν χώρα σε οποιοδήποτε στέλεχος.Το Wa στέλεχος κατατάσσεται πλήρως ως G1P1A[8].[98]
Δομή[Επεξεργασία | επεξεργασία κώδικα]
Το γονιδίωμα του ιού Ρότα συνίσταται από 11 μοναδικά δίκλωνα μόρια RNA τα οποία είναι συνολικά 18,555 νουκλεοτίδια. Κάθε έλικα, ή τμήμα, είναι ένα γονίδιο, αριθμημένο από το 1 έως το 11 κατά μειούμενη σειρά. Κάθε γονίδιο κωδικοποιεί μια πρωτεΐνη, εκτός από τα γονίδια 9 και 11, το καθένα από τα οποία κωδικοποιεί 2.[99] Το RNA περιβάλλεται από ένα καψίδιο μιας τριτοταγούς εικοσαεδρικής πρωτεΐνης. Τα ιικά σωματίδια έχουν εώς και 76.5 nm διάμετρο[100][101] και δεν έχουν περίβλημα.
Πρωτεΐνες[Επεξεργασία | επεξεργασία κώδικα]
Υπάρχουν 6 ιικές πρωτεΐνες (VPs) που συγκροτούν το σωματίδιο του ιού (βίριο ή ιοσωμάτιο). Αυτές οι δομικές πρωτεΐνες ονομάζονται VP1, VP2, VP3, VP4, VP6 and VP7. Εκτός από τις VPs, υπάρχουν 6 μη δομικές πρωτεΐνες (NSPs), που παράγονται μόνο σε κύτταρα μολυσμένα από τον ιό Ρότα. Αυτές ονομάζονται NSP1, NSP2, NSP3, NSP4, NSP5 and NSP6 πρωτεΐνες.[96]
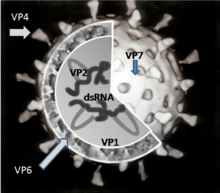
Τουλάχιστον 6 από τις 12 πρωτεΐνες κωδικοποιούμενες από το γονιδίωμα του ιού δεσμεύουν RNA.[102] Ο ρόλος που διαδραματίζουν αυτές οι πρωτεΐνες στην αναπαραγωγή του ιού δεν είναι πλήρως κατανοητός. Οι λειτουργίες τους πιστεύεται ότι σχετίζονται με τη σύνθεση και το πακετάρισμα του RNA στο βίριο, τη μεταφορά του mRNA στον τόπο της αντιγραφής του γονιδιώματος, τη μετάφραση του mRNA και τη ρύθμιση της γονιδιακής έκφρασης.[103]
Δομικές πρωτεΐνες[Επεξεργασία | επεξεργασία κώδικα]
Η VP1 βρίσκεται στον πυρήνα του σωματιδίου και είναι ένα ένζυμο RNA πολυμεράση.[104] Σε ένα μολυσμένο κύτταρο αυτό το ένζυμο παράγει mRNA αντίγραφα για τη σύνθεση των ιικών πρωτεϊνών και αντίγραφα του γονιδιώματος του ιού για πρόσφατα παραχθέντα σωματίδια του ιού.
Η VP2 αποτελεί το στρώμα του πυρήνα του βιρίου και δεσμεύει το RNA γονιδίωμα.[105]
Η VP3 είναι μέρος του εσωτερικού πυρήνα του βιρίου και είναι ένα ένζυμο που ονομάζεται γουανυλική τρανσφεράση. Αυτό είναι ένα ένζυμο που καταλύει το σχηματισμό της 5'καλύπτρας στη μετα-μεταγραφική επεξεργασία του mRNA.[106] Η καλύπτρα σταθεροποιεί το ιικό mRNA προστατευοντάς το από ένζυμα που διασπούν το νουκλεϊκό οξύ και λέγονται νουκλεάσες.
Η VP4 βρίσκεται στην επιφάνεια του βιρίου και προεξέχει σαν ακίδα.[107] Ενώνεται με μόρια στην επιφάνεια των κυττάρων που ονομάζονται υποδοχείς και οδηγεί την είσοδο του ιού στο κύτταρο.[108] Η VP4 πρέπει να τροποποιηθεί από μια πρωτεάση(ένζυμο που βρίσκεται στο έντερο) σε VP5* and VP8* πριν ο ιός να γίνει μεταδοτικός.[109] Καθορίζει πόσο παθογόνος είναι ο ιός και τον P τύπο του.[110]
Η VP6 αποτελεί τον κύριο όγκο του καψιδίου. Είναι πολύ αντιγονικό και μπορεί να χρησιμοποιηθεί στην αναγνώριση των ειδών ιού ρότα.[4] Αυτή η πρωτεΐνη χρησιμοποιείται σε εργαστηριακές δοκιμές για λοίμωξη από ιό ρότα Α.[50]
Η VP7 είναι μια γλυκοπρωτεΐνη που σχηματίζει την εξωτερική επιφάνεια του βιρίου. Εκτός από τις δομικές της λειτουργίες,καθορίζει τον G-τύπο του στελέχους και, μαζί με την VP4, εμπλέκεται στην ανοσία στη μόλυνση.[100]
Μή δομικές ιικές πρωτεΐνες[Επεξεργασία | επεξεργασία κώδικα]
Η NSP1,το προϊόν του γονιδίου 5,είναι μια μή δομική RNA-δεσμευτική πρωτεΐνη.[111]
Η NSP2 είναι μια RNA δεσμευτική πρωτεΐνη που συσσωρεύεται στα κυτταροπλασματικά έγκλειστα (ιικό πλάσμα)και απαιτείται για την αντιγραφή του γονιδιώματος.[112][113]
Η NSP3 είναι δεσμευμένη σε ιικά mRNA σε μολυσμένα κύτταρα και είναι υπεύθυνη για τη διακοπή της λειτουργίας της κυτταρικής πρωτεϊνοσύνθεσης.[114]
Η NSP4 είναι μια ιική εντεροτοξίνη που επάγει τη διάρροια και ήταν η πρώτη ιική εντεροτοξίνη που ανακαλύφθηκε.[115]
Η NSP5 κωδικοποιείται από το γονιδιακό τμήμα 11 του ιού ρότα Α και σε κύτταρα μολυσμένα από ιό συσσωρεύεται στο ιικό πλάσμα.[116]
Η NSP6 είναι μια πρωτεΐνη που δεσμεύει νουκλεϊκό οξύ,[117] και κωδικοποιείται από το γονίδιο 11 από ένα ανοιχτό πλαίσιο ανάγνωσης.[118]
| RNA κατά τομέα (Γένος) | Μέγεθος (ζεύγη βάσεων) | Πρωτεΐνη | Μοριακό Βάρος kDa | Τοποθεσία | Αντίγραφα ανά σωματίδιο | Λειτουργία |
|---|---|---|---|---|---|---|
| 1 | 3302 | VP1 | 125 | Στις κορυφές του πυρήνα | <25 | RNA-εξαρτώμενη RNA πολυμεράση |
| 2 | 2690 | VP2 | 102 | Μορφές στο εσωτερικό κέλυφος του πυρήνα | 120 | Διεγείρει την αντιγραφή του ιικό RNA |
| 3 | 2591 | VP3 | 88 | Στις κορυφές του πυρήνα | <25 | Γουανιλική τρανσφεράση του mRNA |
| 4 | 2362 | VP4 | 87 | Επιφανειακή ακίδα | 120 | Προσκόλληση των κυττάρων, λοιμογόνος δύναμη |
| 5 | 1611 | NSP1 | 59 | Μη δομική | 0 | Δεσμεύει 5'RNA |
| 6 | 1356 | VP6 | 45 | Εσωτερικό καψίδιο | 780 | Δομικό και ειδικό για είδη αντιγόνο |
| 7 | 1104 | NSP3 | 37 | Μη δομική | 0 | Δυναμώνει την RNA ιική δραστηριότητα και σταματά την πρωτεινοσύνθεση |
| 8 | 1059 | NSP2 | 35 | Μη δομική | 0 | ΝTP-άση που εμπλέκεται σε συσκευασία RNA συσκευασία |
| 9 | 1062 | VP71 VP72 | 38 and 34 | Επιφάνεια | 780 | Δομικό και εξουδετερωτικό αντιγόνο |
| 10 | 751 | NSP4 | 20 | Μη δομικό | 0 | Εντεροτοξίνη |
| 11 | 667 | NSP5 NSP6 | 22 | Μη δομικό | 0 | ssRNA και dsRNA δεσμευτικό του NSP2 |
Ο πίνακας αυτός βασίζεται στο στέλεχος SA11 ιού ρότα πιθήκου.[119][120][121] Οι αποστολές των RNA κωδικευουσών πρωτεϊνών διαφέρουν σε ορισμένα στελέχη.
Αντιγραφή[Επεξεργασία | επεξεργασία κώδικα]
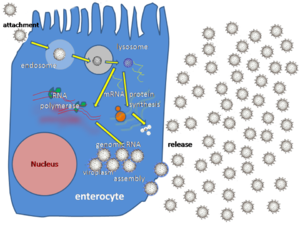
Οι ροταϊοί αναπαράγονται κυρίως στο έντερο,[122] και μολύνουν εντεροκύτταρα των λαχνών του λεπτού εντέρου, οδηγώντας σε δομικές και λειτουργικές αλλαγές του επιθηλίου.[123] Το τριπλό πρωτεϊνικό στρώμα τα κάνει ανθεκτικά στο όξινο pH του στομάχου και των πεπτικών ενζύμων στο έντερο.
Ο ιός εισέρχεται στα κύτταρα με τη μεσολάβηση υποδοχέα ενδοκυττάρωσης και σχηματίζει μια κύστη γνωστή ως ενδόσωμα. Οι πρωτεΐνες στο τρίτο στρώμα (VP7 and the VP4) διαταράσσουν τη μεμβράνη του ενδοσώματος, δημιουργώντας μια διαφορά στη συγκέντρωση ασβεστίου. Αυτό προκαλεί το σπάσιμο των VP7 τριμερών σε ενιαίες πρωτεϊνικές υπομονάδες, αφήνοντας τα VP2 και VP6 πρωτεϊνικά στρώματα γύρω από το ιικό dsRNA, σχηματίζοντας ένα σωματίδιο διπλής στρώσης (DLP).
Τα 11 dsRNA κλώνοι παραμένουν μέσα στη προστασία των δύο πρωτεϊνικών κελύφων και η ιική RNA εξαρτώμενη πολυμεράση δημιουργεί mRNA αντίγραφα του ιικού γονιδιώματος. Παραμένοντας στον πυρήνα, το ιικό RNA αποφεύγει ανοσολογικές απαντήσεις που ονομάζονται RNA παρεμβολές και επάγονται από την παρουσία τουt δίκλωνου RNA.
Κατά τη διάρκεια της λοίμωξης, ο ιός Ρότα παράγει mRNA και για την βιοσύνθεση των πρωτεϊνών και για την αναπαραγωγή των γονιδίων. Οι περισσότερες πρωτεΐνες του ιού Ρότα συσσωρεύονται στον ιικό πλάσμα, όπου το RNA αντιγράφεται και τα διπλής στρώσης σωματίδια συγκεντρώνονται. Ιικό πλάσμα σχηματίζεται γύρω από τον πυρήνα του κυττάρου δύο ώρες μετά τη λοίμωξη από τον ιό, και αποτελείται από "ιικά εργοστάσια" που πιστεύεται ότι σχηματίζονται από δύο ιικές μη δομικές πρωτεΐνες: NSP5 and NSP2. Η αναστολή της NSP5 από RNA παρεμβολή έχει ως αποτέλεσμα μια απότομη μείωση της αντιγραφής του ιού Ρότα. Τα DLPs μεταναστεύουν στο ενδοπλασματικό δίκτυο όπου και αποκτούν το τρίτο τους εξωτερικό στρώμα (σχηματιζόμενο από VP7 and VP4). Τα νέα ιοσωμάτια απελευθερώνονται από το κύτταρο με τη λύση.[124][125]
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 1,2 Dennehy PH (2000). «Transmission of rotavirus and other enteric pathogens in the home». Pediatr. Infect. Dis. J. 19 (10 Suppl): S103–5. doi:. PMID 11052397.
- ↑ 2,0 2,1 Velázquez FR, Matson DO, Calva JJ, Guerrero L, Morrow AL, Carter-Campbell S, Glass RI, Estes MK, Pickering LK, Ruiz-Palacios GM (1996). «Rotavirus infections in infants as protection against subsequent infections». N. Engl. J. Med. 335 (14): 1022–8. doi:. PMID 8793926. http://content.nejm.org/cgi/content/full/335/14/1022.
- ↑ 3,0 3,1 Linhares AC, Gabbay YB, Mascarenhas JD, Freitas RB, Flewett TH, Beards GM (1988). «Epidemiology of rotavirus subgroups and serotypes in Belem, Brazil: a three-year study». Ann. Inst. Pasteur Virol. 139 (1): 89–99. doi:. PMID 2849961.
- ↑ 4,0 4,1 4,2 4,3 Bishop RF (1996). «Natural history of human rotavirus infection». Arch. Virol. Suppl. 12: 119–28. PMID 9015109.
- ↑ «ICTV Virus Taxonomy: 2009 Release». Αρχειοθετήθηκε από το πρωτότυπο στις 4 Οκτωβρίου 2013. Ανακτήθηκε στις 29 Νοεμβρίου 2011.
- ↑ 6,0 6,1 Bishop RF, Davidson GP, Holmes IH, Ruck BJ (1973). «Virus particles in epithelial cells of duodenal mucosa from children with acute non-bacterial gastroenteritis». Lancet 2 (7841): 1281–3. doi:. PMID 4127639.
- ↑ 7,0 7,1 Rheingans RD, Heylen J, Giaquinto C (2006). «Economics of rotavirus gastroenteritis and vaccination in Europe: what makes sense?». Pediatr. Infect. Dis. J. 25 (1 Suppl): S48–55. doi:. PMID 16397429.
- ↑ 8,0 8,1 8,2 8,3 8,4 Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL (2007). «Use of formative research in developing a knowledge translation approach to rotavirus vaccine introduction in developing countries». BMC Public Health 7: 281. doi:. PMID 17919334. PMC 2173895. http://www.biomedcentral.com/1471-2458/7/281.
- ↑ 9,0 9,1 9,2 Holland RE (1 October 1990). «Some infectious causes of diarrhea in young farm animals» (PDF). Clin. Microbiol. Rev. 3 (4): 345–75. PMID 2224836. PMC 358168. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928100652/http://cmr.asm.org/cgi/reprint/3/4/345. Ανακτήθηκε στις 2011-11-30.
- ↑ 10,0 10,1 10,2 Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD (October 2011). «2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis». Lancet Infect Dis. doi:. PMID 22030330.
- ↑ 11,0 11,1 Fischer TK, Viboud C, Parashar U, et al. (2007). «Hospitalizations and deaths from diarrhea and rotavirus among children <5 years of age in the United States, 1993–2003». J. Infect. Dis. 195 (8): 1117–25. doi:. PMID 17357047.
- ↑ 12,0 12,1 Diggle L (2007). «Rotavirus diarrhoea and future prospects for prevention». Br. J. Nurs. 16 (16): 970–4. PMID 18026034.
- ↑ Light JS, Hodes HL (1943). «Studies on epidemic diarrhea of the new-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves». Am. J. Public Health Nations Health 33 (12): 1451–4. doi:. PMID 18015921.
- ↑ Mebus CA, Wyatt RG, Sharpee RL, et al. (1 August 1976). «Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis» (PDF). Infect. Immun. 14 (2): 471–4. PMID 184047. PMC 420908. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-29. https://web.archive.org/web/20110929135934/http://iai.asm.org/cgi/reprint/14/2/471. Ανακτήθηκε στις 2011-11-29.
- ↑ Rubenstein D, Milne RG, Buckland R, Tyrrell DA (1971). «The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium». British journal of experimental pathology 52 (4): 442–45. PMID 4998842.
- ↑ 16,0 16,1 Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1 September 1976). «Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals» (PDF). Infect. Immun. 14 (3): 804–10. PMID 965097. PMC 420956. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-29. https://web.archive.org/web/20110929135952/http://iai.asm.org/cgi/reprint/14/3/804. Ανακτήθηκε στις 2011-11-29.
- ↑ Bishop RF, Davidson GP, Holmes IH, Ruck BJ (1973). «Letter: Evidence for viral gastroenteritis». N. Engl. J. Med. 289 (20): 1096–7. doi:. PMID 4742237.
- ↑ 18,0 18,1 Flewett TH, Woode GN (1978). «The rotaviruses». Arch. Virol. 57 (1): 1–23. doi:. PMID 77663.
- ↑ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM (1974). «Relation between viruses from acute gastroenteritis of children and newborn calves». Lancet 2 (7872): 61–3. doi:. PMID 4137164.
- ↑ Matthews RE (1979). «Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses». Intervirology 12 (3–5): 129–296. doi:. PMID 43850.
- ↑ Beards GM, Pilfold JN, Thouless ME, Flewett TH (1980). «Rotavirus serotypes by serum neutralisation». J. Med. Virol. 5 (3): 231–7. doi:. PMID 6262451.
- ↑ Urasawa T, Urasawa S, Taniguchi K (1981). «Sequential passages of human rotavirus in MA-104 cells». Microbiol. Immunol. 25 (10): 1025–35. PMID 6273696.
- ↑ Vesikari T, Isolauri E, Delem A, et al. (1985). «Clinical efficacy of the RIT 4237 live attenuated bovine rotavirus vaccine in infants vaccinated before a rotavirus epidemic». J. Pediatr. 107 (2): 189–94. doi:. PMID 3894608. https://archive.org/details/sim_journal-of-pediatrics_1985-08_107_2/page/189.
- ↑ «Rotavirus vaccine for the prevention of rotavirus gastroenteritis among children. Recommendations of the Advisory Committee on Immunization Practices (ACIP)». MMWR Recomm Rep 48 (RR–2): 1–20. 1999. PMID 10219046.
- ↑ Kapikian AZ (2001). «A rotavirus vaccine for prevention of severe diarrhoea of infants and young children: development, utilization and withdrawal». Novartis Found. Symp. 238: 153–71; discussion 171–9. doi:. PMID 11444025.
- ↑ Bines JE (2005). «Rotavirus vaccines and intussusception risk». Curr. Opin. Gastroenterol. 21 (1): 20–5. PMID 15687880. Αρχειοθετήθηκε από το πρωτότυπο στις 2013-05-11. https://web.archive.org/web/20130511014221/http://meta.wkhealth.com/pt/pt-core/template-journal/lwwgateway/media/landingpage.htm?issn=0267-1379&volume=21&issue=1&spage=20. Ανακτήθηκε στις 2011-11-29.
- ↑ Bines J (2006). «Intussusception and rotavirus vaccines». Vaccine 24 (18): 3772–6. doi:. PMID 16099078.
- ↑ 28,0 28,1 Dennehy PH (2008). «Rotavirus vaccines: an overview». Clin. Microbiol. Rev. 21 (1): 198–208. doi:. PMID 18202442. PMC 2223838. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928101415/http://cmr.asm.org/cgi/content/full/21/1/198?view=long&pmid=18202442. Ανακτήθηκε στις 2011-11-29.
- ↑ «Meeting of the immunization Strategic Advisory Group of Experts, April 2009—conclusions and recommendations». Relevé Épidémiologique Hebdomadaire / Section D'hygiène Du Secrétariat De La Société Des Nations = Weekly Epidemiological Record / Health Section of the Secretariat of the League of Nations 84 (23): 220–36. June 2009. PMID 19499606.[1]
- ↑ Hochwald C, Kivela L (1999). «Rotavirus vaccine, live, oral, tetravalent (RotaShield)». Pediatr. Nurs. 25 (2): 203–4, 207. PMID 10532018.
- ↑ Maldonado YA, Yolken RH (1990). «Rotavirus». Baillieres Clin. Gastroenterol. 4 (3): 609–25. doi:. PMID 1962726.
- ↑ Bernstein DI, Sander DS, Smith VE, Schiff GM, Ward RL (1991). «Protection from rotavirus reinfection: 2-year prospective study». J. Infect. Dis. 164 (2): 277–83. doi:. PMID 1649875. https://archive.org/details/sim_journal-of-infectious-diseases_1991-08_164_2/page/277.
- ↑ Koopman JS, Monto AS (1989). «The Tecumseh Study. XV: Rotavirus infection and pathogenicity». Am. J. Epidemiol. 130 (4): 750–9. PMID 2549788.
- ↑ Cameron DJ, Bishop RF, Veenstra AA, Barnes GL (1 July 1978). «Noncultivable viruses and neonatal diarrhea: Fifteen-month survey in a newborn special care nursery» (PDF). J. Clin. Microbiol. 8 (1): 93–8. PMID 209058. PMC 275123. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927143254/http://jcm.asm.org/cgi/reprint/8/1/93. Ανακτήθηκε στις 2011-11-29.
- ↑ Grillner L, Broberger U, Chrystie I, Ransjö U (1985). «Rotavirus infections in newborns: an epidemiological and clinical study». Scand. J. Infect. Dis. 17 (4): 349–55. PMID 3003889.
- ↑ Hrdy DB (1987). «Epidemiology of rotaviral infection in adults». Rev. Infect. Dis. 9 (3): 461–9. doi:. PMID 3037675.
- ↑ De Champs C, Laveran H, Peigue-Lafeuille H, et al. (1991). «Sequential rotavirus infections: characterization of serotypes and electrophoretypes». Res. Virol. 142 (1): 39–45. doi:. PMID 1647052.
- ↑ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R (1993). «Prevalence of rotavirus on high-risk fomites in day-care facilities». Pediatrics 92 (2): 202–5. PMID 8393172. https://archive.org/details/sim_pediatrics_1993-08_92_2/page/202.
- ↑ Graham DY, Dufour GR, Estes MK (1987). «Minimal infective dose of rotavirus». Arch. Virol. 92 (3–4): 261–71. doi:. PMID 3028333.
- ↑ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1 August 1984). «Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments» (PDF). Appl. Environ. Microbiol. 48 (2): 404–9. PMID 6091548. PMC 241526. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927141439/http://aem.asm.org/cgi/reprint/48/2/404. Ανακτήθηκε στις 2011-11-29.
- ↑ Ball JM, Mitchell DM, Gibbons TF, Parr RD (2005). «Rotavirus NSP4: a multifunctional viral enterotoxin». Viral Immunol. 18 (1): 27–40. doi:. PMID 15802952.
- ↑ Lorrot M, Vasseur M (2007). «How do the rotavirus NSP4 and bacterial enterotoxins lead differently to diarrhea?». Virol. J. 4 (1): 31. doi:. PMID 17376232. PMC 1839081. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928140919/http://www.virologyj.com/content/4/1/31. Ανακτήθηκε στις 2011-11-29.
- ↑ Jourdan N, Brunet JP, Sapin C, et al. (1 September 1998). «Rotavirus infection reduces sucrase-isomaltase expression in human intestinal epithelial cells by perturbing protein targeting and organization of microvillar cytoskeleton». J. Virol. 72 (9): 7228–36. PMID 9696817. PMC 109945. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928063120/http://jvi.asm.org/cgi/content/full/72/9/7228. Ανακτήθηκε στις 2011-11-29.
- ↑ Davidson GP, Barnes GL (1979). «Structural and functional abnormalities of the small intestine in infants and young children with rotavirus enteritis». Acta Paediatr. Scand. 68 (2): 181–6. doi:. PMID 217231.
- ↑ Ouwehand A, Vesterlund S (2003). «Health aspects of probiotics». IDrugs 6 (6): 573–80. PMID 12811680.
- ↑ Arya SC (1984). «Rotaviral infection and intestinal lactase level». J. Infect. Dis. 150 (5): 791. PMID 6436397. https://archive.org/details/sim_journal-of-infectious-diseases_1984-11_150_5/page/791.
- ↑ 47,0 47,1 Patel MM, Tate JE, Selvarangan R, et al. (2007). «Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination». Pediatr. Infect. Dis. J. 26 (10): 914–9. doi:. PMID 17901797. https://archive.org/details/sim_pediatric-infectious-disease-journal_2007-10_26_10/page/914.
- ↑ The Pediatric ROTavirus European CommitTee (PROTECT) (2006). «The paediatric burden of rotavirus disease in Europe». Epidemiol. Infect. 134 (5): 908–16. doi:. PMID 16650331. PMC 2870494. https://archive.org/details/sim_epidemiology-and-infection_2006-10_134_5/page/908.
- ↑ Smith TF, Wold AD, Espy MJ, Marshall WF (1993). «New developments in the diagnosis of viral diseases». Infect. Dis. Clin. North Am. 7 (2): 183–201. PMID 8345165. https://archive.org/details/sim_infectious-disease-clinics-of-north-america_1993-06_7_2/page/183.
- ↑ 50,0 50,1 Beards GM, Campbell AD, Cottrell NR, Peiris JS, Rees N, Sanders RC, Shirley JA, Wood HC, Flewett TH (1 February 1984). «Enzyme-linked immunosorbent assays based on polyclonal and monoclonal antibodies for rotavirus detection» (PDF). J. Clin. Microbiol. 19 (2): 248–54. PMID 6321549. PMC 271031. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927143331/http://jcm.asm.org/cgi/reprint/19/2/248. Ανακτήθηκε στις 2011-11-30.
- ↑ Beards GM (1988). «Laboratory diagnosis of viral gastroenteritis». Eur. J. Clin. Microbiol. Infect. Dis. 7 (1): 11–3. doi:. PMID 3132369.
- ↑ Fischer TK, Gentsch JR (2004). «Rotavirus typing methods and algorithms». Rev. Med. Virol. 14 (2): 71–82. doi:. PMID 15027000.
- ↑ Alam NH, Ashraf H (2003). «Treatment of infectious diarrhea in children». Paediatr. Drugs 5 (3): 151–65. PMID 12608880.
- ↑ Sachdev HP (1996). «Oral rehydration therapy». Journal of the Indian Medical Association 94 (8): 298–305. PMID 8855579.
- ↑ Haffejee IE (1991). «The pathophysiology, clinical features and management of rotavirus diarrhoea». Q. J. Med. 79 (288): 289–99. PMID 1649479. http://qjmed.oxfordjournals.org/cgi/reprint/79/1/289.
- ↑ Ramig RF (2007). «Systemic rotavirus infection». Expert review of anti-infective therapy 5 (4): 591–612. doi:. PMID 17678424.
- ↑ Goto T, Kimura H, Numazaki K, et al. (2007). «A case of meningoencephalitis associated with G1P[8] rotavirus infection in a Japanese child». Scand. J. Infect. Dis. 39 (11): 1067–70. doi:. PMID 17852929.
- ↑ Kehle J, Metzger-Boddien C, Tewald F, Wald M, Schüürmann J, Enders G (2003). «First case of confirmed rotavirus meningoencephalitis in Germany». Pediatr. Infect. Dis. J. 22 (5): 468–70. doi:. PMID 12797316. https://archive.org/details/sim_pediatric-infectious-disease-journal_2003-05_22_5/page/468.
- ↑ Pager C, Steele D, Gwamanda P, Driessen M (2000). «A neonatal death associated with rotavirus infection—detection of rotavirus dsRNA in the cerebrospinal fluid». S. Afr. Med. J. 90 (4): 364–5. PMID 10957919.
- ↑ Widdowson MA, Bresee JS, Gentsch JR, Glass RI (2005). «Rotavirus disease and its prevention». Curr. Opin. Gastroenterol. 21 (1): 26–31. PMID 15687881. Αρχειοθετήθηκε από το πρωτότυπο στις 2012-02-09. https://web.archive.org/web/20120209161915/http://meta.wkhealth.com/pt/pt-core/template-journal/lwwgateway/media/landingpage.htm?issn=0267-1379&volume=21&issue=1&spage=26. Ανακτήθηκε στις 2011-11-30.
- ↑ Leung AK, Kellner JD, Davies HD (2005). «Rotavirus gastroenteritis». Adv. Ther. 22 (5): 476–87. doi:. PMID 16418157.
- ↑ Centers for Disease Control and Prevention (CDC) (October 2009). «Reduction in rotavirus after vaccine introduction—United States, 2000–2009». MMWR. Morbidity and Mortality Weekly Report 58 (41): 1146–9. PMID 19847149. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5841a2.htm. Ανακτήθηκε στις 2009-12-20.
- ↑ Rodrigo C, Salman N, Tatochenko V, Mészner Z, Giaquinto C (May 2010). «Recommendations for rotavirus vaccination: A worldwide perspective». Vaccine 28 (31): 5100–8. doi:. PMID 20472032.
- ↑ Parashar UD, Gibson CJ, Bresse JS, Glass RI (2006). «Rotavirus and severe childhood diarrhea». Emerging Infect. Dis. 12 (2): 304–6. PMID 16494759.
- ↑ Ryan MJ, Ramsay M, Brown D, Gay NJ, Farrington CP, Wall PG (1996). «Hospital admissions attributable to rotavirus infection in England and Wales». J. Infect. Dis. 174 Suppl 1: S12–8. PMID 8752285.
- ↑ Cook SM, Glass RI, LeBaron CW, Ho MS (1990). «Global seasonality of rotavirus infections». Bull. World Health Organ. 68 (2): 171–7. PMID 1694734.
- ↑ Moe K, Harper GJ (1983). «The effect of relative humidity and temperature on the survival of bovine rotavirus in aerosol». Arch. Virol. 76 (3): 211–6. doi:. PMID 6307226. https://archive.org/details/sim_archives-of-virology_1983_76_3/page/211.
- ↑ Moe K, Shirley JA (1982). «The effects of relative humidity and temperature on the survival of human rotavirus in faeces». Arch. Virol. 72 (3): 179–86. doi:. PMID 6287970.
- ↑ Koopmans M, Brown D (1999). «Seasonality and diversity of Group A rotaviruses in Europe». Acta Paediatrica Supplement 88 (426): 14–9. doi:. PMID 10088906.
- ↑ UNICEF/WHO (2009) "Diarrhoea: Why children are still dying and what can be done." Retrieved 23 May 2010
- ↑ Anderson EJ, Weber SG (February 2004). «Rotavirus infection in adults». The Lancet Infectious Diseases 4 (2): 91–9. doi:. PMID 14871633. http://linkinghub.elsevier.com/retrieve/pii/S1473309904009284.
- ↑ Hopkins RS, Gaspard GB, Williams FP, Karlin RJ, Cukor G, Blacklow NR (1984). «A community waterborne gastroenteritis outbreak: evidence for rotavirus as the agent». American Journal of Public Health 74 (3): 263–5. doi:. PMID 6320684. PMC 1651463. https://archive.org/details/sim_american-journal-of-public-health_1984-03_74_3/page/263.
- ↑ Bucardo F, Karlsson B, Nordgren J, et al. (2007). «Mutated G4P[8] rotavirus associated with a nationwide outbreak of gastroenteritis in Nicaragua in 2005». J. Clin. Microbiol. 45 (3): 990–7. doi:. PMID 17229854. PMC 1829148. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927143527/http://jcm.asm.org/cgi/content/full/45/3/990. Ανακτήθηκε στις 2011-11-30.
- ↑ Linhares AC, Pinheiro FP, Freitas RB, Gabbay YB, Shirley JA, Beards GM (1981). «An outbreak of rotavirus diarrhea among a non-immune, isolated South American Indian community». Am. J. Epidemiol. 113 (6): 703–10. PMID 6263087.
- ↑ Hung T, Chen GM, Wang CG, et al. (1984). «Waterborne outbreak of rotavirus diarrhea in adults in China caused by a novel rotavirus». Lancet 1 (8387): 1139–42. doi:. PMID 6144874.
- ↑ Fang ZY, Ye Q, Ho MS, et al. (1989). «Investigation of an outbreak of adult diarrhea rotavirus in China». J. Infect. Dis. 160 (6): 948–53. doi:. PMID 2555422. https://archive.org/details/sim_journal-of-infectious-diseases_1989-12_160_6/page/948.
- ↑ Kelkar SD, Zade JK (2004). «Group B rotaviruses similar to strain CAL-1, have been circulating in Western India since 1993». Epidemiol. Infect. 132 (4): 745–9. doi:. PMID 15310177. PMC 2870156. https://archive.org/details/sim_epidemiology-and-infection_2004-08_132_4/page/745.
- ↑ Ahmed MU, Kobayashi N, Wakuda M, Sanekata T, Taniguchi K, Kader A, Naik TN, Ishino M, Alam MM, Kojima K, Mise K, Sumi A (2004). «Genetic analysis of group B human rotaviruses detected in Bangladesh in 2000 and 2001». J. Med. Virol. 72 (1): 149–55. doi:. PMID 14635024.
- ↑ Penaranda ME, Ho MS, Fang ZY, et al. (1 October 1989). «Seroepidemiology of adult diarrhea rotavirus in China, 1977 to 1987» (PDF). J. Clin. Microbiol. 27 (10): 2180–3. PMID 2479654. PMC 266989. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927143544/http://jcm.asm.org/cgi/reprint/27/10/2180. Ανακτήθηκε στις 2011-11-30.
- ↑ Kuzuya M, Fujii R, Hamano M, Nishijima M, Ogura Η (2007). «Detection and molecular characterization of human group C rotaviruses in Okayama Prefecture, Japan, between 1986 and 2005». J. Med. Virol. 79 (8): 1219–28. doi:. PMID 17596825.
- ↑ Brown DW, Campbell L, Tomkins DS, Hambling MH (1989). «School outbreak of gastroenteritis due to atypical rotavirus». Lancet 2 (8665): 737–8. doi:. PMID 2570978.
- ↑ Bernstein DI (March 2009). «Rotavirus overview». Pediatr. Infect. Dis. J. 28 (3 Suppl): S50–3. doi:. PMID 19252423. http://meta.wkhealth.com/pt/pt-core/template-journal/lwwgateway/media/landingpage.htm?an=00006454-200903001-00002. Ανακτήθηκε στις 2009-03-15.[νεκρός σύνδεσμος]
- ↑ Dwight C. Hirsh· Nigel James Maclachlan· Richard L. Walker (2004). Veterinary microbiology. Cambridge, MA: Blackwell Pub. σελίδες 404–5. ISBN 0-8138-0379-9.
- ↑ Ashley CR, Caul EO, Clarke SK, Corner BD, Dunn S (1978). «Rotavirus infections of apes». Lancet 2 (8087): 477. doi:. PMID 79844.
- ↑ Wani SA, Bhat MA, Ishaq SM, Ashrafi MA (2004). «Determination of bovine rotavirus G genotypes in Kashmir, India». Rev. – Off. Int. Epizoot. 23 (3): 931–6. PMID 15861888.
- ↑ Saif LJ (1999). «Enteric viral infections of pigs and strategies for induction of mucosal immunity». Advances in veterinary medicine 41: 429–46. doi:. PMID 9890034.
- ↑ Pérez-Cano FJ, Castell M, Castellote C, Franch A (2007). «Characterization of Clinical and Immune Response in a Rotavirus Diarrhea Model in Suckling Lewis Rats». Pediatr Res 62 (6): 658. doi:. PMID 17957154.
- ↑ Enriquez C, Nwachuku N, Gerba CP (2001). «Direct exposure to animal enteric pathogens». Reviews on environmental health 16 (2): 117–31. PMID 11512628.
- ↑ Feng N, Franco MA, Greenberg HB (1997). «Murine model of rotavirus infection». Adv. Exp. Med. Biol. 412: 233–40. PMID 9192019.
- ↑ Hardy ME, Woode GN, Xu ZC, et al. (May 1991). «Analysis of serotypes and electropherotypes of equine rotaviruses isolated in the United States». J. Clin. Microbiol. 29 (5): 889–93. PMID 1647407. PMC 269902. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-05-25. https://web.archive.org/web/20110525204912/http://jcm.asm.org/cgi/reprint/29/5/889?view=long&pmid=1647407. Ανακτήθηκε στις 2011-11-30.
- ↑ Thouless ME, DiGiacomo RF, Deeb BJ, Howard Η (1 May 1988). «Pathogenicity of rotavirus in rabbits» (PDF). J. Clin. Microbiol. 26 (5): 943–7. PMID 2838507. PMC 266491. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-27. https://web.archive.org/web/20110927143559/http://jcm.asm.org/cgi/reprint/26/5/943. Ανακτήθηκε στις 2011-11-30.
- ↑ Guy JS (1 August 1998). «Virus infections of the gastrointestinal tract of poultry» (PDF). Poult. Sci. 77 (8): 1166–75. PMID 9706084. Αρχειοθετήθηκε από το πρωτότυπο στις 2008-12-25. https://web.archive.org/web/20081225021439/http://ps.fass.org/cgi/reprint/77/8/1166. Ανακτήθηκε στις 2011-11-30.
- ↑ Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (2010). «Zoonotic aspects of rotaviruses». Veterinary Microbiology 140 (3-4): 246–55. doi:. PMID 19781872.
- ↑ Müller H, Johne R (2007). «Rotaviruses: diversity and zoonotic potential—a brief review». Berl. Munch. Tierarztl. Wochenschr. 120 (3–4): 108–12. PMID 17416132.
- ↑ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J (2004). «The zoonotic potential of rotavirus». J. Infect. 48 (4): 289–302. doi:. PMID 15066329.
- ↑ 96,0 96,1 Kirkwood CD (September 2010). «Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs». The Journal of Infectious Diseases 202 Suppl: S43–8. doi:. PMID 20684716.
- ↑ Santos N, Hoshino Y (2005). «Global distribution of rotavirus serotypes/genotypes and its implication for the development and implementation of an effective rotavirus vaccine». Rev. Med. Virol. 15 (1): 29–56. doi:. PMID 15484186.
- ↑ Desselberger U, Wolleswinkel-van den Bosch J, Mrukowicz J, Rodrigo C, Giaquinto C, Vesikari T (2006). «Rotavirus types in Europe and their significance for vaccination». Pediatr. Infect. Dis. J. 25 (1 Suppl.): S30–41. doi:. PMID 16397427. Αρχειοθετήθηκε από το πρωτότυπο στις 2013-05-11. https://web.archive.org/web/20130511004523/http://meta.wkhealth.com/pt/pt-core/template-journal/lwwgateway/media/landingpage.htm?an=00006454-200601001-00005. Ανακτήθηκε στις 2011-11-30.
- ↑ Chan WK, Penaranda ME, Crawford SE, Estes MK (1986). «Two glycoproteins are produced from the rotavirus neutralization gene». Virology 151 (2): 243–52. doi:. PMID 3010552.
- ↑ 100,0 100,1 Pesavento JB, Crawford SE, Estes MK, Prasad BV (2006). «Rotavirus proteins: structure and assembly». Curr. Top. Microbiol. Immunol. 309: 189–219. doi:. PMID 16913048.
- ↑ Prasad BV, Chiu W (1994). «Structure of rotavirus». Curr. Top. Microbiol. Immunol. 185: 9–29. PMID 8050286.
- ↑ Patton JT (1995). «Structure and function of the rotavirus RNA-binding proteins» (PDF). J. Gen. Virol. 76 (Pt 11) (11): 2633–44. doi:. PMID 7595370. Αρχειοθετήθηκε από το πρωτότυπο στις 2012-12-09. https://archive.today/20121209041049/http://vir.sgmjournals.org/cgi/reprint/76/11/2633. Ανακτήθηκε στις 2011-11-30.
- ↑ Patton JT (2001). «Rotavirus RNA replication and gene expression». Novartis Found. Symp. 238: 64–77; discussion 77–81. doi:. PMID 11444036.
- ↑ Vásquez-del Carpió R, Morales JL, Barro M, Ricardo A, Spencer E (2006). «Bioinformatic prediction of polymerase elements in the rotavirus VP1 protein». Biol. Res. 39 (4): 649–59. doi:. PMID 17657346. http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0716-97602006000500008&tlng=en&lng=en&nrm=iso.
- ↑ Arnoldi F, Campagna M, Eichwald C, Desselberger U, Burrone OR (2007). «Interaction of rotavirus polymerase VP1 with nonstructural protein NSP5 is stronger than that with NSP2». J. Virol. 81 (5): 2128–37. doi:. PMID 17182692. PMC 1865955. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928063150/http://jvi.asm.org/cgi/content/full/81/5/2128. Ανακτήθηκε στις 2011-11-30.
- ↑ Fresco LD, Buratowski S (1994). «Active site of the mRNA-capping enzyme guanylyltransferase from Saccharomyces cerevisiae: similarity to the nucleotidyl attachment motif of DNA and RNA ligases» (PDF). Proc. Natl. Acad. Sci. U.S.A. 91 (14): 6624–8. doi:. PMID 8022828. PMC 44255. http://www.pnas.org/content/91/14/6624.full.pdf+html.
- ↑ Gardet A, Breton M, Fontanges P, Trugnan G, Chwetzoff S (2006). «Rotavirus spike protein VP4 binds to and remodels actin bundles of the epithelial brush border into actin bodies». J. Virol. 80 (8): 3947–56. doi:. PMID 16571811. PMC 1440440. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928063206/http://jvi.asm.org/cgi/content/full/80/8/3947. Ανακτήθηκε στις 2011-11-30.
- ↑ Arias CF, Isa P, Guerrero CA, Méndez E, Zárate S, López T, Espinosa R, Romero P, López S (2002). «Molecular biology of rotavirus cell entry». Arch. Med. Res. 33 (4): 356–61. doi:. PMID 12234525.
- ↑ Konno T, Suzuki H, Kitaoka S, Sato T, Fukuhara N, Yoshie O, Fukudome K, Numazaki Y (1993). «Proteolytic enhancement of human rotavirus infectivity». Clin. Infect. Dis. 16 Suppl 2: S92–7. PMID 8384014.
- ↑ Hoshino Y, Jones RW, Kapikian AZ (2002). «Characterization of neutralization specificities of outer capsid spike protein VP4 of selected murine, lapine, and human rotavirus strains». Virology 299 (1): 64–71. doi:. PMID 12167342.
- ↑ Hua J, Mansell EA, Patton JT (1993). «Comparative analysis of the rotavirus NS53 gene: conservation of basic and cysteine-rich regions in the protein and possible stem-loop structures in the RNA». Virology 196 (1): 372–8. doi:. PMID 8395125.
- ↑ Kattoura MD, Chen X, Patton JT (1994). «The rotavirus RNA-binding protein NS35 (NSP2) forms 10S multimers and interacts with the viral RNA polymerase». Virology 202 (2): 803–13. doi:. PMID 8030243.
- ↑ Taraporewala ZF, Patton JT (2004). «Nonstructural proteins involved in genome packaging and replication of rotaviruses and other members of the Reoviridae». Virus Res. 101 (1): 57–66. doi:. PMID 15010217.
- ↑ Poncet D, Aponte C, Cohen J (1 June 1993). «Rotavirus protein NSP3 (NS34) is bound to the 3' end consensus sequence of viral mRNAs in infected cells» (PDF). J. Virol. 67 (6): 3159–65. PMID 8388495. PMC 237654. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-09-28. https://web.archive.org/web/20110928063238/http://jvi.asm.org/cgi/reprint/67/6/3159. Ανακτήθηκε στις 2011-11-30.
- ↑ Dong Y, Zeng CQ, Ball JM, Estes MK, Morris AP (1997). «The rotavirus enterotoxin NSP4 mobilizes intracellular calcium in human intestinal cells by stimulating phospholipase C-mediated inositol 1,4,5-trisphosphate production». Proc. Natl. Acad. Sci. U.S.A. 94 (8): 3960–5. doi:. PMID 9108087. PMC 20550. http://www.pnas.org/content/94/8/3960.full.
- ↑ Afrikanova I, Miozzo MC, Giambiagi S, Burrone Ο (1996). «Phosphorylation generates different forms of rotavirus NSP5». J. Gen. Virol. 77 ( Pt 9) (9): 2059–65. doi:. PMID 8811003. Αρχειοθετήθηκε από το πρωτότυπο στις 2012-05-26. https://archive.today/20120526030014/http://vir.sgmjournals.org/cgi/reprint/77/9/2059. Ανακτήθηκε στις 2011-11-30.
- ↑ Rainsford EW, McCrae MA (2007). «Characterization of the NSP6 protein product of rotavirus gene 11». Virus Res. 130 (1–2): 193–201. doi:. PMID 17658646.
- ↑ Mohan KV, Atreya CD (2001). «Nucleotide sequence analysis of rotavirus gene 11 from two tissue culture-adapted ATCC strains, RRV and Wa». Virus Genes 23 (3): 321–9. doi:. PMID 11778700.
- ↑ Desselberger U. Rotavirus: basic facts. In Rotaviruses Methods and Protocols. Ed. Gray, J. and Desselberger U. Humana Press, 2000, pp. 1–8. ISBN 0-89603-736-3
- ↑ Patton JT. Rotavirus RNA replication and gene expression. In Novartis Foundation. Gastroenteritis Viruses, Humana Press, 2001, pp. 64–81. ISBN 0-471-49663-4
- ↑ Claude M. Fauquet· J. Maniloff· Desselberger, U. (2005). Virus taxonomy: classification and nomenclature of viruses: 8th report of the International Committee on Taxonomy of Viruses. Amsterdam: Elsevier/Academic Press. σελίδες 489. ISBN 0-12-249951-4.
- ↑ Greenberg HB, Estes MK (May 2009). «Rotaviruses: from pathogenesis to vaccination». Gastroenterology 136 (6): 1939–51. doi:. PMID 19457420. https://archive.org/details/sim_gastroenterology_2009-05_136_6/page/1939.
- ↑ Greenberg HB, Clark HF, Offit PA (1994). «Rotavirus pathology and pathophysiology». Curr. Top. Microbiol. Immunol. 185: 255–83. PMID 8050281.
- ↑ Jayaram H, Estes MK, Prasad BV (2004). «Emerging themes in rotavirus cell entry, genome organization, transcription and replication». Virus Res. 101 (1): 67–81. doi:. PMID 15010218.
- ↑ Patton JT, Vasquez-Del Carpio R, Spencer E (2004). «Replication and transcription of the rotavirus genome». Curr. Pharm. Des. 10 (30): 3769–77. doi:. PMID 15579070.
