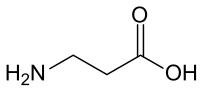
β-αλανίνη
| β-αλανίνη | |
|---|---|
| |
| Γενικά | |
| Όνομα IUPAC | 3-αμινοπροπανικό οξύ |
| Άλλες ονομασίες | β-αλανίνη |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C3H7NO2 |
| Μοριακή μάζα | 89,09 amu |
| Σύντομος συντακτικός τύπος |
H2NCH2CH2COOH |
| Αριθμός CAS | 107-95-9 |
| SMILES | O=C(O)CCN |
| InChI | 1S/C3H7NO2/c4-2-1-3(5)6/h1-2,4H2,(H,5,6) |
| Αριθμός EINECS | 203-536-5 |
| Αριθμός RTECS | SJ3325000 |
| Αριθμός UN | 11P2JDE17B |
| PubChem CID | 239 |
| ChemSpider ID | 234 |
| Ισομέρεια | |
| Ισομερή θέσης | >119 |
| Φυσικές ιδιότητες | |
| Σημείο τήξης | 207 °C (διάσπαση) |
| Πυκνότητα | 1.437 kg/m3 (19 °C) |
| Διαλυτότητα στο νερό |
Διαλυτή |
| Εμφάνιση | λευκό διπυραμιδικό κρυσταλλικό στερεό |
| Χημικές ιδιότητες | |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
Η β-αλανίνη ή 3-αμινοπροπανικό οξύ είναι ένα β-αμινοξύ που υπάρχει στη φύση. Το πρόθεμα β- δείχνει ότι η αμινομάδα συνδέεται με το 2ο άτομο άνθρακα μετά το καρβοξύλιο, ενώ στη συστηματική ονομασία, το 3- μετρά και το άτομο άνθρακα του καρβοξυλίου, ως #1. Αντίθετα με την ισομερή της αλανίνη, η β-αλανίνη δεν έχει οπτικά ισομερή:
Ισομέρεια[Επεξεργασία | επεξεργασία κώδικα]
Με βάση το χημικό τύπο της, C3H7NO2, έχει τουλάχιστον τα ακόλουθα 119 ισομερή θέσης:
- 1-νιτροπροπάνιο με σύντομο συντακτικό τύπο: CH3CH2CH2NO2.
- 2-νιτροπροπάνιο με σύντομο συντακτικό τύπο: CH3CH(NO2)CH3.
- Νιτρώδης προπυλεστέρας με σύντομο συντακτικό τύπο: CH3CH2CH2ONO (ο προπυλεστέρας του νιτρώδους οξέος).
- Νιτρώδης ισοπροπυλεστέρας με σύντομο συντακτικό τύπο: CH3CH(ONO)CH3 (ο ισοπροπυλεστέρας του νιτρώδους οξέος).
- 1-νιτρωδοπροπανόλη-1 με σύντομο συντακτικό τύπο: CH3CH2CH(NO)OH (σε δύο (2) οπτικά ισομερή).
- 2-νιτρωδοπροπανόλη-1 με σύντομο συντακτικό τύπο: CH3CH(NO)CH2OH (σε δύο (2) οπτικά ισομερή).
- 3-νιτρωδοπροπανόλη-1 με σύντομο συντακτικό τύπο: ONCH3CH2CH2OH.
- 1-νιτρωδοπροπανόλη-2 με σύντομο συντακτικό τύπο: CH3CH(OH)CH2NO (σε δύο (2) οπτικά ισομερή).
- 2-νιτρωδοπροπανόλη-2 με σύντομο συντακτικό τύπο: CH3C(NO)(OH)CH3.
- 2-αμινοπροπεν-1-διόλη-1,1 με σύντομο συντακτικό τύπο: CH3C(NH2=C(OH)2.
- 3-αμινοπροπεν-1-διόλη-1,1 με σύντομο συντακτικό τύπο: H2NCH2CH=C(OH)2.
- 1-αμινοπροπεν-2-διόλη-1,1 με σύντομο συντακτικό τύπο: CH2=CHC(NH2)(OH)2.
- 2-αμινοπροπεν-2-διόλη-1,1 με σύντομο συντακτικό τύπο: CH2=C(NH2CH(OH)2.
- 3-αμινοπροπεν-2-διόλη-1,1 με σύντομο συντακτικό τύπο: H2NCH=CHCH(OH)2 (σε δύο (2) γεωμετρικά ισομερή).
- 1-αμινοπροπεν-1-διόλη-1,2 με σύντομο συντακτικό τύπο: CH3C(OH)=C(NH2)OH (σε δύο (2) γεωμετρικά ισομερή).
- 3-αμινοπροπεν-1-διόλη-1,2 με σύντομο συντακτικό τύπο: H2NCH2C(OH)=CHOH (σε δύο (2) γεωμετρικά ισομερή).
- 1-αμινοπροπεν-2-διόλη-1,2 με σύντομο συντακτικό τύπο: CH2=C(OH)CH(NH2)OH (σε δύο (2) οπτικά ισομερή).
- 3-αμινοπροπεν-2-διόλη-1,2 με σύντομο συντακτικό τύπο: H2NCH=C(OH)CH2OH (σε δύο (2) γεωμετρικά ισομερή).
- 1-αμινοπροπεν-1-διόλη-1,3 με σύντομο συντακτικό τύπο: HOCH2CH=C(NH2)OH (σε δύο (2) γεωμετρικά ισομερή).
- 2-αμινοπροπεν-1-διόλη-1,3 με σύντομο συντακτικό τύπο: HOCH2C(NH2)=CHOH (σε δύο (2) γεωμετρικά ισομερή).
- 1-αμινοπροπεν-2-διόλη-1,3 με σύντομο συντακτικό τύπο: HOCH=CHCH(NH2)OH (σε τέσσερα στερεοϊσομερή: δύο (2) γεωμετρικά + δύο (2) οπτικά).
- 1-υδροξυπροπεν-1-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: CH3CH=C(OH)NHOH (σε δύο (2) γεωμετρικά ισομερή).
- 2-υδροξυπροπεν-1-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: CH3C(OH)=CHNHOH (σε δύο (2) γεωμετρικά ισομερή).
- 3-υδροξυπροπεν-1-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: HOCH2CH=CHNHOH (σε δύο (2) γεωμετρικά ισομερή).
- 1-υδροξυπροπεν-2-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: CH2=CHCH(OH)NHOH (σε δύο (2) οπτικά ισομερή).
- 2-υδροξυπροπεν-2-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: CH2=C(OH)CH2NHOH.
- 3-υδροξυπροπεν-2-υδροξυλαμίνη-1 με σύντομο συντακτικό τύπο: HOCH=CHCH2NHOH (σε δύο (2) οπτικά ισομερή).
- Υδροξυπροπεν-1-υδροξυλαμίνη-2 με σύντομο συντακτικό τύπο: CH3C(NHOH)=CHOH (σε δύο (2) γεωμετρικά ισομερή).
- Υδροξυπροπεν-2-υδροξυλαμίνη-2 με σύντομο συντακτικό τύπο: CH2=C(NHOH)CH2OH.
- Μεθυλαμινοαιθενοδιόλη-1,1 με σύντομο συντακτικό τύπο: CH3NHCH=C(OH)2.
- Μεθυλαμινοαιθενοδιόλη-1,2 με σύντομο συντακτικό τύπο: HOCH=C(NHCH3)OH.
- Βινυλαμινομεθανοδιόλη με σύντομο συντακτικό τύπο: CH2=CHNHCH(OH)2
- Ν-μεθυλο-1-υδροξυαιθενοϋδροξυλαμίνη με σύντομο συντακτικό τύπο: CH2=C(OH)N(OH)CH3.
- Ν-μεθυλο-2-υδροξυαιθενοϋδροξυλαμίνη με σύντομο συντακτικό τύπο: HOCH=CHN(OH)CH3 (σε δύο (2) γεωμετρικά ισομερή).
- Υδροξυμεθυλαμινοαιθενόλη με σύντομο συντακτικό τύπο: CH2=CΗNHCH2OH.
- 1-αμινο-2-μεθοξυαιθενόλη με σύντομο συντακτικό τύπο: CH3OCH=C(NH2)OH (σε δύο (2) γεωμετρικά ισομερή).
- 2-αμινο-1-μεθοξυαιθενόλη με σύντομο συντακτικό τύπο: H2NCH=C(OCH3)OH (σε δύο (2) γεωμετρικά ισομερή).
- 1-(αμινομεθοξυ)αιθενόλη με σύντομο συντακτικό τύπο: CH2=C(OCH2NH2)OH.
- 2-(αμινομεθοξυ)αιθενόλη με σύντομο συντακτικό τύπο: H2NCH2OCH=CHOH (σε δύο (2) γεωμετρικά ισομερή).
- 1-μεθοξυαμινοαιθενόλη με σύντομο συντακτικό τύπο: CH2=C(NHOCH3)OH.
- 2-μεθοξυαμινοαιθενόλη με σύντομο συντακτικό τύπο: CH3ONHCHCHOH (σε δύο (2) γεωμετρικά ισομερή).
- Αιθενοξυαμινομεθανόλη με σύντομο συντακτικό τύπο: CH2=CΗΟCH(NH2)OH (σε δύο (2) οπτικά ισομερή).
- 1-μεθοξυαιθενυδροξυλαμίνη με σύντομο συντακτικό τύπο: CH2=C(OCH3)NOH.
- 2-μεθοξυαιθενυδροξυλαμίνη με σύντομο συντακτικό τύπο: CH3OCH=CHNOH (σε δύο (2) γεωμετρικά ισομερή).
- 2-ιμινοπροπανοδιόλη-1,1 με σύντομο συντακτικό τύπο: CH3C(=NH)CH(OH)2.
- 3-ιμινοπροπανοδιόλη-1,1 με σύντομο συντακτικό τύπο: HN=CHCH2CH(OH)2.
- 1-ιμινοπροπανοδιόλη-1,2 με σύντομο συντακτικό τύπο: CH3CH(OH)C(=NH)OH (σε δύο (2) οπτικά ισομερή).
- 3-ιμινοπροπανοδιόλη-1,2 με σύντομο συντακτικό τύπο: HN=CHCH(OH)CH2OH (σε δύο (2) οπτικά ισομερή).
- Ιμινοπροπανοδιόλη-1,3 με σύντομο συντακτικό τύπο: HOCH2C(=NH)CH2OH.
- 1-υδροξυπροπανυδροξυλιμίνη-1 με σύντομο συντακτικό τύπο: CH3CH2C(OH)=NOH.
- 2-υδροξυπροπανυδροξυλιμίνη-1 με σύντομο συντακτικό τύπο: CH3CH(OH)CH=NOH (σε δύο (2) οπτικά ισομερή).
- 3-υδροξυπροπανυδροξυλιμίνη-1 με σύντομο συντακτικό τύπο: HOCH3CH2CH=NOH.
- Υδροξυπροπανυδροξυλιμίνη-2 με σύντομο συντακτικό τύπο: CH3C(=NOH)CH2OH.
- Μεθυλιμινοαιθανοδιόλη-1,1 με σύντομο συντακτικό τύπο: CH3N=CHCH(OH)2
- Μεθυλιμινοαιθανοδιόλη-1,2 με σύντομο συντακτικό τύπο: HOCH2C(=NCH3)OH.
- Ν-υδροξυμεθυλοαιθανιμίνη με σύντομο συντακτικό τύπο: CH3CH=NCH2OH.
- 2-μεθοξυ-1-ιμινοαιθανόλη με σύντομο συντακτικό τύπο: CH3OCH2C(=NH)OH.
- 1-μεθοξυ-2-ιμινοαιθανόλη με σύντομο συντακτικό τύπο: HN=CHCH(OCH3)OH (σε δύο (2) οπτικά ισομερή).
- 2-μεθοξυ-2-ιμινοαιθανόλη με σύντομο συντακτικό τύπο: HN=C(OCH3CH2OH.
- 1-μεθοξυαιθανυδροξυλιμίνη με σύντομο συντακτικό τύπο: CH3C(OCH3)=NOH.
- 2-μεθοξυαιθανυδροξυλιμίνη με σύντομο συντακτικό τύπο: CH3OCH2CH=NOH.
- 1-(μεθοξυϊμινο)αιθανόλη με σύντομο συντακτικό τύπο: CH3C(=NOCH3)OH.
- 2-(μεθοξυϊμινο)αιθανόλη με σύντομο συντακτικό τύπο: CH3ON=CHCH2OH.
- Αιθυλιμινομεθανοδιόλη με σύντομο συντακτικό τύπο: CH3CH2N=C(OH)2.
- (1-υδροξυαιθυλιμινο)μεθανόλη με σύντομο συντακτικό τύπο: CH3CH(OH)N=CHOH (σε δύο (2) οπτικά ισομερή).
- (2-υδροξυαιθυλιμινο)μεθανόλη με σύντομο συντακτικό τύπο: HOCH2CH2N=CHOH.
- Ν-(1,1-διυδροξυαιθυλο)μεθανιμίνη με σύντομο συντακτικό τύπο: CH3C(OH)2)N=CH2.
- Ν-(1,2-διυδροξυαιθυλο)μεθανιμίνη με σύντομο συντακτικό τύπο: HOCH2CH(OH)N=CH2 (σε δύο (2) οπτικά ισομερή).
- Ν-(2,2-διυδροξυαιθυλο)μεθανιμίνη με σύντομο συντακτικό τύπο: (HO)2CHCH2N=CH2.
- N-(1-υδροξυαιθυλ)ιμινομεθανόλη με σύντομο συντακτικό τύπο: CH3CH(OH)N=CHOH (σε δύο (2) οπτικά ισομερή).
- N-(2-υδροξυαιθυλ)ιμινομεθανόλη με σύντομο συντακτικό τύπο: HOCH2CH2N=CHOH.
- 1-αιθοξυϊμινομεθανόλη με σύντομο συντακτικό τύπο: CH3CH2OC(=NH)OH.
- N-αιθοξυϊμινομεθανόλη με σύντομο συντακτικό τύπο: CH3CH2ON=CHOH.
- N-(1-υδροξυαιθοξυ)μεθανιμίνη με σύντομο συντακτικό τύπο: CH3CH(OH)ON=CH2 (σε δύο (2) οπτικά ισομερή).
- N-(2-υδροξυαιθοξυ)μεθανιμίνη με σύντομο συντακτικό τύπο: HOCH2CH2ON=CH2.
- N-(μεθοξυμεθυλο)ιμινομεθανόλη με σύντομο συντακτικό τύπο: CH3OCH2N=CHOH.
- N-(μεθοξυδροξυμεθυλο)μεθανιμίνη με σύντομο συντακτικό τύπο: CH3OCH(OH)N=CH2 (σε δύο (2) οπτικά ισομερή).
- N-(υδροξυμεθοξυμεθυλο)μεθανιμίνη με σύντομο συντακτικό τύπο: ΗΟCH2OCH2N=CH2.
- 1,1-διμεθοξυμεθανιμίνη με σύντομο συντακτικό τύπο: CH3OC(=NH)OCH3.
- 1,Ν-διμεθοξυμεθανιμίνη με σύντομο συντακτικό τύπο: CH3OCH=NOCH3.
- 1-(ιμινομεθοξυ)αιθανόλη με σύντομο συντακτικό τύπο: HN=CHOCH(OH)CH3 (σε δύο (2) οπτικά ισομερή).
- 2-(ιμινομεθοξυ)αιθανόλη με σύντομο συντακτικό τύπο: HN=CHOCH2CH2OH.
- Αιθοξυμεθανυδροξυλιμίνη με σύντομο συντακτικό τύπο: CH3CH2OCH=NOH.
- Αιθοξυϊμινομεθανόλη με σύντομο συντακτικό τύπο: CH3CH2ON=CHOH.
- 2-αμινο-2-υδροξυπροπανάλη με σύντομο συντακτικό τύπο: CH3C(NH2)(OH)CHO (σε δύο (2) οπτικά ισομερή).
- 3-αμινο-2-υδροξυπροπανάλη με σύντομο συντακτικό τύπο: H2NCH2CH(OH)CHO (σε δύο (2) οπτικά ισομερή).
- 2-αμινο-3-υδροξυπροπανάλη με σύντομο συντακτικό τύπο: HOCH2CH(NH2)CHO (σε δύο (2) οπτικά ισομερή).
- 2-αμινο-2-υδροξυπροπανάλη με σύντομο συντακτικό τύπο: HOCH(NH2)CH2CHO (σε δύο (2) οπτικά ισομερή).
- 1-αμινο-1-υδροξυπροπανόνη με σύντομο συντακτικό τύπο: CH3COCH(NH2)OH (σε δύο (2) οπτικά ισομερή).
- 3-αμινο-1-υδροξυπροπανόνη με σύντομο συντακτικό τύπο: H2NCH3COCH2OH.
- Μεθυλοαμινο-2-υδροξυαιθανάλη με σύντομο συντακτικό τύπο: CH3NHCH(OH)CHO (σε δύο (2) οπτικά ισομερή).
- Μεθυλοαμινο-N-υδροξυαιθανάλη με σύντομο συντακτικό τύπο: CH3N(OH)CH2CHO.
- Υδροξυμεθυλαμιναιθανάλη με σύντομο συντακτικό τύπο: ΗΟCH2NΗCH2CHO.
- Αμινομεθοξυαιθανάλη με σύντομο συντακτικό τύπο: CH3OCH(NH2)CHO (σε δύο (2) οπτικά ισομερή).
- (Αμινομεθοξυ)αιθανάλη με σύντομο συντακτικό τύπο: H2NCH2OCH2CHO.
- Μεθυλαμινοξυαιθανάλη με σύντομο συντακτικό τύπο: CH2NHOCH2CHO.
- Αλανίνη ή 2-αμινοπροπανικό οξύ με σύντομο συντακτικό τύπο: CH3CH(NH2)COOH (σε δύο (2) οπτικά ισομερή).
- Σαρκοζίνη ή μεθυλαμιναιθανικό οξύ με σύντομο συντακτικό τύπο: CH3NHCH2COOH.
- Αιθυλαμινομεθανικό οξύ με σύντομο συντακτικό τύπο: CH3CH2NHCOOH.
- Διμεθυλαμινομεθανικό οξύ με σύντομο συντακτικό τύπο: (CH3)2NCOOH.
- 2-υδροξυπροπαναμίδιο με σύντομο συντακτικό τύπο: CH3CH(OH)CONH2 (σε δύο (2) οπτικά ισομερή).
- 3-υδροξυπροπαναμίδιο με σύντομο συντακτικό τύπο: HOCH2CH2CONH2.
- Προπανυδροξυλαμίδιο με σύντομο συντακτικό τύπο: CH3CH2CONHOH.
- Υδροξυαιθανομεθυλαμίδιο με σύντομο συντακτικό τύπο: HOCH2CONHCH3.
- Αιθανομεθυλυδροξυλαμίδιο με σύντομο συντακτικό τύπο: CH3CON(OH)CH3.
- Αιθαν(υδροξυμεθύλ)αμίδιο με σύντομο συντακτικό τύπο: CH3CONCH2OH.
- Μεθοξυαιθαναμίδιο με σύντομο συντακτικό τύπο: CH3OCH2CONH2.
- 2-αμινοκυκλοπροπανοδιόλη-1,1 με σύντομο συντακτικό τύπο:
- 1-αμινοκυκλοπροπανοδιόλη-1,2 με σύντομο συντακτικό τύπο:
- 3-αμινοκυκλοπροπανοδιόλη-1,2 με σύντομο συντακτικό τύπο:
- 1-υδροξυκυκλοπροπανυδροξυλαμίνη με σύντομο συντακτικό τύπο:
- 2-υδροξυκυκλοπροπανυδροξυλαμίνη με σύντομο συντακτικό τύπο:
- Κυκλοπροπανοδιυδροξυλαμίνη με σύντομο συντακτικό τύπο:
- 1,2,3-διοξαζιδίνη με σύντομο συντακτικό τύπο:
- 1,2,4-διοξαζιδίνη με σύντομο συντακτικό τύπο:
- 1,3,2-διοξαζιδίνη με σύντομο συντακτικό τύπο:
- 1,3,4-διοξαζιδίνη με σύντομο συντακτικό τύπο:
- 1,3,5-διοξαζιδίνη με σύντομο συντακτικό τύπο:
- 1,4,2-διοξαζιδίνη με σύντομο συντακτικό τύπο:
Δομή[Επεξεργασία | επεξεργασία κώδικα]
Είναι το απλούστερο β-αμινοξύ.
| Δεσμοί[1] | ||||
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
|---|---|---|---|---|
| C-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C#3-C#2 | σ | 2sp3-2sp3 | 154 pm | |
| C#2-C#1 | σ | 2sp3-2sp2 | 151 pm | |
| C-N | σ | 2sp3-2sp3 | 152 pm | 6% C+ Ν- |
| Ν-H | σ | 2sp3-1s | 101,7 pm | 17% N- H+ |
| C=O | σ | 2sp2-2sp2 | 132 pm | 19% C+ O- |
| π | 2p-2p | |||
| C-O | σ | 2sp2-2sp3 | 147 pm | 19% C+ O- |
| O-H | σ | 2sp3-1s | 96 pm | 32% O- H+ |
| Κατανομή φορτίων σε ουδέτερο μόριο | ||||
| -O | -0,51 | |||
| -N | -0,40 | |||
| =O | -0,38 | |||
| C#2 | -0,06 | |||
| C#3 | -0,03 | |||
| H(CH) | +0,03 | |||
| H(NH2) | +0,17 | |||
| H(OH) | +0,32 | |||
| C#1 | +0,57 | |||
Παραγωγή β-αλανίνης[Επεξεργασία | επεξεργασία κώδικα]
Από β-αλοπροπανικό οξύ[Επεξεργασία | επεξεργασία κώδικα]
2. Μέσω οργανομαγνησιακών ενώσεων και αλαμίνης με εστεροποίηση για «προστασία»[3] της καρβοξυλομάδας[4]:
3. Με φθαλιμιδικό κάλιο (σύνθεση Gabriel)[5]:
Αντίδραση Stracker[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση υδροκυανίου (HCN) και αμμωνίας (NH3) σε εποξυαιθάνιο[6]:
Με αναγωγική αμμωνίωση 2-φορμυλαιθανικού οξέος[Επεξεργασία | επεξεργασία κώδικα]
Με αναγωγική αμμωνίωση 2-φορμυλαιθανικού οξέος[7]::
Με αναγωγή β-νιτροπροπανικού οξέος[Επεξεργασία | επεξεργασία κώδικα]
Από β-νιτροπροπανικό οξύ με αναγωγή[8]:
- Το β-νιτροαιθανικό οξύ παράγεται από Β-αλοπροπανικό οξύ:
Από ηλεκτρικό οξύ[Επεξεργασία | επεξεργασία κώδικα]
Από ηλεκτρικό οξύ με μετροπή σε μονοαμίδιο και αποικοδόμηση-μετάθεση Hofmann[9]:
Από β-αμινοπροπανονιτρίλιο[Επεξεργασία | επεξεργασία κώδικα]
Από β-αμινοπροπανονιτρίλιο με υδρόλυση:
- Το β-αμινοπροπανονιτρίλιο παράγεται από αιθένιο με επίδραση κυαναμίδιου:
Χημικές ιδιότητες και παράγωγα[Επεξεργασία | επεξεργασία κώδικα]
Αμφολυτική αυμπεριφορά[Επεξεργασία | επεξεργασία κώδικα]
1. Η πιο χαρακτηριστική είναι η αμφολυτική διάστασή της:
- Η κεντρική πάνω κατάσταση ισχύει για αδιάλυτη (ή διαλυτή σε απρωτικούς διαλύτες) αλανίνη.
- Σε υδατικά διαλύματα:
- Για pH<pK1 ιονίζεται η αμινομάδα (δεξιά).
- Για pH=pI ιονίζονται και η αμινομάδα και η καρβοξυλομάδα (κένρο κάτω).
- Για pH>pK2 ιονίζεται μόνο η καρβοξυλομάδα (αριστερά).
2. Παραγωγή αλάτων με οξέα και βάσεις. Π.χ.:
και
Εστεροποίηση[Επεξεργασία | επεξεργασία κώδικα]
Αντιδρά με αλκοόλες σχηματίζοντας αμινεστέρες. Αποτελεί και μέθοδο «προστασίας»[10] της καρβοξυλομάδας.
Αλκυλίωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση αλκυλοαλογονιδίων σχηματίζονται δευτεροταγή αμινοξέα:
Ακυλίωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση ακυλοαλογονιδίων σχηματίζονται δευτεροταγή αμιδοξέα. Αποτελεί και μέθοδο «προστασίας»[10] της αμινομάδας, αφού τα αμίδια υδρολύονται.
Απαζώτωση[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση νιτρώδους οξέος πρακτικά αντικαθίστανται η αμινομάδα με υδροξυλομάδα. Παράγεται 3-υδροξυπροπανικό οξύ:
Βιοχημικοί ρόλοι[Επεξεργασία | επεξεργασία κώδικα]
Η β-αλανίνη δεν μετέχει στη βιοσύνθεση καμμιάς σημαντικής πρωτεΐνης ή ενζύμου. Συνθέται, ωστόσο, «εν ζωή» (in vivo) με αποικοδόμιση της δεϋδρουρακίλης και της καρνοσίνης. Επίσης, σχηματίζει πεπτίδια όπως την καρνοσίνη, την ανσερίνη, καθώς και το παντοθεμικό οξύ (βιταμίνη B5) που είναι τμήμα του συνενζύμου Α. Κάτω από φυσιολογικές συνθήκες, η β-αλανίνη μεταβολίζεται σε αιθανικό οξύ.
Η β-αλανίνη είναι ένα (σχετικά) σπάνιο συστατικό της καρνοσίνης και αυτό σημαίνει συνήθως ότι το επίπεδο συγκέντερωσης της πρώτης (β-αλανίνης) ρυθμίζει (ουσιαστικά) το επίπεδο συγκέντερωσης της δεύτερης (καρνοσίνης). Γι' αυτό, συμπλήρωμα έξτρα β-αλανίνης αυξάνει τη συγκέντρωση της καρνοσίνης στους μύες, ελατώνει το λίπος στους αθλητές και αυξάνει τη γύμνασή τους[11][12].
Τυπικά, έχουν γίνει μελέτες για στρατηγικές χορήγησης πολλαπλών δόσεων 400–800 mg β-αλανίνης σε κανονικά χρονικά διαστήματα ως και 8, για περιόδους 4-10 εβδομάδων. Μετά από τη στρατηγική χορήγησης των 10 εβδομάδων, αναφέρθηκε αύξηση της ενδομυϊκής καρνοσίνης κατά ένα μέσο όρο 80,1% (με διακύμανση 18-205%)[12][13] .
Η L-ιστιδίνη, με pKa = 6,1 είναι ένας σχετικά αδύναμος παράγοντας ρύθυμισης της φυσιολογικής ενδομυϊκής διακύμανσης του pH. Ωστόσο, όταν συνδέεται σε πεπτίδια με άλλα αμινοξέα, ο παράγοντας αυτός αυξάνεται πιο κοντά στο 6,8-7,0. Ειδικότερα, όταν η L-ιστιδίνη σχηματίζει διπεπτίδιο με υη β-αλανίνη το pKa του διπεπτίδιου γίνεται 6,83[14], οπότε γίνεται ένας πολύ πιο αποτελεσματικός παράγοντας. Επιπλέον, επειδή η β-αλανίνη ως β-αμινοξύ δεν συνεργάζεται με τις πρωτεΐνες μπορεί, με το σχηματισμό των διπεπτιδίων με την L-ιστιδίνη, να αποθηκευθεί σε σχετικά υψηλές συγκεντώσεις (στην τάξη των mmole). Σε παρουσία 17-25 mmole/kg (ξηρού μυός),[15], η κσρνοσίνη (που είναι β-αλανυλο-L-ιστιδίνη) είναι ένας σημαντικός ενδομυϊκός ρυθμιστής, συνεισφέροντας σε ένα ποσοστό 10-20% στη συνολική ρυθμιστική χωρητικότητα στις μυϊκές ίνες τύπων I και II.
Ακόμη και ασθενέστερη από τη γλυκίνη, η β-αλανίνη είναι ένας ανταγωνιστής ως προς την τελευταία στο να γίνει ένας συναρμοτής για τη στρυχνίνη (με σειρά ικανότητας γλυκίνη >> β-αλανίνη > ταυρίνη > L-αλανίνη - L-σερίνη > προλίνη).[16].
Ως γλυκαντικό[Επεξεργασία | επεξεργασία κώδικα]
Ένα υψηλού δυναμικού τεχνητό γλυκαντικό, που ονομάζεται σουσάν, είναι παράγωγο της β-αλανίνης[17].
Κίνδυνοι υπερβολικής δόσης[Επεξεργασία | επεξεργασία κώδικα]
Η β-αλανίνη παρέχεται σε διάλυμα ή σε σκόνη σε καψούλες ζελατίνης, αλλά μπορεί να προκαλέσει παραισθησία όταν λαμβάνεται σε δόσεος πάνω από 10 mg/kg σωματικού βάρους (bwt) [13]. Αυτό όμως κυμαίνεται ανάμεσα στα διαφορετικά άτομα: Σε ορισμένα πιο ευαίσθητα, τα συμπτώματα γίνονται αισθητά από τα 10 mg/kg bwt, στην πλειοψηφία γίνονται αισθητά από τα 20 mg/kg bwt και μερικά πιο ανθεκτικά χρειάζονται συγκέντρωση 40 mg/kg, για να αρχίσουν να νοιώθουν τα συμπτώματα υπεβολικής δόσης[13]. Ωστόσο, ενέσινμες δόσεις 40 mg/kg β-αλανίνης, αλλά σε διπεπτίδια με L-ιστιδίνη σε κοτόπουλα δεν προκάλεσαν παραισθησία[13] .
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 243, §10.2Α.
- ↑ Προσωρινή κάλυψη χαρακτηριστικής ομάδας για την αποφυγή παραγωγής ανεπιθύμητων παραπροϊόντων.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 298, §13.3Α1, σελ. 243, §10.2B4 και σελ. 301. §13.4.αII.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 329, §14.2.1.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 329, §14.2.2.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 329, §14.2.3.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 243, §10.2B2α.
- ↑ «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982, σελ. 298, §13.3Α1, σελ. 296, §13.2Αα, §13.2Γ1, σελ. 243, §10.2B3 και σελ. 301. §13.4.αII.
- ↑ 10,0 10,1 Προστασία ονομάζεται η προσωρινή δέσμευση μιας χαρακτηριστικής ενεργής ομάδας, ώστε αυτή να μη δώσει ανεπιθύμητες αντιδράσεις και παράγωγα με την επίδραση αντιδραστηρίων που σκοπεύουμε να χρησιμοποιήσουμε πάνω στην ένωση με σκοπό να αξιοποιήσουμε μια άλλη ομάδα και να πάρουμε τα επιθυμητά αποτελέσματα-παράγωγα. Μετά απελευθερώνουμε ή αποπροστατεύουμε την αρχική ομάδα, δηλαδή φροντίζουμε να απομακρυνθεί η ομάδα που την προστάτεψε προσωρινά.
- ↑ Derave W, Ozdemir MS, Harris R, Pottier A, Reyngoudt H, Koppo K, Wise JA, Achten E. (August 9, 2007). «Beta-alanine supplementation augments muscle carnosine content and attenuates fatigue during repeated isokinetic contraction bouts in trained sprinters». J Appl Physiol 103 (5): 1736. doi:. PMID 17690198.
- ↑ 12,0 12,1 Hill CA, Harris RC, Kim HJ, Harris BD, Sale C, Boobis LH, Kim CK, Wise JA. (2007). «Influence of beta-alanine supplementation on skeletal muscle carnosine concentrations and high intensity cycling capacity». Amino Acids 32 (2): 225–33. doi:. PMID 16868650.
- ↑ 13,0 13,1 13,2 13,3 Harris, RC; Tallon, MJ; Dunnett, M; Boobis, L; Coakley, J; Kim, HJ; Fallowfield, JL; Hill, CA και άλλοι. (2006). «The absorption of orally supplied β-alanine and its effect on muscle carnosine synthesis in human vastus lateralis». Amino Acids 30 (3): 279–289. doi:. PMID 16554972.
- ↑ Bate-Smith, EC (1938). «The buffering of muscle in rigor: protein, phosphate and carnosine». Journal of Physiology 92 (3): 336–343. PMID 16994977.
- ↑ Mannion, AF; Jakeman, PM; Dunnett, M; Harris, RC; Willan, PLT (1992). «Carnosine and anserine concentrations in the quadriceps femoris muscle of healthy humans». Eur. J. Appl. Physiol 64: 47–50. doi:. https://archive.org/details/sim_european-journal-of-applied-physiology_1992-01_64_1/page/47.
- ↑ Encyclopedia of Life Sciences Amino Acid Neurotransmitters. Jeremy M Henley, 2001 John Wiley & Sons, Ltd. DOI: 10.1038/npg.els.0000010 Article Online Posting Date: April 19, 2001
- ↑ ChemIDplus, « Aspartic acid-beta-4-nitroanilide - RN:102-66-9 » on chem.sis.nlm.nih.gov, U.S. National Library of Medicine.
Βιβλιογραφία[Επεξεργασία | επεξεργασία κώδικα]
- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ ΈκδοσηΘεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Διαδικτυακοί τόποι που αναφέρονται στις «Αναφορές και παρατηρήσεις».
| ||||||||



![{\displaystyle \mathrm {XCH_{2}CH_{2}COOH+ROH{\stackrel {-H_{2}O}{\overrightarrow {\longleftarrow }}}XCH_{2}CH_{2}COOR{\xrightarrow[{|Et_{2}O|}]{+Mg}}XMgCH_{2}CH_{2}COOR{\xrightarrow[{-MgX_{2}}]{+NH_{2}X}}H_{2}NCH_{2}CH_{2}COOR{\stackrel {+H_{2}O}{\overrightarrow {\longleftarrow }}}H_{2}NCH_{2}CH_{2}COOH+ROH} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/a781ac40c010d319eac43c563f0d2fe341302159)

![{\displaystyle \mathrm {+XCH_{2}CH_{2}COOH{\xrightarrow[{+2H_{2}O}]{-KBr}}H_{2}NCH_{2}CH_{2}COOH+} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/d927d2c9a766857d5e3f5db6fba60e86f8928edb)


![{\displaystyle \mathrm {OCHCH_{2}COOH+2NH_{3}{\xrightarrow {-H_{2}O}}HN=CHCH_{2}CCOONH_{4}{\xrightarrow[{Ni}]{+H_{2}}}H_{2}NCH_{2}CH_{2}COONH_{4}{\xrightarrow {+HCl}}H_{2}NCH_{2}CH_{2}COOH+NH_{4}Cl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/343f9a50d1741ed93c2bd95cc472682c76619c93)















